阅读:0
听报道
编者按
2017年9月13日,《新英格兰医学杂志》在线发表(10月5日纸质版)“悲剧、坚持和机遇——CAR-T疗法的故事”(Tragedy, Perseverance, and Chance — The Story of CAR-T Therapy)。《NEJM医学前沿》邀请到美国南卡罗莱纳医科大学李子海教授撰写述评,解读CAR-T历史、进展和挑战。《知识分子》获授权转载。《NEJM医学前沿》将于10月13日在其app和官网发表综述的中译全文。
撰文 | 李子海(美国南卡医科大学医学微生物学和免疫学教授)
● ● ●
众所周知,肿瘤免疫治疗和其它治疗的根本区别在于它利用人体自身的免疫系统来攻击肿瘤。免疫治疗有特异、持久(免疫记忆)、适应性强的特点,而且它的效果和应用往往不取决于肿瘤病理分型,被认为是癌症的克星和治疗癌症的关键。从概念上来讲,免疫治疗是现代医学肿瘤学的一个革命,一个转折点[1]。
近五年来,肿瘤免疫治疗的药物和手段也显现出爆炸性的增长,包括CTLA-4,PD-1和PD-L1等T细胞检查点抑制剂[2],新抗原疫苗,融瘤病毒,以及细胞治疗(包括CAR-T,T细胞共激活因子,白细胞介素)等等;此外,肿瘤免疫治疗还有各种各样的联合疗法。
这里最具有戏剧性的发展是最近被美国食品药品管理局(FDA)批准的治疗难治复发的急性淋巴细胞白血病(急淋;ALL)25岁以下患者的CAR-T19细胞治疗[3]。
在2017年10月5日出版的《新英格兰医学杂志》(NEJM)上,医生记者(physician correspondent)Lisa Rosenbaum回顾了CAR-T19细胞治疗的发展历史及挑战[4]。如果CAR-T19的发展是一部戏的话,那么这部戏的主要演员是病人、免疫学家、医生和人类最精华的精神:乐观、坚持和追求知识与生命的执着。这一过程中的喜怒哀乐,最终带来人类征服癌症无限的希望。

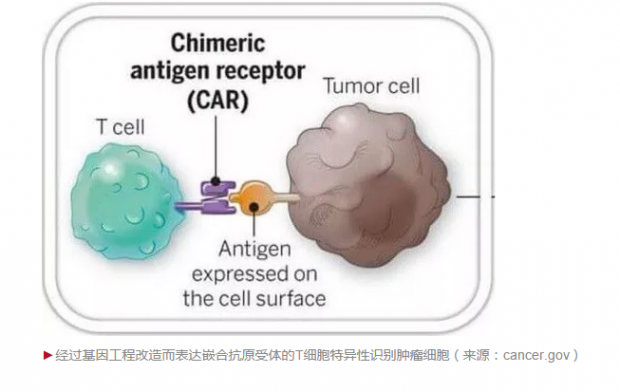
2010年,5岁的急淋患者Emily Whitehead,在多方诊治无效的情况下,成为了接受宾大(宾夕法尼亚大学)和诺华(Novartis)CAR-T19治疗的第一位儿童病人。CAR是嵌合抗原受体(Chimeric Antigen Receptor)的英文缩写[5]。这个CD19-CAR嵌合抗原受体的细胞表面的一端(氨基端)是抗B细胞分化分子CD19的单链抗体,细胞内的另一端(羧基端)是活化T细胞的两个信号的共价键联接:4-1BB和CD3δ。
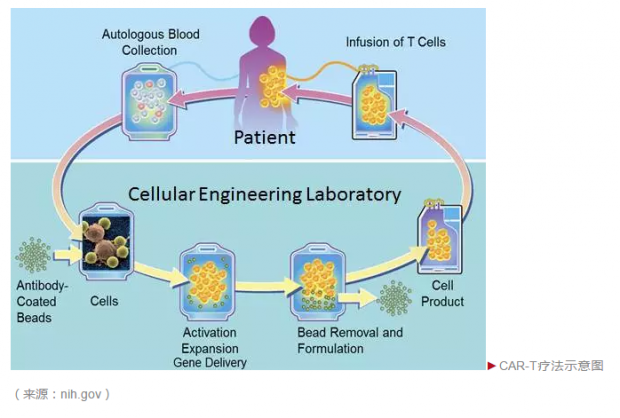
CAR-T19治疗先把病人自身周围血T细胞分离出来,再通过逆转录病毒载体把CD19-CAR分子高量稳定地在T细胞表达。这样一个表达CD19-CAR的T细胞,输入体内后会识别B细胞(正常及白血病B细胞),被激活后通过直接杀伤或其分泌的细胞因子而消灭B细胞。
在这篇《新英格兰医学杂志》文章里,Rosenbaum描写了Emily起死回生并成为美国精准医学和癌症登月计划象征的故事,讲述了宾大Carl June教授团队的创造力、艰辛和幸运,CAR-T19这种有生命药物的特殊性及CAR-T19定价高达47万美元的社会经济问题。她最终得出两个结论:
(1)机遇永远青睐有准备的人;
(2)FDA对CAR-T19的批准意味着人类攻克癌症征程中拉开的新的一幕。
那么,现在大家对CAR-T技术最关心的热点是什么?
Carl June教授的贡献
June是肿瘤内科的医生科学家,曾拜师于诺贝尔奖获得者Edward Donnall Thomas做骨髓移植专科训练,一生中一直专攻细胞治疗。CAR-T的概念由以色列的免疫学家Zelig Eshhar在1993年提出并证明。当时,Eshhar的论文也只是出于科学家的好奇——用抗体取代T细胞的受体看是否可激活T细胞[6]。

June的最大贡献是细胞工程学,这与他早期决心制造抵制艾滋病病毒的T细胞有重大关系。他证明了T细胞激活需要CD28等共激活分子[7],而且经逆转录病毒载体修饰的T细胞可以在人体内安全存活12年以上[8]。更重要的是,June使得CD19-CAR治疗急淋从概念变为现实[3],这也是他和很多著名过继性细胞治疗免疫学家(包括Steven A. Rosenberg,Philip D. Greenberg,Michel Sadelain等)的最大区别。
CAR-T19的神奇之处
FDA对CAR-T19的批准是基于国际多个肿瘤中心参与的2期临床试验。参与试验的63个病人资料齐全,都是25岁以下难治复发的急淋病人。83%的病人在接受治疗3个月时骨髓癌细胞彻底消除。除了宾大和诺华CAR-T19,Kite和Juno公司的产品对B细胞癌症也有类似的效果。同时,世界各地包括中国在内的众多医院也在不同规模上重复了CAR-T19的临床疗效[9]。
那么,CAR-T19为什么如此有效?这可能与以下几个因素有关:第一,CD19是最佳抗原,除B细胞以外,其它细胞没有表达;第二,B细胞有免疫耐受的作用,去除B细胞后有可能有助T细胞的活化及记忆力产生[10];第三,和实体瘤不同,B细胞癌症的微环境更有利于免疫反应;最后,B细胞癌症也可能对一些细胞因子异常敏感。
CAR-T19的前景
当然CAR-T19疗效是不是持久,能不能成为治疗急淋等B细胞癌症的一线治疗,只有时间才能回答这些问题。与此同时,二代、三代CAR-T19研发竞争已很激烈[5]。需要克服的问题包括,如何减低细胞因子风暴及脑水肿等严重的副作用,如何降低产品成本和费用,以及如何普及CAR-T19治疗等等。
把本来是个体化的CAR-T19细胞变成所有病人都能拿来直接使用的产品,将会对CAR-T领域有很大的冲击。基因编辑的技术已经成熟[11,12],可以通这个方法把T细胞内源受体和组织相容抗原去掉,这样的CAR-T所有病人都可以用,输入体内不会被排斥。现在,概念和技术已经摆在我们面前,就看谁能像Carl June一样把它很快变成临床现实。
中国在CAR-T技术的贡献和挑战
现在使用CAR-T最多的国家,不是美国,而是中国[9]。中国有患者,有智慧,有资源。尤其是在生物工程很浓的CAR-T领域,中国一定会有突出的贡献。现在的关键是监管部门如何引导这个领域,使得CAR-T更标准化,科学化和国际化。
在此,我提出以下几点,供大家参考:
第一,CAR-T是一种药物,应该用与药物相同的方式监管。
第二,可以考虑建立一个庞大的患者数据库。所有使用CAR-T的医院及研究单位可以把治疗患者的情况和CAR-T的特征等资料放到这个公开的数据库,这样会起到CAR-T 领域里同行自动调节和约束的效果。
第三,加强与国外的沟通与合作。比方说,如果诺华的CAR-T19想打入中国市场,到底如何做?这是不可避免的问题。
最后,赢得世人尊重的不是仿制药,而是创新药。近两年来,中国科学家利用针对BCMA分子的CAR-T治疗骨髓瘤取得的成果就是一个例子[13]。
CAR-T技术对实体瘤的作用
大家最关心的是CAR-T在实体瘤治疗中的前景。这里特别需要克服肿瘤抗原特异性的困难。对于抗原而言,研究人员已经尝试过用Her2和mesothelin做靶点,但它们导致了致命的副作用,原因是正常细胞对这些抗原也有不同程度的表达。那么与肿瘤相关的病毒,如乙肝病毒、HPV和EBV病毒等,其抗原在肿瘤细胞表面特异表达,它们是不是最佳的选择呢?很多此类临床试验也正在进行。当然,肿瘤特异性的驱动癌变的突变分子应该是理想的抗原。中枢角质母细胞瘤有一部分病人有表皮生长因子受体(EGFR)的突变,从而产生一个真正的肿瘤特异性的受体, 叫EGFR variant III(EGFRvIII)。早期临床实验证明,针对EGFRvIII的CAR-T没有特殊的毒性,值得更进一步探讨[14]。
另外,实体瘤的免疫耐受微环境是不可忽视的因素。免疫检查点的抑制剂和CAR-T的联合应用有可能对实体瘤更重要。
就像Lisa Rosenbaum 所说,CAR-T19 的今天归功于一代代科学家的高瞻远瞩和辛勤耕耘,病人,免疫学家,所有临床医护人员及工业界的希望和永不罢休的精神。战胜癌症需要全人类的努力。
作者简介

李子海,美国南卡医科大学(MUSC)医学微生物学和免疫学教授,系主任,Hollings癌症中心肿瘤免疫负责人,美国华裔血液和肿瘤学家专家协会(CAHON)主席,美国临床研究协会(ASCI)的当选成员,白血病和淋巴瘤协会临床学者,美国临床肿瘤协会(ASCO)免疫治疗的轨道负责人。在纽约爱因斯坦医学院完成内科住院医培训,获得美国医生证书;在西雅图Fred Hutchinson肿瘤中心做内科肿瘤学专科培训,成为美国内科协会指定认可的肿瘤学专家。主要从事肿瘤免疫治疗,调节性T细胞生物学,先天免疫,免疫耐受,热休克蛋白疫苗和生物学等方面的研究,并在这些领域取得卓越成果。
参考文献
[1] Li Z, Chen L, Rubinstein MP. Cancer immunotherapy: are we there yet? Exp Hematol Oncol 2013;2:33.
[2] Wang J, Yuan R, Song W, et al. PD-1, PD-L1 (B7-H1) and Tumor-Site Immune Modulation Therapy: The Historical Perspective. J Hematol Oncol 2017;10:34.
[3] American Association for Cancer Research. First-Ever CAR T-cell Therapy Approved in U.S. Cancer Discov 2017 Sep 8. doi:10.1158/2159-8290.CD-NB2017-126. [Epub ahead of print].
[4] Rosenbaum L. Tragedy, Perseverance, and Chance - The Story of CAR-T Therapy. N Engl J Med 2017;377:1313-15.
[5] Lim WA, June CH. The principles of engineering immune cells to treat cancer. Cell 2017;168:724-40.
[6] Gross G, Waks T, Eshhar Z. Expression of immunoglobulin-T-cell receptor chimeric molecules as functional receptors with antibody-type specificity. Proc Natl Acad Sci USA 1989;86:10024-8.
[7] June CH, Bluestone JA, Nadler LM, et al. The B7 and CD28 receptor families. Immunol Today 1994;15:321-31.
[8] Scholler J, Brady TL, Binder-Scholl G, et al. Decade-long safety and function of retroviral-modifiedchimeric antigen receptor T cells. Sci Transl Med 2012;4:132ra53.
[9] Luo C, Wei J, Han W. Spotlight on chimericantigen receptor engineered T cell research and clinical trials in China. Sci China Life Sci 2016;59:349-59.
[10] Mauri C, Bosma A. Immune regulatory function of B cells. Annu Rev Immunol 2012;30:221-41.
[11] Qasim W, Zhan H, Samarasinghe S, et al.Molecular remission of infant B-ALL after infusion of universal TALEN gene-edited CAR T cells. Sci Transl Med 2017;9:pii:eaaj2013.
[12] Eyquem J, Mansilla-Soto J, Giavridis T,et al. Targeting a CAR to the TRAC locus with CRISPR/Cas9 enhances tumour rejection. Nature 2017;543: 113-7.
[13] Mikkilineni L, Kochenderfer JN. Chimeric antigen receptor T-cell therapies for multiple myeloma. Blood 2017 Sep 19. pii:blood-2017-06-793869. doi: 10.1182/blood-2017-06-793869. [Epub ahead of print].
[14] O'Rourke DM, Nasrallah MP, Desai A, et al. A single dose of peripherally infused EGFRvIII-directed CAR T cells mediates antigen loss and induces adaptive resistance in patients with recurrent glioblastoma. Sci Transl Med 2017;9:pii: eaaa0984.
版权信息
本文由《NEJM医学前沿》编辑部负责翻译及编写,内容以英文原版为准,中译全文由马萨诸塞州医学会NEJM集团独家授权。欢迎转发至朋友圈,如需转载,请联系collaboration@nejmqianyan.cn。未经授权的翻译是侵权行为,版权方将保留追究法律责任的权利。
Copyright ©2017 Jiahui Medical Research and Education Group. All Rights Reserved

话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。



 京公网安备 11010502034662号
京公网安备 11010502034662号 