阅读:0
听报道

► Photo by Drew Hays on Unsplash
编译 | 韩东升
责编 | 叶水送
● ● ●
对于肿瘤免疫药物来说,没有哪种药物的研发能比它更能吸引眼球。
2017年5月27日,美国食品药物管理局(FDA)批准美国默克公司(Merck)研发的抗癌新药Keytruda用于治疗微卫星不稳定的实体瘤,这一广谱抗肿瘤药被生物科技风险投资大神Bruce Booth称为是“爆炸级超新星”药物。
Keytruda是一种阻断PD-1受体分子的人源化单克隆抗体。临床试验表明,Keytruda至少对十余种癌症有效,是首个不分肿瘤类别的抗癌药物。
研发过程艰难而曲折
Keytruda的研发过程充满了曲折和偶然性。该研发项目最初并非是为了筛选抗癌抗体药物,在后来默克公司的并购过程中,该项目甚至曾被默克公司强制关停,直到最后时刻才被重新重视,并被视为可以与对手百时美施贵宝公司(BMS)竞争的重要项目。
但从长远看来,它的研发成功也是必然的。因为药物开发不只靠运气,更需要优秀的人才:有能力使项目不断推进的研发带头人,以及重视和投资项目的高级管理层。
最初,该抗体药物由荷兰Oss公司(阿克苏诺贝尔公司的健康产品部门)位于剑桥的Organon团队筛选出的。项目始于2003年,最初在安德烈·范·埃尔萨斯(Andrea van Elsas)的实验室里进行。
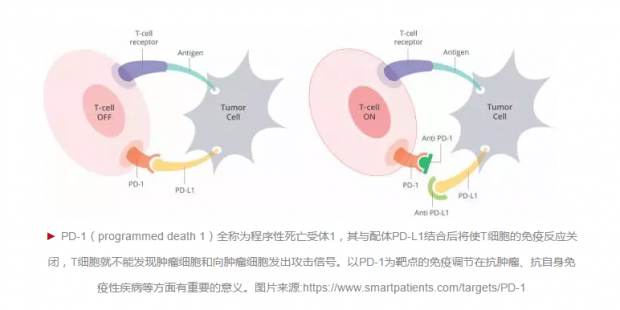
据介绍,该抗体研发的初衷并非用于治疗癌症,他们最初的希望是通过筛选PD-1的抗体找到激活PD-1受体的激动剂,从而关闭T细胞的免疫反应,达到治疗免疫反应过激的自身免疫性疾病(类风湿关节炎等)。但出乎意料的是,该小组最终并没有筛选出良好的PD-1激动剂,却筛选到了PD-1的抑制剂。当时肿瘤免疫疗法还存在很多争议和不确定性,Organon团队并没有意识到该抗体在抗癌领域的巨大潜力。
并购中惨遭冷遇
Organon团队成功制备人源化单克隆抗体Pembro(Keytruda)后,下一步准备进行新药申报(IND)。不幸的是,随着2007年Organon被先灵葆雅公司(Schering Plough)收购,IND申请也被搁置下来。
当时肿瘤学对于PD-1免疫疗法的研究并无太多报道,先灵葆雅公司并不看好该项目,但幸运的是该项目继续由安德烈·范·埃尔萨斯负责,在其带领下该项目不断取得新的进展。2009年,当他们准备进行第二次新药申报时,却不幸被再次收购。这一次远没有上次那么幸运,默克公司管理层直接把该项目定为低优先级,并随后停止了该项目。
巨大转机
一切似乎都要结束了。但在2010年,BMS公司在《新英格兰医学杂志》(NEJM)上发表的一项研究使该项目迎来了巨大转机。研究中介绍了BMS公司CTLA4抑制剂药物ipilimumab(Yervoy)的最新研究,CTLA4是另一种T细胞抑制剂分子,与PD-1类似。研究中称该药物已成功进入三期临床,暗示着免疫细胞疗法中“检查位点抑制剂”方案的可行性。后来默克公司又得知BMS公司通过收购Medarex获得了一种靶向PD-1分子的抑制剂药物: nivolumab。
一切都在暗示着单抗Keytruda的巨大商业价值。默克管理层及时醒悟,迅速组织对Keytruda的新药申请(IND),并计划在2010年底提交申请。
Keytruda如期进入一期临床试验。最初,默克公司根据已有的结果先筛选出一批对PD-1免疫疗法可能产生反应的黑色素瘤(melanoma)患者,然后对其进行试验。这一点是值得借鉴的,也为默克公司与BMS公司竞争赢得了信心。
令人惊喜的是,7名患者中,6名对药物产生反应。如此高的反应率是前所未有的,给了项目组成员巨大的鼓舞,也给了默克集团赶超BMS公司的机会。临床试验的关键成员安东尼·里巴斯(Antoni Ribas)曾因担心患者人数不够导致一期临床试验中断而彻夜未眠。
但他的担心无疑是多余的,在默克公司高层的重视和安排下,一期临床的试验人数包含了655名黑色素瘤患者以及约650名肺癌患者,是肿瘤学上已有的最大规模一期临床试验。
策略至上
此次Keytruda的研发历程对于默克公司是前所未有的,因为BMS公司早在四年前已提交了对Opdivo的新药申请,对默克公司来说这意味着存在巨大的风险。但默克公司已制备了极具竞争性的研发方案,不甘放弃这次大好机遇。
为了与对手BMS公司竞争,默克公司采取极具挑战性的试验方案:主要选取对之前所有治疗方法都未产生反应的黑色素瘤患者进行临床试验,当然也包括使用了BMS公司新药Yervoy的患者。如果方案产生不错的效果,不仅可以增强Keytruda的竞争力,也可以为之后Keytruda得到快速批准打下基础。
全力冲刺
默克公司在它的成功路上还有一个王牌。2012年,非临床安全主管Joseph DeGeorge曾在FDA工作13年,他从FDA前同事那里了解到FDA正在计划实施一种称为突破性疗法认定(BTD)的政策,旨在使新药的批准更加合理和快速。默克公司及时抓住这一重要机遇,于2013年一月秘密组织了对新药Keytruda的BTD申请,而且为了避免打草惊蛇,没有对外部发布任何消息。
最初,默克的研发落后于BMS公司好几年,对于默克公司来说,要想赢得这场硬仗,需要相对更加集中的投入。默克研发总监Roger Perlmutter认为Keytruda绝对是一款值得自己甚至整个默克公司全身心投入研发的药物。他告诉研究中心的每个人:停下你手头的工作,开始集中精力做Keytruda相关的工作。
当他被问及与Keytruda相关的一系列临床试验项目的优先顺序时,他说:“全都要做!”Perlmutter无疑是有远见和魄力的,当他看到Keytruda已有的临床数据结果时,感觉到其绝非等同于传统的抗癌药物,并相信其将对整个肿瘤治疗界造成巨大冲击。
之后约翰·霍普金斯癌症研究所的研究者与默克公司合作,用Keytruda药物证明了PD-1免疫疗法对于微卫星不稳定(MSI-H)的多种癌症有效。排除千难万险,加上默克公司高效的行动力,最终在2017年5月,成为首个可以治疗多种癌症的药物。
经验总结
在默克公司抗癌药物Keytruda上市的整个过程中,可以总结出以下几点经验:
1. 实验室中重要的研究发现在最后获得审批上市之前,往往还有很长的路要走;
2. 新药研发中不确定性极大,随着时间的推移,可能暴露出各种问题,也可能存在各种机遇;
3. 要及时关注药品监管政策的变化,并处理好与监管部门的关系;
4. 灵活选择合适的策略,为研发赢得竞争力和时间;
5. 最重要的,药物研发需要有能力的研究者来推进研究,也需要有远见和魄力的公司管理层人士为其保驾护航。
文章来源:
https://www.forbes.com/sites/davidshaywitz/2017/07/26/the-startling-history-behind-mercks-new-cancer-blockbuster/3/#260c9faa3f6f

话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。



 京公网安备 11010502034662号
京公网安备 11010502034662号 