撰文 | 王承志
责编 | 冯水寒
液体活检技术可能是近年来临床上发展最快的检验方法之一,通过检测血液或尿液等无创的方式,对癌症等疾病做出诊断。这项技术被《麻省理工科技评论》评选为“2015年十大突破技术”,同时也进入世界经济论坛评出的“2017年度全球十大新兴技术榜单”。
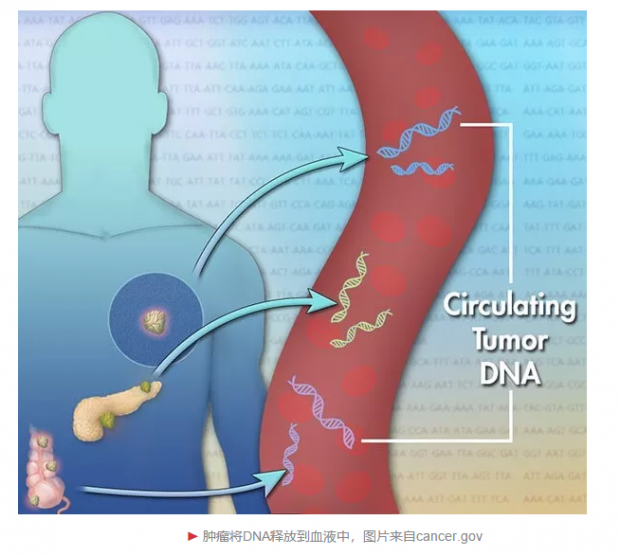
检测血液中含量极少的循环肿瘤DNA(ctDNA,Circulating Tumor DNA)是目前液体活检领域最为火热的检测方法。由于体内肿瘤细胞坏死后有少量DNA(其往往携带肿瘤细胞突变或重组的基因,能反映肿瘤细胞的准确信息)会进入循环系统,因而可以利用DNA扩增或高通量测序等技术检测并计数。同时,该方法具有无创的特点,可以早期、廉价且多次获得体内肿瘤DNA的信息,目前正以极快的速度被临床广泛接受。
但由于该方法在临床上推广的速度过于迅猛,使得针对该方法的临床有效性等相关研究未能及时跟上。近日,美国临床肿瘤学会(ASCO)和美国病理医师学会(CAP)组织了专家委员会(以下简称委员会)联合对已经发表的1338篇临床ctDNA检测的论文进行了综述分析,认为当下的液体活检技术临床有效性非常有限,并对该领域提出框架性意见,相关研究发表在权威期刊Journal of Clinical Oncology杂志上。

该综述从分析效度(analytical validity)、临床有效性(clinical validity)和临床效用(clinical utility)三个方面评价了ctDNA检测方法。其中,分析效度是指是否能准确可靠地从测序数据中发现目标突变的能力;临床有效性是指是否能准确地检测到某个病理阶段的存在,或者对不同检测结果的群体做出预测;临床效用是指是否有足够证据表明进行该项检测会对病人的生存带来益处。
目前发表的与ctDNA分析效度相关的研究都是通过比较肿瘤组织和血浆中致病突变的一致性,进而得出结论,但有很多生物学因素可能影响这种一致性(比如肿瘤类型、肿瘤异质性、组织和血液取样时间等)。因此,委员会认为以后该类型的研究需要以标准样品(含有已知突变信息的样品,比如含1% EGFR T790M突变的样品、单次检测样品中含有10个突变)作为对照。此外,不同类型肿瘤突变的最低检测丰度目前也没有系统性的研究。委员会建议该领域进行大规模的跨平台比较研究,为临床医师提供准确的分析效度参考。
而对于晚期肿瘤病例,液体活检的临床效用可以通过两种范式来检测。一种是比较可靠的前瞻性临床实验,但目前还没有任何这类实验报道;另一种是评估ctDNA是否能和组织活检提供相同的信息。目前,只有一种基于基因扩增(PCR)的检测方法在非小细胞肺癌EGFR突变体检验中获得了美国和欧洲的批准。有关证据表明,虽然EGFR ctDNA检测阳性可以很好地指导后续治疗,但结果阴性的病人仍然需要做组织活检,因为ctDNA阴性病人在组织检测中发现阳性相当常见。此外,其它类型的肿瘤ctDNA检测的临床有效性研究鲜有报道。委员会认为,未来需要包含尽可能符合相同标准的病人队列以及从前瞻性研究中根据特定标准,严格筛选的样品,来研究ctDNA检测的临床有效性和临床效用。
ctDNA检测的另一个用途是动态检测肿瘤效果,比如在治疗的不同时间点对ctDNA进行定量分析。一些小规模的研究对这一方法进行了验证,能够从一定程度上显示ctDNA水平和肿瘤对药物响应的相关性。此外,也有研究表明ctDNA能够比影像学更早地发现耐药突变。但委员会认为,目前还没有可靠的证据证明ctDNA对肿瘤动态检测的临床有效性。对于临床期待的ctDNA检测对早期肿瘤的筛查,委员会认为其临床有效性证据相当有限,也没有任何证据表明ctDNA检测对病人预后和花费有改善。
总的来说,这项综述性研究为当前大红大紫的ctDNA液体活检带来更为理性的分析和思考。正如任何其它检测方法一样,液体活检也需要大规模的队列研究来确定其对不同疾病的有效性和敏感性。在激进的临床应用背后,扎实的临床有效性和临床效用评价也需要及时跟上。而对该领域的研究人员和商业公司来说,这项报告也是一份及时的提示,为液体活检更好地应用指明了方向。
参考文献
Merker J D, Oxnard G R, Compton C, et al. Circulating Tumor DNA Analysis in Patients With Cancer: American Society of Clinical Oncology and College of American Pathologists Joint Review[J]. Journal of Clinical Oncology, 2018: JCO. 2017.76. 8671.

0
推荐



 京公网安备 11010502034662号
京公网安备 11010502034662号 