宫颈癌是唯一有可能被消除的癌症 | 图源:
导 读
2020年世界卫生大会决议通过的《启动加速消除宫颈癌全球战略》指出,到2030年需实现以下三项目标:90%的女孩在15岁之前完成HPV(人乳头瘤病毒)疫苗接种;70%的妇女在35岁和45岁之前接受高效检测方法筛查;90%确诊宫颈疾病的妇女得到治疗。
作为世界上人口最多的国家,我国肩负沉重的HPV相关癌症负担,且宫颈癌在中国的发病率和死亡率仍在逐年攀升。今年以来,我国内蒙古鄂尔多斯、广东深圳、四川成都、江苏无锡、山东济南、福建厦门等城市陆续启动或宣布启动HPV疫苗免费接种项目。
HPV疫苗加速免费接种,距离我们消除宫颈癌还有多远?
撰文 | 柴逸涵
责编 | 刘楚
2021年3月,全国爱卫办、健康中国办公室发布 “健康城市” 计划,正式把宫颈癌防治纳入考核指标。
“健康中国” 行动具体目标包括:至2025年底,在试点地区常住人口实现15岁前适龄女孩的人乳头瘤病毒(HPV)疫苗人群接种覆盖率>90%、在35岁和45岁接受高精度宫颈癌筛查的比例>70%、宫颈癌及癌前病变患者规范治疗率>90%。
目前,国内15个健康中国行动创新模式试点城市中,内蒙古鄂尔多斯、广东深圳、四川成都、江苏无锡、山东济南、福建厦门等6个城市都已启动或宣布启动HPV疫苗免费接种项目。
这距离我国宣布将全力支持世界卫生组织(WHO)提出的《加速消除宫颈癌全球战略》仅一年时间,但由于负担重、起步晚,据国家癌症中心、中国医学科学院肿瘤医院流行病学室主任赵方辉教授团队今年在 BMC Medicine 杂志上发表的研究文章显示,通过对国内宫颈癌防控现状进行量化分析发现,当前我国离消除宫颈癌的目标存在巨大差距,如不改变防控策略,在宫颈癌发病率快速增长的背景下实现消除目标几乎不可能 [2]。
正如肿瘤流行病学家乔友林所言,一方面社会对于HPV疫苗的认可度很高,甚至自费接种常出现 “一苗难求” 的现象;另一方面HPV 疫苗的组织实施策略都集中于城市及学校,而农村地区尤其是人口分散的边远地区的需求则大多未被充分重视。
1、试点城市和国产HPV疫苗的加速之路
作为健康中国创新模式试点城市之一,自2020年9月份起厦门市率先在全省范围内为学籍在厦门的13周岁至14周岁半的在校女生,实施为期三年的国产二价宫颈癌疫苗自愿免费接种。
2021年4月,内蒙古自治区鄂尔多斯全市HPV疫苗免费接种项目正式启动,各旗县根据安排陆续开始接种工作,组织该市13~18岁女性免费接种三针HPV疫苗,民众仅需缴纳接种服务费,即可在本市定点医疗机构实施接种。作为全国早期开展宫颈癌筛查预防的地区之一,鄂尔多斯市在2020年就在准格尔旗率先开展了 “关爱女生健康进校园” 项目,截至今年4月,在准格尔旗将近一万名13~18岁女生中,已有近85%的人免费接种了HPV疫苗。
济南市也明确提出,将于2025年实现以下目标:15岁之前适龄女孩HPV疫苗接种率达到90%以上,35~45岁妇女宫颈癌规范筛查覆盖率达到70%以上,宫颈癌及癌前病变规范治疗率达到90%以上。
今年10月,广东省印发《广东省适龄女生人乳头瘤病毒(HPV)疫苗免费接种工作方案(2022—2024年)》,指出将自2022年9月起,将对具有广东省学籍、9月起新进入初中一年级未接种过HPV疫苗的14周岁以下女生进行HPV疫苗免费接种。
11月15日,成都市多部门下发《成都市宫颈癌综合防控HPV疫苗接种实施方案(2021年版)》。方案明确,对于当年13-14岁的在校女学生,学生家长(监护人)可以在国产/进口双价和进口四价HPV疫苗中自主选择,由财政资金给予600元/人的疫苗接种补助,补助后的疫苗费差额和疫苗接种服务费(20元/剂)由受种者家长(监护人)承担。
11月22日,江苏生无锡市发布《无锡市适龄女生HPV疫苗群体性免疫实施方案》,将通过HPV疫苗群体性免疫策略的实施,实现市区常住人口中初二年级女生HPV疫苗接种率达90%以上。预计政府每年将为HPV疫苗免费接种投入近1000万元,该项目也将列入2022年政府为民办实事项目。
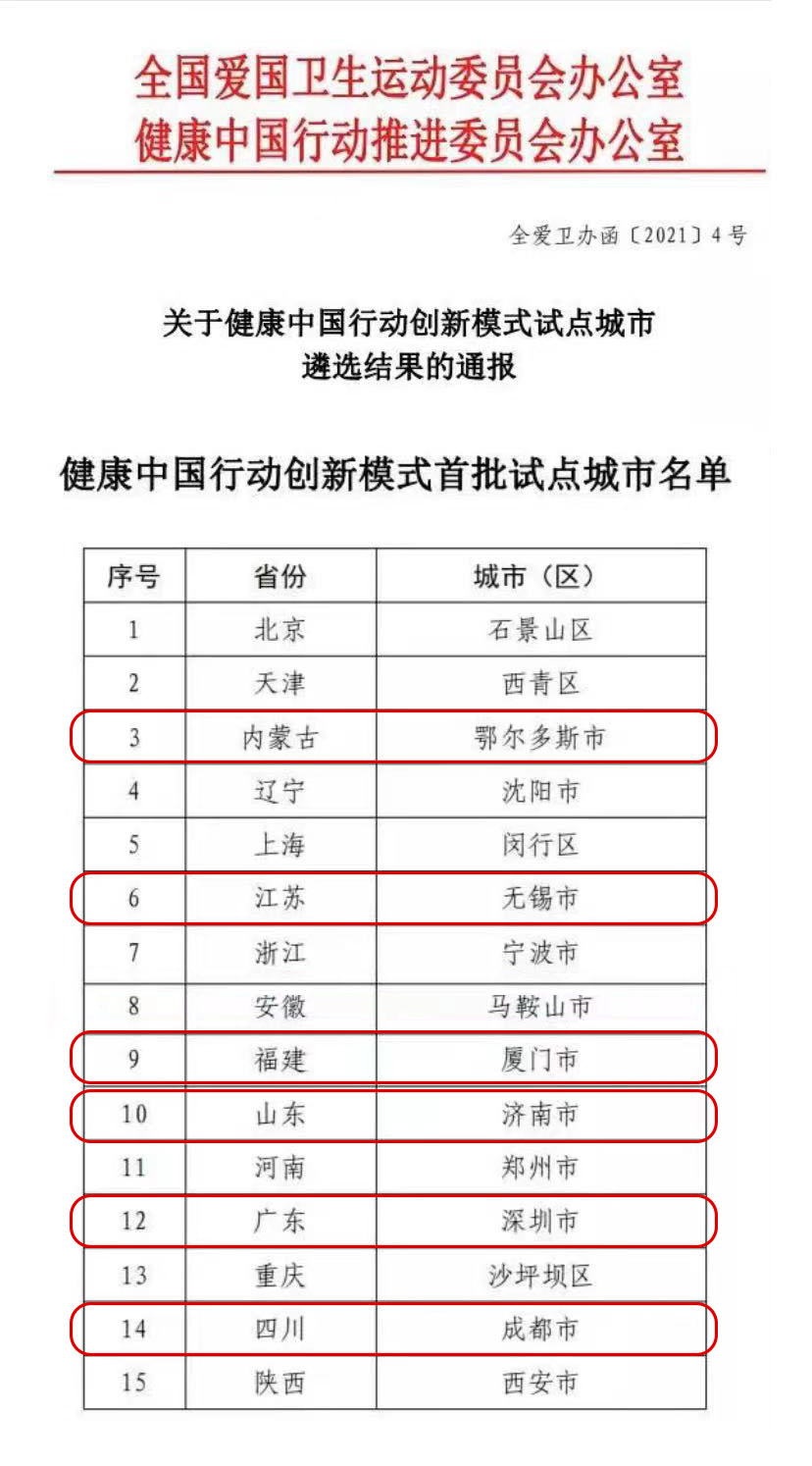
图1 首批试点城市已有6个启动HPV免费接种项目
除了预防接种在各地相继被纳入免疫规划,HPV疫苗在生产研发上也进展迅速。
2021年10月18日,世卫组织官方网站公布的信息显示,由厦门万泰沧海生物技术有限公司制造生产的二价HPV疫苗(商品名 “馨可宁”)获得世卫组织预认证,成为首个获得该认证的由中国生产的宫颈癌疫苗产品。
2020年,馨可宁的获批上市使得疫苗短缺情况有所改善。据中国食品药品检定研究院数据测算,该疫苗累计批签发约350万支。对9~14岁人群来说,相比此前已获批的HPV疫苗,馨可宁只需要接种两针剂,成为国内唯一获批二针法的HPV疫苗。发表在《中国科学:生命科学》的相关临床试验数据 [3] 显示,9~14岁女性接种两剂HPV疫苗后,血清阳转率达到了100%,并且抗体水平高于接种三剂的18~26岁成年女性。
接种剂次的减少,除了在接种程序上更为方便外,也对疫苗短缺情况起到一定的缓解效果。换言之,在同等产量的情况下,两针剂让更多女性能够得到疫苗保护。
2021年10月17日,北京神州细胞生物技术集团股份公司自主研发的全球首个14价HPV疫苗SCT1000临床II期研究于顺利启动。SCT1000覆盖WHO认定的全部12个高危致癌的HPV病毒型和2个导致尖锐湿疣的HPV病毒型,对宫颈癌的保护性预计累计增加到96%。
除此之外,很多疫苗厂商的疫苗也都相继投入临床研究。截至今年4月,国内共有9家企业申报的18项HPV疫苗获批可以进行临床试验,包含 2价、3价、4价、6价、 9价、11价和14价HPV疫苗产品,其中9价以上疫苗临床试验申请就有8个。
然而,中国作为世界人口第一大国,是宫颈癌新发病例最多的国家,情势依然非常严峻,宫颈癌防治任务任重道远。
2、唯一有希望被消除的癌症
宫颈癌(cervical cancer)是导致女性癌症相关死亡的第四大常见原因。据估计,2020年,全球约有60.4万新确诊病例,34.2万人死亡 [4]。
人乳头瘤病毒(HPV)是世界范围内一组极为常见的病毒,有100多种类型,其中至少有14种可引起癌症。而宫颈癌是迄今为止最常见的与人乳头状瘤病毒有关的疾病,几乎所有的宫颈癌病例都可以追溯到人乳头状瘤病毒感染。
2006年,默沙东公司和葛兰素史克公司生产的宫颈癌疫苗面世,一年之内,包括美国、英国、加拿大和澳大利亚等在内的80个国家先后批准了这种疫苗的使用。
《英国医学杂志》(BMJ)于2019年4月发表的一项研究[5]发现,对年龄在12~13岁的苏格兰女孩进行HPV疫苗常规接种,可以显著降低她们宫颈疾病发病率,特别是16型和18型HPV的患病率从30.0%(95%置信区间(confidence interval,CI)26.9~33.1)大幅降低到4.5%(95%CI 3.5~5.7),疫苗有效性为89.1%(95%CI 85.1~92.3)。
研究人员还发现,即便是未接种疫苗的妇女,宫颈疾病发病率也有所减少,原因可能是由于群体保护的效应。据研究 [6] 显示,自2008年开始接种HPV疫苗之后,苏格兰的HPV病毒感染水平已经下降了90%,或将使苏格兰妇女的宫颈癌病例减少90%。
今年11月发表于《柳叶刀》的研究 [7] 再次证明,在英国,开始于2008年的HPV疫苗接种计划取得了成功,数据表明接种疫苗的人群中宫颈癌的发病率大幅降低,进一步支持了疫苗的有效性。具体而言,在12~13岁(首次性行为之前)接种HPV疫苗,宫颈癌发病率比之前未接种疫苗的几代人降低87%;在14~16岁时接种疫苗,宫颈癌发病率降低62%;在16~18岁时接种,发病率降低34%。
2018年发表在 Clinical Infectious Diseases 上的一项研究 [8] ,对丹麦、冰岛、挪威和瑞典四个北欧国家的四价HPV疫苗的长期有效性进行了长达12年的随访考察。数据显示,HPV疫苗的有效性至少在10年内都保持在90%以上,并且,随着时间的推移,疫苗呈现继续有效的趋势。
在HPV疫苗上市十多年之后,其有效性和安全性已经获得了多项研究的证明,因此世界卫生组织(WHO)始终呼吁各国将HPV疫苗纳入免疫规划范畴,即给适龄女性免费接种HPV疫苗。
多项研究发现,在HPV的感染途径中,男性也扮演了极其重要的角色。
HPV广泛存在于男性的生殖道中,尤其是前列腺——它也是造成前列腺癌的原因之一 [9]。除此之外,HPV病毒还会引起男性的其他相关癌症,包括口咽癌、肛门癌、阴茎癌和生殖器疣等。
美国疾病防御和控制中心的数据显示,在美国,人乳头状瘤病毒相关癌症新增病例中,平均每年有约2.1万女性和1.5万男性。男性病例中,79.7%因HPV罹患口咽癌,14.2%患肛门癌,6.1%患阴茎癌。
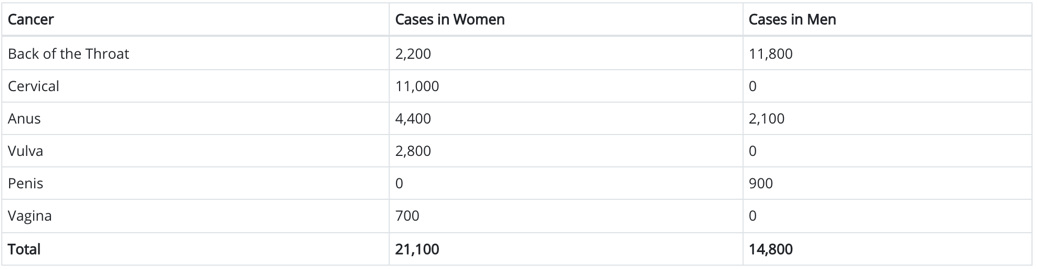
图2 美国每年由 HPV 引起的癌症数量,2020年8月统计 | 图源[10]
男性接种HPV疫苗不仅可以保护自己不被感染和引发相关疾病,而且可以降低携带病毒的几率,更有助于保护女性。
所以,一些国家也把男性纳入接种范围。2011年,美国开始为11~12岁男孩接种。2019年,英国政府宣布HPV疫苗接种计划覆盖范围将从女孩扩展至男孩。[11]
与所有疫苗一样,HPV疫苗的接种覆盖率也呈现着不均衡的态势,在发达国家之外的许多国家和地区,HPV疫苗依然未能免费,甚至因为产量的问题使得自费接种也 “一苗难求”。
2020年11月,世界卫生组织启动《加速消除宫颈癌全球战略》,宣布全球194个国家将共同寻求在2030年实现90%的女孩在15岁前完成HPV疫苗接种、70%的妇女在35岁和45岁之前接受高效检测方法筛查和90%确诊宫颈疾病的妇女得到治疗的计划目标。这是全球范围内首次承诺将力争消除一种癌症。
截至日前,全球已有110个国家和地区,包括卢旺达等部分低收入国家,将HPV疫苗纳入国家免疫规划(免费接种),超过75个国家和地区对9~14岁女孩采用两剂次免疫程序。在疫苗接种覆盖率高的国家和地区,HPV感染率和宫颈癌前病变的发病率下降达到90%。
3、HPV疫苗接种被耽误的那些年
虽然消除宫颈癌的措施已得到研究充分证实,但其仍未在世界上疾病负担高的区域得到广泛实施。在低收入和中等收入国家,宫颈癌的发病率几乎是高收入国家的两倍,死亡率更甚,是高收入国家的三倍。
我国也面临诸多挑战,包括个人对宫颈癌的防治意识不强、疫苗价格过高、人口基数大导致疫苗供应不足、区域经济与卫生水平发展不平衡、预防与治疗条件有限等 [12]。
大众对于未知发生的事情存在普遍的侥幸心理,更多人选择生病之后治病,而不是提前接种预防。疫苗的过高价格也让不少人望而却步。最突出问题则是疫苗供应严重不足。
在此之前,世界上第一支HPV疫苗在中国上市的时间比国外整整晚了10年。
2017年,中国加入国际人用药品注册技术协调会(ICH),并开始接受境外临床试验数据。2018年,九价HPV疫苗也作为第一批以境外临床试验数据递交并审批通过的进口药物。
而在此之前,所有进口药物必须在中国本地人群开展临床试验,跨国药企葛兰素史克(GSK)和默沙东分别在2008年底和2009年才开始在中国招募临床试验志愿者,又经过数年的研发、数据递交、审查不通过、再次递交等流程,二价和四价HPV疫苗分别直到2016和2017年才在国内上市。
好处是,在疫苗上市的十多年后,一些发达国家和地区在对疫苗、筛查与治疗策略的践行在已取得优秀成果,或可为我国提供防控经验。
澳大利亚是最早将HPV疫苗纳入国家免疫规划的国家之一,自2007年开始为12~13岁的女孩免费接种佳达修四价疫苗(分3剂次),并在2013年将12~13岁的男孩也被纳入接种范围。2016年,在15岁及以上青少年中,三剂次完整接种的疫苗覆盖率在女孩中达到了78.6%,在男孩中达到了72.9%。2018年,接种疫苗及程序变更为佳达修九价疫苗二剂次。
澳大利亚自1991年引入国家宫颈癌筛查项目,在2011~2015年间平均筛查覆盖率达到了83%。2017年12月,澳大利亚转变筛查策略,为25~69岁妇女每5年进行一次HPV检测,直到70~74岁。专家预计,澳大利亚有望在2028年实现消除目标,并且在 2034 年将宫颈癌死亡率降到1/10万以下。
在非洲,2010年,默沙东公司与卢旺达政府达成合作,为卢旺达适龄女孩提供免费HPV疫苗。2011年4月,该项目正式启动,卢旺达成为世界上第一个承诺为每一位适龄女孩提供免费HPV疫苗接种的低收入国家。[13]
该项目为小学六年级女孩提供三剂次免费接种,并且在2012~2013年分别为中学三年级的女孩进行补接种,以此保证所有青春期前和青春期女孩均能接种HPV疫苗。2014年以后,则只为六年级女孩免费接种疫苗;2015年以后,转变为两剂次接种。
除了基于学校的免疫接种方案以外,对于未能进入学校学习的12岁女孩,项目也通过社区服务为其接种疫苗。2013年以后,全球疫苗免疫联盟(GAVI)成为卢旺达HPV疫苗的主要资助方,通过共同融资模式支持卢旺达的HPV计划,大幅降低疫苗使用费用,使更多女性有机会接种疫苗。每剂疫苗GAVI支付4.5美元,卢旺达仅需要支付20美分,是前者的零头。
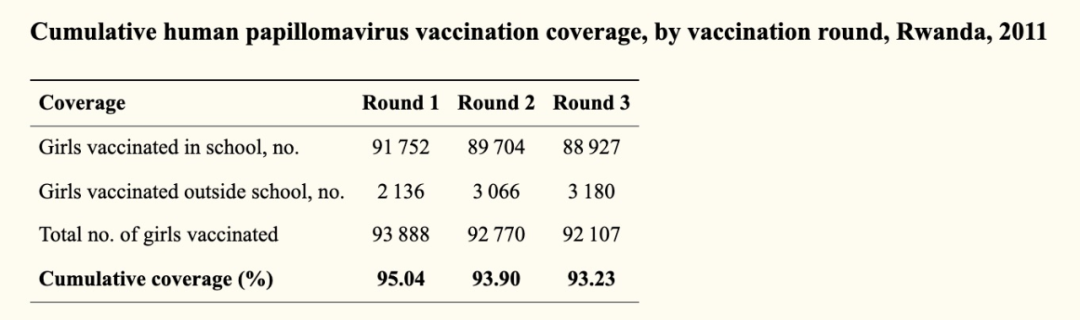
图3 2011年卢旺达的累计人乳头瘤病毒疫苗接种覆盖率 | 图源[14]
上述项目的开展,使得在卢旺达,完整接种三剂次的疫苗覆盖率在 2011年即达到了93%,2012~2013年持续升至97%。自2011至2018年,共有115.7万名适龄卢旺达女孩成功接种第一针HPV疫苗,相当于该国适龄女孩的98%。这无疑是巨大的成功。
卢旺达的HPV疫苗项目有诸多值得推广的经验,包括在项目正式推行之前通过报纸、杂志、广播、电视等多媒体开展大量相关宣传和健康教育活动,进行多中心、多部门、跨领域合作,争取稳定的资金支持和疫苗供应,采纳基于学校的接种方案,依据实际情况灵活在 “依据年级” 和 “依据年龄” 两种接种方式间的切换;同时采用“多阶段疫苗接种策略”,动员社区力量,使未能上学的女孩也能顺利接种。
作为世界上人口最多的国家,我国肩负沉重的HPV相关癌症负担,且宫颈癌在中国的发病率和死亡率仍在逐年攀升。
2009年,农村 “两癌”(宫颈癌和乳腺癌)检查项目启动,其中宫颈癌筛查已在全国覆盖至2 118个县区,累计为1亿余人次的35~64岁(其中2009—2011年的1 000万筛查任务针对35~59岁)农村女性提供了免费的宫颈癌检查。2019年,农村女性 “两癌” 检查项目被纳入基本公共卫生服务,宫颈癌筛查工作的连续性得到提升。在城市地区,各地组织开展了大量宫颈癌筛查与体检服务,对宫颈癌的防控投入力度超过农村。
最新数据显示,2015年我国20~64岁女性既往接受过宫颈癌筛查的比例仅为25.7%(其中35~64岁筛查比例为31.4%),其中城市地区为30.0%,农村地区为22.6%,我国离普及规律宫颈癌筛查的目标仍有较大差距 [15]。
2016年以来,乔友林团队在内蒙古鄂尔多斯参与以人群为基础的所有35-64岁女性的宫颈癌筛查工作时,“发现很多接受筛查的女性都已经不是癌前病变而是宫颈癌了,令人痛心。”
为了加速完成目标,上述提及的国家癌症中心赵方辉教授团队为中国量身定制了一条通向消除宫颈癌目标的最优路径,结合了HPV疫苗接种、宫颈癌筛查乃至规范治疗等多种策略交织而成的复合路径。
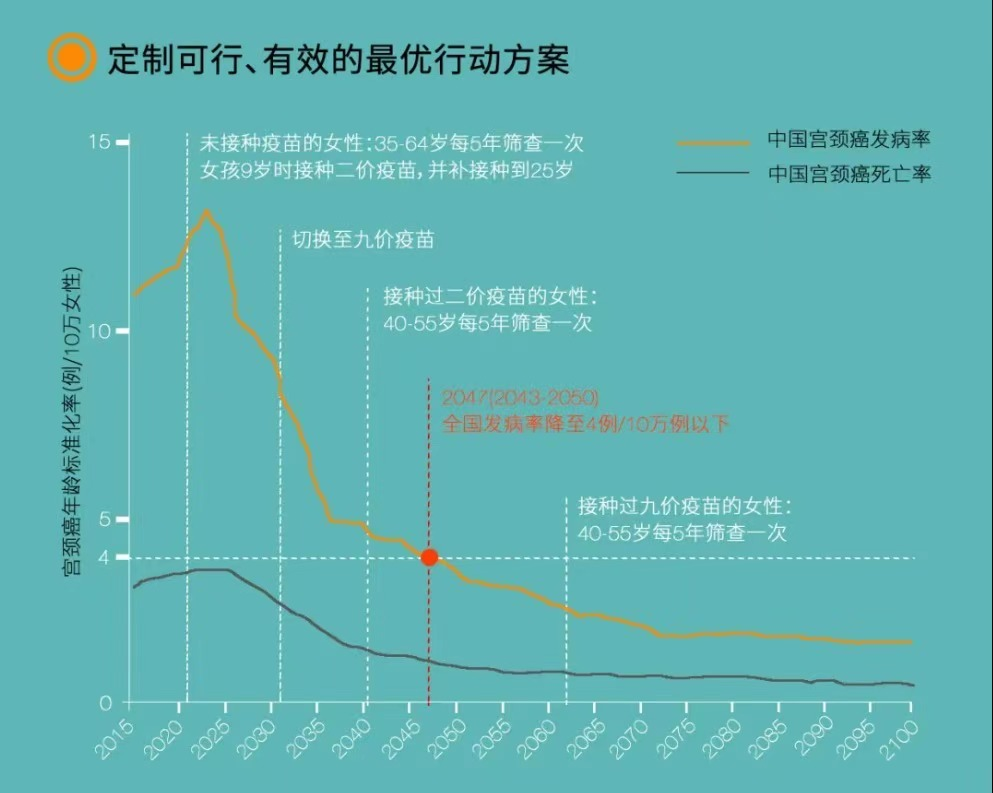
图4 图源:盖茨基金会
如果我国从2020年开始采取上述优化的策略,在不增加防控预算的情况下有可能在21世纪70年代实现消除目标;如果提高宫颈癌的防控预算,我国将可能大幅提前消除宫颈癌的时间,在2050年前后实现消除目标。
参考文献:
[1] 广东省卫生健康委员会. 《广东省适龄女生人乳头瘤病毒(HPV)疫苗免费接种工作方案(2022—2024年)》政策解读. 2021
[2] XiaC, HuS, XuX, et al. Projections up to 2100 and a budget optimisation strategy towards cervical cancer elimination in China: a modelling study[J]. Lancet Public Health, 2019,4(9):e462-e472. DOI: 10.1016/S2468-2667(19)30162-8.
[3] Hu Yue-Mei,Guo Meng,Li Chang-Gui,Chu Kai,He Wen-Gang,Zhang Jing,Gu Jian-Xiang,Li Juan,Zhao Hui,Wu Xiang-Hong,Lin BiZhen,Lin Zhi-Jie,Yao Xing-Mei,Li Ya-Fei,Wei FeiXue,Huang Yue,Su Ying-Ying,Zhu Feng-Cai,Huang Shou-Jie,Pan Hui-Rong,Wu Ting,Zhang Jun,Xia Ning-Shao. Immunogenicity noninferiority study of 2 doses and 3 doses of an Escherichia coli-produced HPV bivalent vaccine in girls vs. 3 doses in young women.[J]. Science China. Life sciences,2020,63(4):
[4] WHO. Human papillomavirus (HPV) and cervical cancer. World Health Organization. (hpv)-and-cervical-cancer. Published 2020. Accessed 12.1, 2021.
[5] Palmer Tim,Wallace Lynn,Pollock Kevin G,Cuschieri Kate,Robertson Chris,Kavanagh Kim,Cruickshank Margaret. Prevalence of cervical disease at age 20 after immunisation with bivalent HPV vaccine at age 12-13 in Scotland: retrospective population study.[J]. BMJ (Clinical research ed.),2019,365:
[6] Brotherton Julia M L. The remarkable impact of bivalent HPV vaccine in Scotland.[J]. BMJ (Clinical research ed.),2019,365:
[7] Falcaro Milena,Castañon Alejandra,Ndlela Busani,Checchi Marta,Soldan Kate,LopezBernal Jamie,EllissBrookes Lucy,Sasieni Peter. The effects of the national HPV vaccination programme in England, UK, on cervical cancer and grade 3 cervical intraepithelial neoplasia incidence: a register-based observational study.[J]. Lancet (London, England),2021:
[8] Kjaer Susanne K,Nygård Mari,Dillner Joakim,Brooke Marshall J,Radley David,Li Meng,Munk Christian,Hansen Bo T,Sigurdardottir Lara G,Hortlund Maria,Tryggvadottir Laufey,Joshi Amita,Das Rituparna,Saah Alfred J. A 12-Year Follow-up on the Long-Term Effectiveness of the Quadrivalent Human Papillomavirus Vaccine in 4 Nordic Countries.[J]. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America,2018,66(3):
[9] Aydin M, Bozkurt A, Cikman A, et al. Lack of evidence of HPV etiology of prostate cancer following radical surgery and higher frequency of the Arg/Pro genotype in turkish men with prostate cancer[J]. International braz j urol, 2017, 43(1): 36-46.
[10] Centers for Disease Control and Prevention. Published 2020. Accessed 12.1, 2021.
[11] Public Health England. Published 2019. Accessed 12.1, 2021.
[12] 新华网. Published 2020. Accessed 12.1, 2021.
[13] Agnes Binagwaho, Fidele Ngabo, Claire M Wagner, et al. Integration of comprehensive women’s health programmes into health systems: cervical cancer prevention, care and control in Rwanda. 2013;91:697-703.
[14] Binagwaho, A., Wagner, C. M., Gatera, M., Karema, C., Nutt, C. T., & Ngabo, F. (2012). Achieving high coverage in Rwanda's national human papillomavirus vaccination programme. Bulletin of the World Health Organization, 90(8), 623–628.
[15]ZhangM, ZhongY, ZhaoZ, et al. Cervical cancer screening rates among Chinese women --China, 2015[J]. China CDC Weekly, 2020, 2(29): 481-486. DOI: 10.46234/ccdcw2020.128.
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 