阅读:0
听报道

新的发现“为新冠病毒自然起源提供了强有力的证据,说明自然界蝙蝠等野生动物可能携带更多的类似病毒。” | 图源:
导 读
巴斯德研究所和老挝国立大学合作的一项研究认为,可以感染人类的冠状病毒很可能在东南亚蝙蝠中广泛传播,证据是在老挝新发现的、与新冠病毒高度相似的三种蝙蝠冠状病毒。
撰文|贾克山
责编|冯灏 陈晓雪
自2019年疫情暴发以来,新冠病毒的起源始终受到科学界和大众的广泛关注 [1]。追溯新冠病毒起源的主流研究方法,是寻找野生动物携带的、与新冠病毒序列相似的冠状病毒。目前的报道中,与新冠病毒全基因组序列最为相似的冠状病毒,是从中菊头蝠(Rhinolophus affinis)中检测到的RaTG13 [2, 3],它与新冠病毒的进化分歧发生在50多年前 [4]。
科学家们普遍认为,决定冠状病毒宿主范围的关键是刺突蛋白,特别是其受体结合域。
根据现有的研究,蝙蝠冠状病毒RaTG13的刺突蛋白结合人类受体的效率较低,病毒感染人类细胞的能力非常有限 [5]。而穿山甲冠状病毒的受体结合域序列与新冠病毒更为接近 [6, 7],具备感染人类细胞的能力 [8]。
因此,科学家们一度判断,新冠病毒可能通过蝙蝠冠状病毒与穿山甲冠状病毒在受体结合域发生重组产生,穿山甲或许是新冠病毒从蝙蝠传染到人的中间宿主。
法国巴斯德研究所、老挝巴斯德研究所和老挝国立大学的科研人员认为,如果新冠病毒由蝙蝠直接 “溢出” 传染到人,应当可以在野生蝙蝠中检测到与新冠病毒受体结合域序列相近的冠状病毒。
为了检验这个假说,他们在老挝北部岩溶(喀斯特)地貌的洞穴中搜集了1551份蝙蝠血液、唾液、肛拭子/粪便和尿液样本,并进行了冠状病毒基因组序列分析 [9]。2021年9月17日,他们将研究结果上传到《自然》杂志社的预印本平台(尚未经过同行评议)。
在搜集到的样本中,研究人员发现了三种蝙蝠冠状病毒(BANAL-52,BANAL-103和BANAL-236)与新冠病毒序列高度相似。其中,BANAL-52在所有已报道的冠状病毒中,与新冠病毒的亲缘关系仅次于RaTG13(图A)。
“这篇文章中发现的病毒是迄今为止发现的新冠病毒最接近的祖先,为新冠病毒自然起源提供了强有力的证据,说明自然界蝙蝠等野生动物可能携带更多的类似病毒。” 在接受《知识分子》采访时,中国科学院武汉病毒研究所研究员石正丽说。
特别值得注意的是,在刺突蛋白的受体结合域与人类受体接触的17个氨基酸中,BANAL-52和BANAL-103有16个氨基酸与新冠病毒相同(图B)。与之形成鲜明对比,RaTG13与新冠病毒仅有11个氨基酸相同。
研究发现,与之前被广泛报道的蝙蝠冠状病毒RaTG13不同,此次新发现的蝙蝠冠状病毒的刺突蛋白可以与人类细胞受体结合,可以介导病毒感染人类细胞,并且可以被人类血清中的新冠病毒抗体中和。
香港大学李嘉诚医学院生物医学学院教授金冬雁则认为,该发现“基本上都是已知或意料之中”,在全基因组层面,新发现的三种蝙蝠病毒并没有显示出比RaTG13更接近新冠病毒。
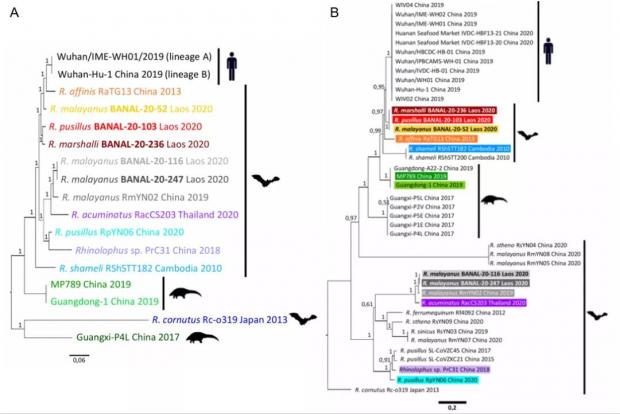
新冠病毒及其相关病毒的进化树。(A)基于全基因组(B)基于包含刺突蛋白受体结合域的序列 | 图源:文献[9]
该研究发现,同一洞穴内不同蝙蝠物种携带的冠状病毒序列高度相似,表明冠状病毒能够在同一洞穴的多个蝙蝠物种间互相传播,为不同来源的蝙蝠冠状病毒发生重组提供了条件。因此,新冠病毒可能是通过来源于多个蝙蝠物种的冠状病毒重组产生的。
对此,汕头大学·香港大学联合病毒学研究所/粤港新发传染病联合实验室副所长朱华晨解释说,蝙蝠就像一个大水库一样,贮存了大量具有高度遗传多样性的冠状病毒,目前已经知道大多数哺乳动物的冠状病毒都可以在蝙蝠中找到与之具有遗传关联的冠状病毒,这些病毒之间有时会发生各种重组,进而产生一些新的变种。
相较于穿山甲冠状病毒,该研究新发现的蝙蝠冠状病毒的受体结合域序列与新冠病毒更为相似。与支持穿山甲作为中间宿主、参与新冠病毒起源的研究不同,该研究支持冠状病毒可以从蝙蝠宿主直接 “溢出” 传染人类。这一结论也与近期基于突变特征的新冠病毒溯源结果一致 [10,11]。
如果冠状病毒从蝙蝠直接 “溢出”,那么,它又是如何传染到人的呢?研究者认为,在洞穴内或附近修行的僧侣、进入洞穴观光的游客,或者在洞穴中工作的相关从业者,都有可能直接暴露于蝙蝠冠状病毒。
此外,该研究还拓展了冠状病毒在不同国家和地区自然分布的认识。朱华晨说,此前,在中国云南、浙江,还有日本、柬埔寨、泰国等地的菊头蝠中,都曾发现过冠状病毒。此研究告诉我们,在老挝北部的蝙蝠群中,同样存在这一类型的病毒。“也许,在中南半岛的石灰岩溶洞系统中、在跨越湄公河两岸的几个国家里,甚至在其他还没有被留意到的国家和地区,可能都有这类病毒在野外活动的痕迹。”
新冠病毒的刺突蛋白存在弗林蛋白酶切割位点,可以提高病毒进入宿主细胞的效率。该研究在新采集到的蝙蝠病毒样本中未发现弗林蛋白酶切割位点,研究者解读为目前采集的蝙蝠冠状病毒样本量仍然不足。
金冬雁也指出,该研究还有待完善,很多具体数据都没给出来,比如,新发现的病毒与RaTG13的同源性比较、受体结合域的同源性比较等等。
在接受采访时,悉尼大学进化生物学家和病毒学家 Eddie Holmes 教授指出,“研究为新冠病毒的自然起源增加了令人信服的证据支持,强调了具备感染人类能力的冠状病毒在自然界中广泛存在”[12]。金冬雁则认为,“就病毒溯源而言,在动物中找到与新冠接近相同的病毒并排除来自人类,才算是真正找到新冠病毒的源头”。
未来,科研人员需要对蝙蝠洞穴周边人群开展调研,评估是否感染过蝙蝠冠状病毒,是否产生了冠状病毒相关抗体。朱华晨提醒说,冠状病毒具有天然的跨物种传播能力,它们所引起的感染事件,不是偶然的一次性事件;至少在菊头蝠属中,它的感染和流行,是可以反复出现的“自然事件”。“这提醒我们注意,自然界中还会不会有更多其他的物种,也能像菊头蝠和穿山甲一样,自然带毒,且还没有被发现?”
“这些结果将为后续的新冠病毒溯源提供方向,凸显了针对野生动物携带病毒的前瞻性研究以及跨种感染风险预警的重要性。” 石正丽说。
参考资料
, B., et al., Characteristics of SARS-CoV-2 and COVID-19. Nature Reviews Microbiology, 2021. 19(3): p. 141-154.
2.Kar, S. and J. Leszczynski, From Animal to Human: Interspecies Analysis Provides a Novel Way of Ascertaining and Fighting COVID-19. The Innovation, 2020. 1(2): p. 100021.
3.Lytras, S., et al., The animal origin of SARS-CoV-2. Science, 2021. 373(6558): p. 968-970.
4.Boni, M.F., et al., Evolutionary origins of the SARS-CoV-2 sarbecovirus lineage responsible for the COVID-19 pandemic. Nat Microbiol, 2020. 5(11): p. 1408-1417.
5.Liu, K.F., et al., Binding and molecular basis of the bat coronavirus RaTG13 virus to ACE2 in humans and other species. Cell, 2021. 184(13): p. 3438-3451.
6.Lam, T.T.Y., et al., Identifying SARS-CoV-2-related coronaviruses in Malayan pangolins. Nature, 2020. 583(7815): p. 282-285
7.Xiao, K.P., et al., Isolation of SARS-CoV-2-related coronavirus from Malayan pangolins. Nature, 2020. 583(7815): p. 286-289.
8.Wrobel, A.G., et al., Structure and binding properties of Pangolin-CoV spike glycoprotein inform the evolution of SARS-CoV-2. Nature Communications, 2021. 12(1): p. 837.
9.Temmam S., et al., Coronaviruses with a SARS-CoV-2-like receptor-binding domain allowing ACE2-mediated entry into human cells isolated from bats of Indochinese peninsula. Research Square, 2021: DOI: 10.21203/rs.3.rs-871965/v1.
10.Shan, K.J., et al., Host-specific asymmetric accumulation of mutation types reveals that the origin of SARS-CoV-2 is consistent with a natural process. The Innovation, 2021. 2(4): p. 100159.
11.Deng, S., K. Xing, and X. He, Mutation signatures inform the natural host of SARS-CoV-2. bioRxiv, 2021: DOI: 2021.07.05.451089.
12.
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 