导 读
一种叫做内源性大麻素的化学物质,对人的发育、睡眠周期、能量代谢、学习和记忆等诸多生理过程非常重要,但要在活体中检测它一直很困难。
最近,专注于神经递质探针研究的李毓龙团队,开发出专门针对内源性大麻素的灵敏荧光探针,使得实时追踪这一物质变得容易起来。
撰文 | 李可
责编 | 计永胜
人类大脑由八百亿个神经元组成,后者又通过数万亿个突触组成复杂的神经网络。在这个复杂网络中,神经元突触末梢会释放神经递质(Neurotransmitter),如乙酰胆碱、多巴胺等,作用于神经元或效应细胞膜上的受体,发挥信息传递的功能。同时,神经元还会产生另一类化学物质,它们不直接传递信息,而是通过间接调制神经递质的量及活动水平,以增强或削弱信息传递效应,这些化学物质被称为神经调质(Neuromodulator)。
内源性大麻素就是其中重要一员,其广泛分布于周围神经和中枢神经系统。与储存在突触囊泡并由突触前末端释放的经典神经递质不同,内源性大麻素通常从突触后膜产生并释放,然后逆行到突触前末端并激活大麻素受体,它的激活通常会抑制一些神经递质的释放。
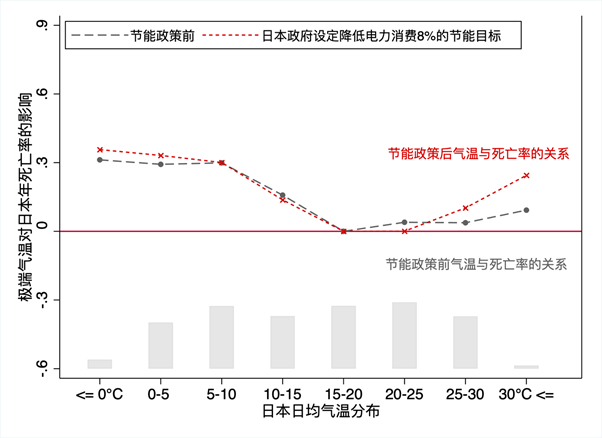
图1 大麻素受体在人体组织器官的分布 | 图源:参考文献[1]
内源性大麻素(Endocannabinoids,eCBs)主要有两种脂质代谢物2-花生四烯酰甘油(2-AG)和花生四烯乙醇胺(AEA),其生物学功能主要由1型和2型大麻素受体(CB1R和CB2R)的激活来介导。它在发育、情绪状态、疼痛、睡眠周期、能量代谢、学习和记忆等诸多生理过程中都发挥着重要的作用。多项研究表明,内源性大麻素系统的失调与多种疾病有关,包括神经精神疾病、神经退行性疾病、癫痫和癌症等。鉴于内源性大麻素在体内分布的广泛性和生理功能的多样性,对其深入探究已成为治疗神经系统疾病一个潜力巨大的研究方向。
要更好地研究内源性大麻素在生理、病理过程中扮演的角色,研究人员需要实时监测其在活体内特定脑区的特异信号变化,看清它的 “一举一动”。然而,受限于传统检测方法的低分子特异性、低时空分辨率及其可能带来的组织损伤,研究人员一直以来都缺乏对内源性大麻素动态变化的精确记录手段。应用新开发的灵敏、特异的内源性大麻素探针以光学成像方式探究内源性大麻素释放及其调控将打破这个困扰研究人员多年的瓶颈。
2021年11月12日,《自然·生物技术》(Nature Biotechnology)杂志在线发表了北京大学生命科学学院李毓龙团队关于内源性大麻素特异性荧光探针的开发与应用的研究论文。这是该团队在连续开发出重要神经递质乙酰胆碱探针、多巴胺探针、去甲肾上腺素探针、腺苷探针和五羟色胺探针之后 [3-7],运用对G蛋白偶联受体的改造在神经递质/调质检测中的再次成功应用。

图2 论文截图
该类研究利用可与神经递质/调质相结合的G蛋白偶联受体作为探针的骨架,把对结构变化敏感的荧光蛋白(cpEGFP)嵌入受体。受体与神经递质/调质结合引发构象变化便会被转换为荧光信号。研究者结合现代成像技术,就能看到神经递质/调质浓度实时变化情况。在此基础上,研究者针对不同的神经递质/调质还对探针进行了全方位的优化,使具有极高的分子特异性和时空分辨率。该团队将这种高效的内源性大麻素探针命名为eCB2.0。

图3 探针设计原理 | 图源:参考文献[2]
该论文开发的内源性大麻素特异性探针eCB2.0具有极高的灵敏度、特异性、信噪比、动力学和光稳定性,可以高时空分辨率地精确检测动物活体内内源性大麻素的动态变化。与以往探针一样,该探针也具有可基因编码的特性。研究者可以通过转染、病毒注射以及构建转基因动物等手段,将eCB2.0表达在HEK293T人胚胎肾细胞、神经元细胞、小鼠脑片,以及活体小鼠中。

图4 eCB2.0可表达在体外培养的细胞膜上 | 图源:参考文献[2]
同时,该探针能够分别特异性检测到清醒小鼠脑杏仁核基底外侧和海马体中由足电击刺激和奔跑触发的内源性大麻素的动态变化。
 图5 eCB2.0可检测自由运动的小鼠大脑杏仁核部位的内源性大麻素的动态变化 | 图源:参考文献[2]
图5 eCB2.0可检测自由运动的小鼠大脑杏仁核部位的内源性大麻素的动态变化 | 图源:参考文献[2]
此外,在小鼠癫痫模型中,研究人员通过该探针检测到了小鼠海马体神经元兴奋导致的内源性大麻素释放。这些结论进一步证实了其在体内应用时强大的灵敏度、特异性、信噪比、动力学和光稳定性,并且清楚地展示了内源性大麻素探针如何帮助阐明生理和病理过程中的快速内源性大麻素动态。

图6 新型探针检测小鼠发生癫痫时海马CA1区内源性大麻素的动态变化 | 图源:参考文献[2]
关于新型内源性大麻素探针的未来发展和应用,论文提到,鉴于神经系统的复杂性,该探针应用的未来研究方向可能包括内源性大麻素释放的细胞类型的识别、内源性大麻素释放的机制和时间特性、内源性大麻素扩散的特征、内源性大麻素信号的持续时间、内源性大麻素对亚细胞元素的影响等。
对这些基本问题的回答,将极大地丰富我们对内源性大麻素信号在突触和神经回路水平的机制和功能的理解。因此,新型探针开启了内源性大麻素研究的新时代,将提供研究者前所未有的、与生理相关的时空尺度来深入理解这一系统。
已逝诺奖得主、生物学家 Sydney Brenner 有一句著名的话:科学的进步取决于新技术、新发现和新想法。李毓龙常常在报告中引用这句话,他坚信技术的价值。
目前,斯坦福大学Ivan Soltesz实验室已经借助这一探针解析了活体动物海马体内源大麻素信号的分子特性和时空动态,发现与正常的生理活动相比,癫痫会引起大量2-AG的释放,而2-AG为长时程的中风样症状提供了基础底物。[8]
不久前,李毓龙在接受Neuron 杂志专访时表示,他的实验室接下来将开发能够检测更多化学信号的探针,也将致力于将这些新工具应用到神经系统的研究中,包括在生理及疾病环境下神经递质释放、回收的调控机制,以及他们所扮演的具体功能的研究 [9]。
神经生物学家、斯坦福大学生物系教授骆利群评论说,李毓龙在开发使用G蛋白偶联受体传感器检测神经递质的探针方面已处于世界领先地位,“他开发的传感器已得到广泛的应用。我相信这些新的传感器将使得新的生物发现成为可能。”
参考文献:
[1] Zou, S., & Kumar, U. (2018). Cannabinoid receptors and the endocannabinoid system: signaling and function in the central nervous system. International journal of molecular sciences, 19(3), 833.
[2] Dong, A., He, K., Dudok, B., Farrell, J., Guan, W., & Li. Y. (2021) . A fluorescent sensor for spatiotemporally resolved imaging of endocannabinoid dynamics in vivo. Nature Biotechnology.
[3] Feng, J., Zhang, C., Lischinsky,J., Jing, M., Zhou, J., Wang, H., ... & Li, Y. (2019). A genetically encoded fluorescent sensor for rapid and specific in vivo detection of norepinephrine. Neuron.
[4] Jing, M., Zhang, P., Wang, G., Feng, J., Mesik, L., Zeng, J., ... Zhu, JJ& Li, Y. (2018). A genetically-encoded fluorescent acetylcholine indicator for in vitro and in vivo studies. Nature Biotechnology.
[5] Sun, F., Zeng, J., Jing, M., Zhou, J., Feng, J., Owen, S., ... & Li, Y.(2018). A genetically-encoded fluorescent sensor enables rapid and specific detection of dopamine in flies, fish, and mice. Cell.
[6] Peng, W., Wu, Z., Song, K., Zhang, S., Li, Y., & Xu, M. (2020). Regulation of sleep homeostasis mediator adenosine by basal forebrain glutamatergic neurons. Science, 369(6508).
[7] Wan, J., Peng, W., Li, X., Qian, T., Song, K., Zeng, J., ... & Li, Y. (2021). A genetically encoded sensor for measuring serotonin dynamics. Nature Neuroscience, 24(5), 746-752.
[8] Farrell, J. S., Colangeli, R., Dong, A., George, A. G., Addo-Osafo, K., Kingsley, P. J., ... & Soltesz, I. (2021). In vivo endocannabinoid dynamics at the timescale of physiological and pathological neural activity. Neuron, 109(15), 2398-2403.
[9]
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 