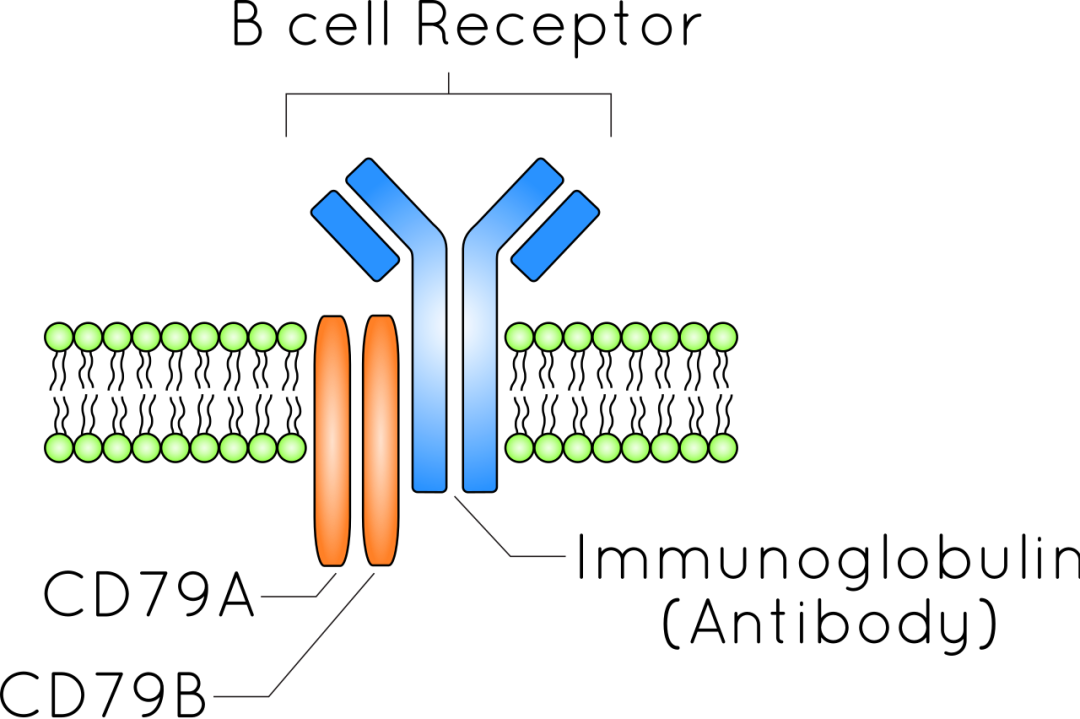
 B细胞受体 | 图源:wikipedia
B细胞受体 | 图源:wikipedia
导 读
完整B细胞抗原受体复合物的高分辨率的结构,一直是领域中的研究难点和热点,半个世纪以来都没有突破,是B细胞免疫学研究领域 “圣杯” 级别的问题之一。现在,随着这个问题的解决,基于免疫学原理来设计疫苗、药物的愿景将会得到新的启发与工具。
撰文 | 宋安娜
8月18日,哈尔滨工业大学生命科学与技术学院黄志伟课题组在《科学》(Science)上发表题为《两种亚型的人类B细胞受体的冷冻电镜结构》(Cryo-EM structures of two human B cell receptor isotypes)的研究文章,报道了B细胞受体复合物亚基的组装、识别机制。
 图1 黄志伟课题组的文章 | 图源:
图1 黄志伟课题组的文章 | 图源:
同一天,《科学》还在线发表了另一篇解析B细胞受体复合体结构的文章,来自西湖大学生命科学学院教授施一公及其博士后宿强等人的论文《人IgM B细胞受体的冷冻电镜结构》(Cryo-EM structure of the human IgM B cell receptor)。
图2 施一公等人的文章 | 图源:
当人体免疫细胞B细胞遇到外来病原体抗原刺激时,B可分化成浆细胞和记忆B细胞,进一步合成和分泌抗体,对付入侵者。这个过程当中,一个关键的步骤是,识别入侵者是敌是友,而这个过程依赖于B细胞受体。因此,B细胞受体的免疫识别、免疫活化的结构基础与分子机制问题一直是免疫学领域的重要基础科学问题。
1972年,杰拉尔德·埃德尔曼(Gerald M. Edelman)和罗德尼·罗伯特·波特(Rodney R. Porter)凭借对可溶性抗体(血液中的抗体)的分子结构的解析而获得诺奖。清华大学生命学院长聘教授、清华大学免疫学研究所研究员刘万里告诉《知识分子》,完整B细胞抗原受体复合物的高分辨率的结构,一直是领域中的研究难点和热点,半个世纪以来都没有突破,是B细胞免疫学研究领域的 “圣杯” 级别的问题之一。
刘万里说,早在1990年代,人们就知道B细胞抗原受体的组分是一个由4个基因编码、6个多肽链组成的复合物,现在,两篇 “背靠背” 论文所报道的工作则是让人们在亚纳米的精度上看清楚这些组分是如何组装在一起的。这就像一张不同组分在一起的家庭照,过去人们看到了成员依稀的轮廓,现在可以看清楚每个人脸上的毛孔。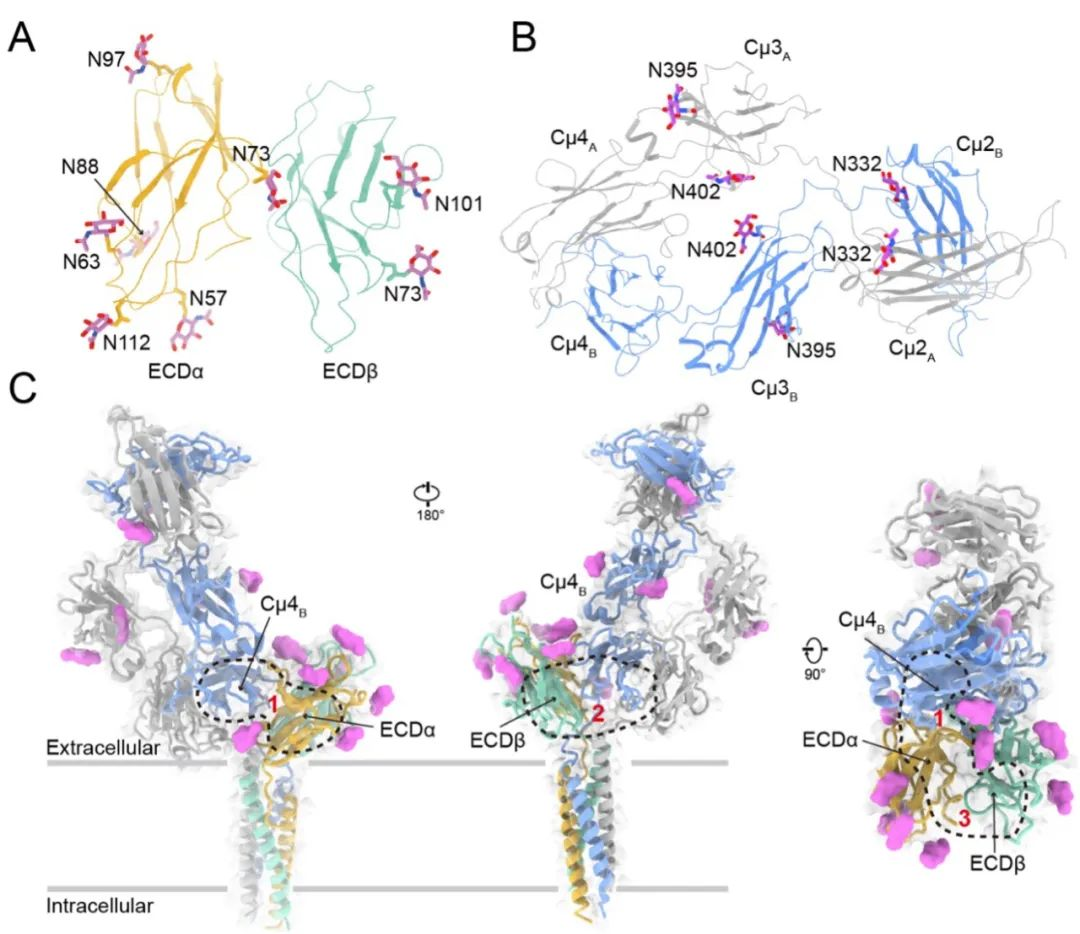
图3 B细胞的 “生命周期” 概略示意图
如何看清楚B细胞受体的每个 “毛孔”?
骨髓中的造血干细胞,一部分在胸腺中发育成T淋巴细胞,一部分在骨髓中发育成B淋巴细胞。T细胞在体液免疫和细胞免疫均发挥作用,且可分泌淋巴因子;B细胞只在体液免疫发挥作用。人体大多数免疫反应都是由细胞免疫和体液免疫共同完成的。
与巨噬细胞,NK细胞等天然免疫细胞不同,B细胞和T细胞参与的适应性免疫具有特异性,能够根据抗原的不同产生针对性的抗体。在这个过程中,T细胞受体(TCR)和B细胞受体(BCR)是关键一环,它们能够识别抗原信号、把信号跨膜传递至胞内。
对于B细胞来说,成熟的每一个B细胞都带一种能识别不同物质结构的蛋白分子,就是B细胞受体(BCR,B cell receptor)。当有病原入侵我们,B细胞在其受体完成病原识别后,就会制造出特异性的抗体并复制自己。抗体飞出去结合在病原上,可以直接杀死或者帮助其他免疫细胞杀死这些病原。当病原被清除,失去了目标的B细胞大多数会自然灭亡,留下少部分分泌抗体在体内巡逻一段时间。
“T细胞受体或者B细胞受体如何把抗原的信号传递到细胞内、完成接下来的免疫反应,这实际上是领域内特别重要的的问题,也是免疫学一个非常基础的问题。” 黄志伟在接受《知识分子》采访时表示。
人类B细胞受体有五种同种型,黄志伟团队解析了人IgG和IgM两种同种型的BCR复合物结构;施一公研究组则报道了人源IgM同种型B细胞受体的电镜结构。为获取BCR高分辨率结构信息,两个课题组成功搭建BCR重组表达和纯化系统,并利用冷冻电镜单颗粒技术对几百万个单一BCR颗粒进行成像解析,最终成功重构出原子级分辨率的视图。
结果发现,两个团队所解析的IgM亚型结构是彼此一致的,这些结构也证实了之前只依靠生化结果推测的结构细节。B 细胞受体的膜抗体具有熟悉的Y形,两个片段抗原结合(Fab)臂通过链接到一个片段可结晶(Fc)腿,继而连接到一个跨膜结构域。
这次研究揭示,BCR膜抗体保持其Y形,其中Fab臂保持自由,而Fc部分以1:1的化学计量学与Iga-Igb异质二聚体结合。同时,二者之间的装配主要依赖跨膜螺旋间多个极性残基的相互作用,而这些膜内的相互作用在不同物种和不同抗体类别中是高度保守的,这也进一步印证了先前该区域对BCR的组装和功能至关重要这一结论。
黄志伟团队还解析了IgG1 B细胞受体的结构,从而对IgM-BCR和IgG-BCR的结构进行比较,揭示了亚型之间的结构差异以及保守之处。
相比较IgM-BCR,IgG-BCR的mIg分子与Igα-Igβ二聚体结合较为松散,更容易出现独立存在于质膜的mIg分子;另一方面也可能为后期IgM-BCR和IgG-BCR信号转导机制上的差异提供了结构学的基础。
西湖大学研究人员、论文第一作者及共同通讯作者宿强在接受《知识分子》访谈时介绍说,他们团队则得出了未结合抗原的静息状态下人IgM-BCR的3.3埃冷冻电子显微镜结构,分辨率更高。此外,他们还揭示了IgM胞外区域三个潜在的表面结合位点,这可能有助于用于疾病干预的治疗性抗体或微型蛋白质的理性设计。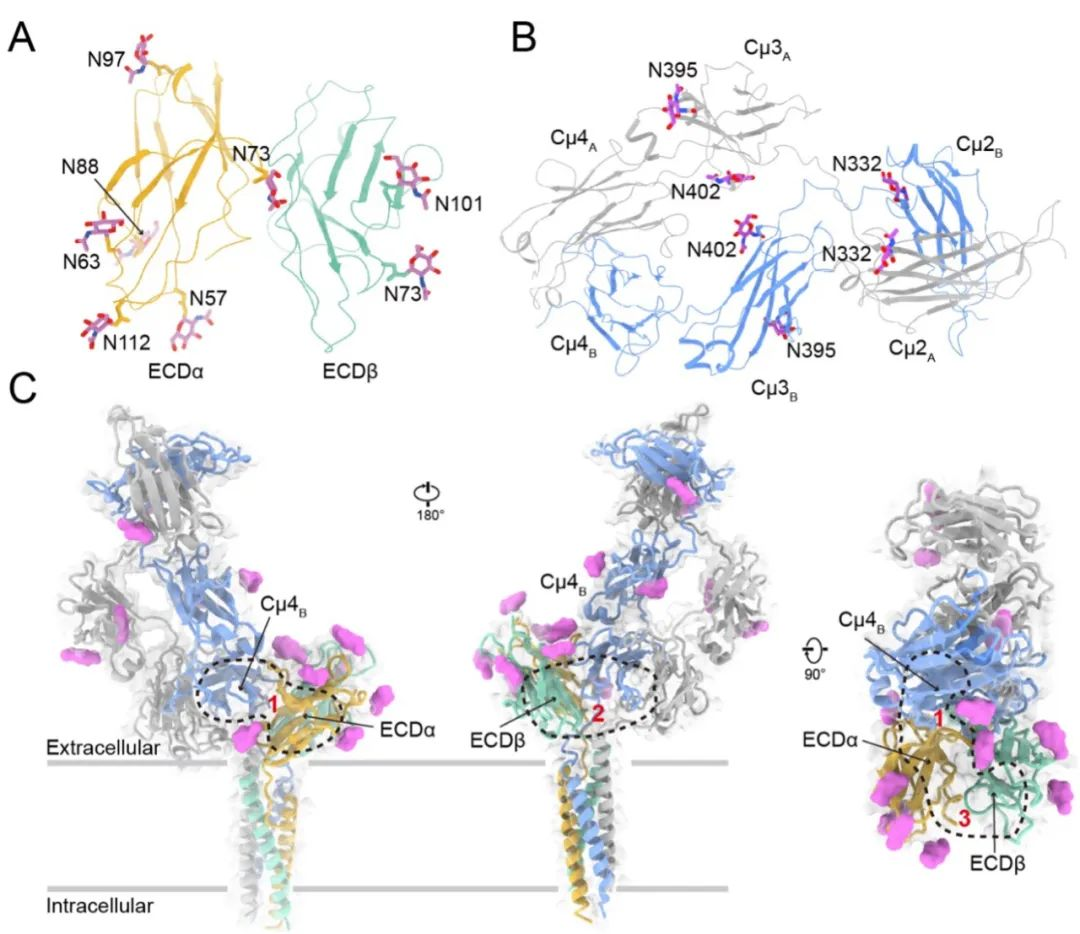
图4 IgM-BCR复合物的整体结构图
支撑抗体类药物和疫苗研发
宿强等人今年2月向Science投稿,半年后发表,整个过程比较顺利,审稿人多对文章的意义持积极、支持的态度。宿强说,有审稿人表示,解析B细胞受体复合体,对于理解B细胞的活化过程非常重要;也有审稿人的审稿意见是,“这项研究是B细胞生物学的一个巨大突破,值得发表在Science。”
B细胞受体的组分由德国马普所的 Michael Reth 实验室于1990年鉴定发表。在之后的三十多年中,人们对BCR胞外区如何识别各种抗原并激活B细胞信号通路进行了深入的研究,但作为BCR复合物如何进行组装的分子机制仍然未知。
既然是免疫学中的基础问题,那么,在过去很多年里,来自全球各地开展免疫学基础研究的科学家们必然也在致力于完成这项任务,为何直到现在才成功?
此前,这的确是一个大家都想解决却未能成功的重要问题。黄志伟解释说,B细胞、T细胞与其它受体不太一样,它们是单次跨膜的多亚基的受体,所以比一般的受体更复杂而且更不稳定,像GPCR这样的受体是7次跨膜,所以相对而言比较稳定。
而B细胞和T细胞的受体,连蛋白都很难表达出来,更不要说解析它的结构了。他介绍,实际上,对于T细胞受体,在大约30年前,如何解析它的结构就是领域内很火的一个研究热点,当时很多实验室在做,但是一直没有成功,很多人就放弃了。
一位不愿具名具名的教授指出,如果没有冷冻电镜的飞速发展,使得单分子的成像分析技术如此先进,肯定是做不了这件事的。但他也表示,黄志伟等团队之所以能够来做出这些成果,除了技术的加持,也非常依赖于他们实验室在纯化和稳定大分子生物复合物蛋白方面的功力。
实际上,黄志伟团队的研究方向主要是免疫和神经生物学领域的重要生物大分子的结构与功能的关系,及天然免疫系统激活的新基因及其信号通路。而基于在T细胞受体的分子组装、免疫性机制方面的研究,黄志伟曾在2020年获得过科学探索奖。
宿强也表示,能够取得这个突破,是团队多年在膜蛋白领域内研究和积累的结果。比如,IgM-BCR本身柔性比较大,他与其他研究人员通过共表达一个pERp1酶,促进二硫键形成,在蛋白质层面将它的结构折叠得更稳定,另外也通过大量的计算尝试,找到一个条件可以解析它最稳定的状态。
B细胞和T细胞的发现,被认为是现代免疫学的起点。最近10年,肿瘤治疗领域最明星的制药成就,便是肿瘤免疫治疗药物。与此同时,2018年诺贝尔生理学或医学奖就颁给了肿瘤免疫治疗方向,这种治疗的原理正是通过释放被癌细胞抑制的T细胞功能,来达到治疗癌症的目的。
除了参与B细胞增殖分化这一重要的免疫过程以外,BCR还是B细胞淋巴瘤的药物靶点。例如,2019年罗氏制药获批的药物Polivy(Polatuzumab vedotin)是一种抗体偶联药物,将单克隆抗体和抑制有丝分裂的细胞毒剂进行偶联。该抗体偶联药物可以结合BCR中的Igβ组分,对B细胞淋巴瘤细胞精准杀伤,被批准用于治疗弥漫大B细胞淋巴瘤。
人们更为熟悉的新冠疫苗,也依赖B细胞的出动。新冠疫苗的原理就是将新冠病毒关键的S蛋白注射到体内,让B细胞、T细胞等去捕获该S蛋白,B细胞就可以分化浆细胞产生抗体,而且会帮助人体 “记住” 病毒的样子,以在下一次病毒真正来临时产生抗体。
而现在,随着这些基础生物学的问题一点点解决,基于免疫学原理来设计疫苗、药物的愿景将会得到新的启发与工具。
刘万里打了一个很通俗的比方,科学家们过去只知道,有一种机器叫BCR,如果把面粉和馅料放进去,就会生产出来美味的饺子,即对付病原体所分泌的抗体,然而,人们不知道这个机器内部是如何运转的,因而也就难以进行改造。而掌握了这个机器运转的机制,就可以更加自主地设计不同口味、精细程度与大小的饺子了。
当面对外来病原体威胁时,机体希望BCR活跃起来,为分泌抗体做好准备,当不需要时,机体希望BCR能安静一些,否则,过分激活可能会带来自身免疫性疾病。这就是医药研发人员希望能够调控的一类免疫状态。
了解B细胞受体的结构,有助于实现这个目的。宿强告诉《知识分子》,他所在的团队已经解析了静息状态下的BCR结构,接下来希望了解B细胞激活时,亦即结合抗原时BCR的结构。基于这些研究,可以设计一些小分子或者纳米抗体,将BCR更好地稳定在激活状态,这样设计出来的疫苗可能就会更加高效;同样,这些小分子或者纳米抗体将BCR稳定在静息状态时,可能作为免疫抑制剂,用于治疗自身免疫性疾病。
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 