阅读:0
听报道

撰文 | 王承志 (《知识分子》特约撰稿人)
责编 | 陈晓雪
● ● ●
自新的基因编辑工具CRISPR/Cas9到来,基因编辑正变得前所未有地容易。科学家已经使用该技术在多个物种中实现基因的敲除或者修改,也就是大家通常所说的转基因动物。通过囊胚注射或者受精卵时期直接注射核酸酶(如Cas9),科学家已经可以制备从啮齿类到灵长类的各种哺乳动物的转基因模型。这些动物模型极大地促进了人类对基因功能的理解,也对在制药等领域的应用有着深远的影响。
但是,当前的基因编辑方法在制备转基因动物时通常出现镶嵌表型,也就是说动物身体一部分细胞的基因是被修改过的,而另一部分则不是。科学家通常的做法是通过杂交的方式在这些动物的后代中筛选出纯合表型(也就是该动物所有的细胞都是同一种基因型)的动物来做研究。这种方法在小鼠等较低等的哺乳动物中是常用的手段,但是在高等哺乳动物比如灵长类动物中则成本过高。以猴子为例,其哺育周期长达5-6年(想想看,等猴子长大的时间都够研究生毕业两次了),而且每胎通常只生1只。因此,在高等哺乳动物中开发高效的基因编辑方法有巨大的实用价值。
最近,中国科学院上海神经科学研究所研究员杨辉和同事合作实现了一种在灵长类动物中一步完全敲除多个基因的方法。6月6日上线的《细胞研究》(Cell Research)发表了这一研究。
“迅速建立基因编辑的猴子模型具有重要意义,特别是一步就可做到完全的基因敲除。”中科院生物物理研究所研究员王晓群评论说。他指出,高效的基因编辑效率,可以降低对受精卵以及代孕母猴的需求,进一步降低了基因编辑的成本。
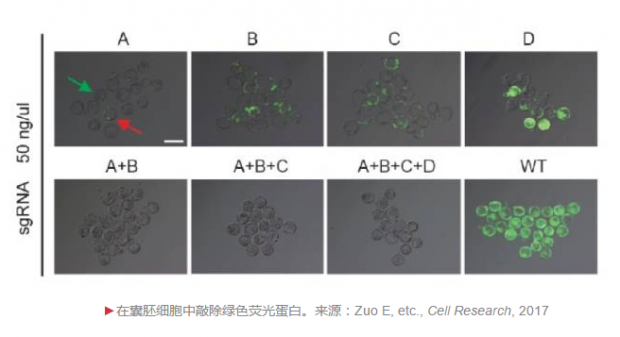
这种方法的核心是在敲除的目标基因的同一个外显子上设计多个sgRNA(被Cas9蛋白用来在基因组上定位的RNA序列)。研究人员首先在囊胚细胞中进行了原理的验证:在已经插入绿色荧光蛋白的细胞中设计了4条sgRNA(A,B,C,D),然后分别单独或联合使用这些sgRNA,结果发现同时使用两条或多条sgRNA时,所有细胞的荧光都消失了。
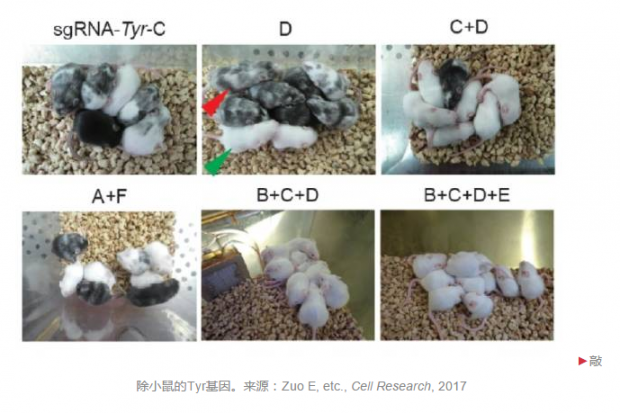
然后,研究人员在小鼠模型上实验了这种方法。他们选取了Tyr基因,因为该基因敲除后小鼠的色素沉着无法发生,基因是否被敲除可以直观地通过小鼠毛色判断。他们发现当只有一条sgRNA时,只有20%左右的后代中出现基因敲除的性状,当同时使用两条sgRNA时,一些组合可以达到70%左右的成功率,而当使用三条或四条sgRNA时,后代中100%出现成功敲除的性状。他们进而选取了Y染色体上的多个基因进行测试,证实了这种方法的有效性。
接着,他们在猴子模型中检验了这种方法。在敲除Prrt2基因的实验中,他们同时转入靶向第3号外显子的三条不同的sgRNA,在获得的11个胚胎中有10个是完全敲除的,而只使用1条sgRNA的实验中,获得的8个胚胎中有5个没有任何敲除,而剩余的3个则是不完全敲除。当把不同处理条件下得到的胚胎植入母猴子宫内发育后,他们分析了子猴的基因型。使用3条sgRNA的实验组共得到两只子猴,其中一只为Prrt2基因完全敲除,另一只为不完全敲除。而只使用1条sgRNA的对照组中,他们得到了4只存活的子猴,其中三只为不完全敲除,而另一只没有发生敲除。通过对Prrt2基因完全敲除的11号子猴全基因组测序,他们也没有发现这种方法有明显的脱靶效应(即在基因组其它位置引起突变)。
该文章的通讯作者杨辉说,这项研究除了可以降低灵长类动物的基因编辑成本,也使得在活体内大规模检测基因功能提供了可能。他介绍,以一次筛选数十个基因为例,如果使用传统方法直接用老鼠来做筛选的话很少有实验室可以承受这样的成本和工作量,但是用这套技术,一个熟练的技术人员一天就能做完所有胚胎注射,两个月就能出结果。“这不仅节约大量成本,而且更加符合动物福利3R原则(3R为Replacement,Reduction,Refinement,即替代、减少和优化),”杨辉说。
“如果能够推广普及,(这个方法)将会很大地推动我国灵长类动物的研究,当然,也会对其他模式动物的基因编辑技术起到推动作用。”王晓群说。他同时强调,这一高效率的方法是否适合其他的重要基因,还需要进一步的结果验证。
参考文献:
Zuo E, Cai YJ, Li K, et al. One-step generationof complete gene knockout mice and monkeys by CRISPR/Cas9-mediated gene editingwith multiple sgRNAs[J]. Cell Research, advance onlinepublication 6 June 2017; doi: 10.1038/cr.2017.81
原文链接:

话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 