阅读:0
听报道
撰文 | 唐华(南昌大学、维克森林大学联合培养博士生)
责编 | 陈晓雪
● ● ●
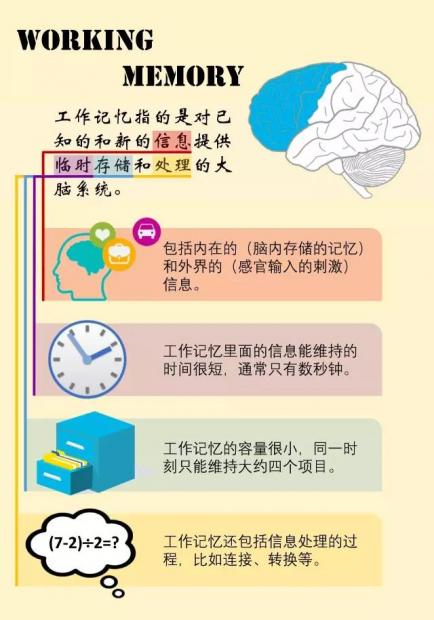
在日常生活中,我们时刻都面临着不同的选择,需要解决许多困难和问题。为了应对各种认知任务,我们需要大脑能在短时间内保存和处理各种信息,完成这个过程的大脑系统就是“工作记忆”(working memory,图1)。它是语言理解、学习与记忆、推理和计划等复杂认知能力的基础[1]。
工作记忆作为一个“思维的黑板” (blackboard of the mind)[2],能为我们提供一个界面,我们可以在这个界面上暂时放置信息,使其“浮现在脑海”。然后我们可以通过一些处理,将这些信息与其他信息联系或转换为新的信息[3]。例如,工作记忆允许我们记住电话号码、完成心算和计划接下来的事情。这些过程通常都在秒级的时间内完成。

什么是“工作记忆容量”?
我们能在某一时刻快速保存、注意或者维持的信息的数目就是工作记忆的“容量”[4]。简单的用电脑做比喻的话,大脑皮层就是我们的“硬盘”,里面存储着海量的信息(记忆);而工作记忆就是我们大脑的“缓存”,工作记忆容量就是“缓存”的容量大小。前额叶皮层(prefrontal cortex, PFC)有如我们的“CPU”。每次执行认知相关任务时,“CPU”会将外界的“输入”(外界的刺激:视觉、听觉等感官刺激)和“硬盘”里面存储的某些信息(脑内的记忆:经验、知识等)放进“缓存”里面进行相关运算。我们知道电脑的硬盘通常很大,但是为了提升运行速度,“缓存”通常比较小。对于工作记忆的容量,也是同样的道理。这种限制很容易就能体会到:我们很难同时进行多项认知任务(比如,边打电话边看书)。
工作记忆容量影响高级认知功能
工作记忆是人类认知功能的基础。个体间工作记忆容量有一定的差异,这与注意力调控、非言语推理以及学业成绩等重要的能力高度相关[5]。并且,患有精神分裂症、中风、脑外伤和注意力缺陷多动障碍(ADHD)等神经精神疾病的人群通常表现出工作记忆容量的下降 [6]。
从儿童期到青春期,我们的工作记忆容量会逐渐增加。这为我们研究工作记忆容量对认知功能的影响提供了良好的机会。某些研究人员认为工作记忆容量的增加是认知功能增长的主要驱动力[7]。一项研究发现,儿童的工作记忆容量可以预测一年之后的推理能力[8]。认知任务的复杂程度可以表示为解决问题时必须同时考虑的项目(item)和项目间关系的数量。而在一系列认知任务测试中,儿童掌握相似复杂程度任务的年龄也基本相同,这提示工作记忆容量可能决定了儿童能掌握的认知任务的复杂程度[9]。这些结果都暗示有限的工作记忆容量可能是高级认知功能的核心限制因素之一。
我们的工作记忆容量有多大?
神奇的数字“4”
最早对工作记忆容量做出测量的是美国心理学家George A. Miller,他在1956年发表了一篇名为《神奇的数字7加减2:人类信息加工容量的某些局限》的论文,认为人类工作记忆的容量大约为7[10]。这篇论文的影响力如此之大,以至于六十多年过去了,普通民众还坚信我们的大脑能够同时维持7条左右信息。事实上,之后大量的研究表明,人类工作记忆的容量其实大致只有4[11],而猕猴的介于3和4之间 [12]。
的确,通常我们大致能记住5~9个随机的数字。但是这并不表示我们的工作记忆容量就有7。实际上,脑内同时处理信息的容量是按“组块”(chunk)来衡量的。每个“组块”可以包含多个数字、字母,也可以是词语或其他形式,不同类型“组块”的分类方式和大小一般不同。这些“组块”间划分的主要依据是:单个“组块”的内部要有较强的联系,而“组块”之间的联系要较弱 [11]。
其实,现在的手机号就不止7个数字,为什么我们都能记住呢?原因正是我们使用了“组块”式记忆。比如,对于手机号16730351028,我们通常会按类似“167-3035-1028”的分组方式进行记忆。这里总共有3个“组块”,“167”因为是运营商的代码而容易记住,“3035” 因为有重复的数字而容易记忆。也就是说,“167” 和 “3035” 分别都有较强的“组块”内联系,而两个者间的联系较弱;所以我们倾向于将“1673035”分成“167”和“3035”这样的两个“组块”,而不是“16730”和“35”。如果我们遇到一串随机的数字87320160531,可能就难记得多了。
当然,大多数人也不会以类似“16-730-351-0-28”这种超过4个“组块”的方式来记忆手机号,一般认为是超过了容量的限制,不利于工作记忆的维持。
两种理论模型
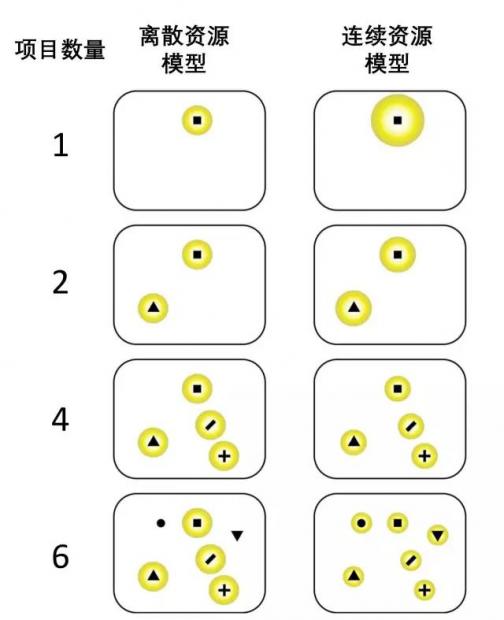
关于如何更好地描述工作记忆容量,学术界一直存在争论。一种观点认为,工作记忆资源以离散的方式分配,数量的上限大约为4个; 另一种观点认为,可以以连续的方式分配,数量上并没有限制(图3)[13]。
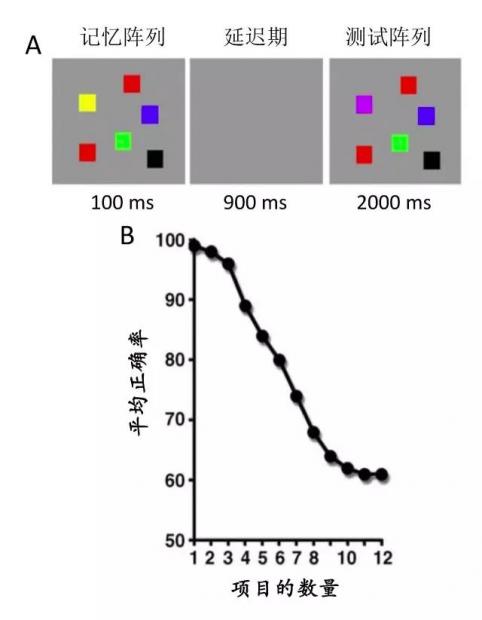
美国认知神经科学家Steve Luck等人通过分析观察者检测视觉刺激是否发生变化的能力来研究工作记忆容量的特性。他们发现,随着需要记忆的项目的数量的增加,人们检测前后两组视觉刺激是否相同的能力越来越低。综合考量,观察者可以在工作记忆中同时维持大约4项信息(图2)。这种基于项目的容量限制符合工作记忆的离散资源模型(discrete resource models)。该模型认为记忆资源是离散分配的,即工作记忆中维持的每个项目必须被分配到单独的“槽”中,且每个项目都占用等量的资源[14]。当需要存储的项目数超过限制时,仅有其中的一部分会被存储,其他的项目将不会被保留任何信息。

相反,连续资源模型(flexible resource models)则认为,在工作记忆中,可以主动维持的项目数没有上限。[16]简单来说,工作记忆资源的总量是固定的,每个项目都占用一部分份额,项目数越多,每个项目所能占用的资源就越少[16]。当不断接收到更多的信息时,记忆资源会被持续地分割,直到表征某个项目的资源被扩展得很微弱时,该项目将不能再被准确地调用(图3)。

哪些因素影响工作记忆容量?
长时记忆
长期记忆是能够保持几天到几年的记忆。它与工作记忆以及短期记忆不同,后二者只保持几秒到几小时。在构建工作记忆的过程中,我们脑内存储的长时记忆起到了非常关键的作用。比如在前面的例子中,记得“167”是常用的手机号前三位很利于工作记忆的维持。同样,如果“1028”正好是你的生日的话,这个号码就更容易记住了。
我们有时会在报道中看到一些记忆力超群的人,他们可以在很短的时间内记住大量的信息,似乎拥有过人的工作记忆容量。事实上,他们中的绝大部分只是经过长期的训练,具备了更强的从长时记忆中提取信息的能力[17]。比如,某些人会将需要记忆的信息通过长时记忆中的场景编成一个有逻辑的故事,当需要复述时,从长时记忆中对这个故事进行调用,并转换成原始信息。这样的记忆技巧并不能真正的提高工作记忆的容量,当面对截然不同的内容时,他们会表现出与普通人差不多的记忆水平。总之,丰富的人生经验和大量的知识储备有利于提高工作记忆的容量,这应该是成年人的工作记忆容量要大于儿童和青少年的重要原因之一。
注意力
注意力被认为是影响工作记忆容量的重要因素。将注意力从关注的项目转移开,会干扰工作记忆的维持[18]。因此,工作记忆可能不只是受其本身固有的存储能力限制,也需要我们将注意力维持在特定的项目上。有趣的是,有研究表明在大量的视觉刺激中,我们最多只能同时追踪4-5个移动的目标,这个数目与工作记忆的容量上限非常接近 [19]。
注意力和工作记忆之间这种紧密的关系,让很多人认为注意力正是导致工作记忆只具备有限容量的关键因素。反之,也有不少人认为,正是因为我们只能同时存储有限数目的信息,才导致我们人类进化成每次只能同时注意极少项的事物。可见,注意力和工作记忆是难以分割的。总之,把注意力集中在某个事物上,会使得它更容易被记住。并且,集中注意力同样意味着忽略外界的干扰信息。Gaspar的研究表明,工作记忆容量小的人不能很好地排除那些影响力大的、让人分心的信息[20]。因此,我们认为维持专注的注意力是形成较高工作记忆容量的重要保障。
生长发育
对儿童及青少年的研究表明,工作记忆容量随着生长发育而逐步增加[21]。脑内神经元之间不断增强的联系被认为与此相关[22]。发育过程中的功能相关研究也表明,较高的工作记忆容量通常伴随着额叶和顶叶皮层内较强的血氧水平依赖的神经元活动[23]。相关计算模型也预测前额叶皮层与其传入皮层之间连接的强度能决定工作记忆的容量,这也可能是人类成长过程中工作记忆容量提升的一个重要因素[24]。 来自青少年和成年猕猴的数据还显示,前额叶皮层神经元之间的总体突触连接强度的增强也与工作记忆的提升相关[25]。
后天训练能否提升工作记忆容量?
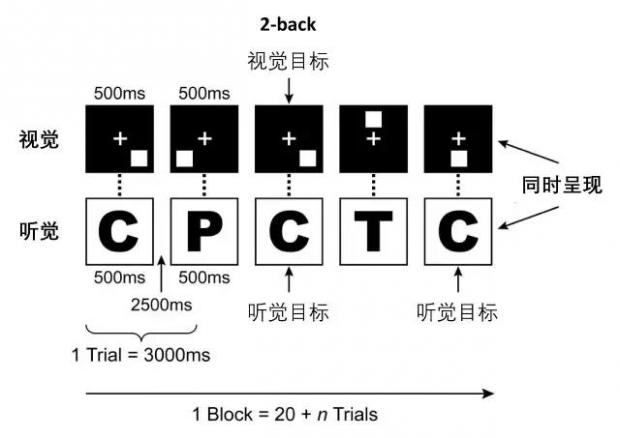
一直以来,人们认为工作记忆容量是不可改变的个体特征。但是最近十几年的研究表明,通过系统的训练(图4),人类,特别是儿童和青少年的工作记忆容量可以得到提升[26, 27]。现今,许多研究开始关注行为训练对工作记忆容量提升的机制。

研究表明,经过相关训练后,大脑不同区域,特别是额顶网络(fronto-parietal network)之间的联系会增强,并且这与个体表现的工作记忆容量的提升成正相关[28]。在猕猴上进行的神经电生理结果进一步揭示,经过训练后,更多的前额叶皮层神经元会以更高的发放频率参与编码视觉刺激[29]。并且,行为训练还能够显著降低前额叶皮层神经元的编码的变异性和噪音的干扰[30]。简而言之,经过相关的行为训练,会有更多的神经元以更强的力度、更精确的方式参与编码相关任务,并且这与工作记忆容量的提升有一定的正相关性[31]。
参考文献
1.Baddeley, A., Working memory. Science, 1992. 255(5044): p. 556-559.
2.Reddy, D., Perception and Production of Fluent Speech. RA Cole (Ed.), 1980: p. 215-242.
3.Goldman-Rakic, P.S., Regional and cellular fractionation of working memory. Proc Natl Acad Sci U S A, 1996. 93(24): p. 13473-80.
4.Cowan, N., T.D. Johnson, and J.S. Saults, Capacity limits in list item recognition: evidence from proactive interference. Memory, 2005. 13(3-4): p. 293-9.
5.Fukuda, K., et al., Quantity, not quality: The relationship between fluid intelligence and working memory capacity. Psychonomic bulletin & review, 2010. 17(5): p. 673-679.
6.Lee, E.-Y., et al., Visual working memory deficits in patients with Parkinson's disease are due to both reduced storage capacity and impaired ability to filter out irrelevant information. Brain, 2010: p. awq197.
7.Pascual-Leone, J., A mathematical model for the transition rule in Piaget's developmental stages. Acta Psychologica, 1970. 32: p. 301-345.
8.Kail, R.V., Longitudinal evidence that increases in processing speed and working memory enhance children's reasoning. Psychol Sci, 2007. 18(4): p. 312-3.
9.Andrews, G. and G.S. Halford, A cognitive complexity metric applied to cognitive development. Cognitive psychology, 2002. 45(2): p. 153-219.
10.Miller, G.A., The magical number seven, plus or minus two: Some limits on our capacity for processing information. Psychological review, 1956. 63(2): p. 81.
11.Cowan, N., The magical number 4 in short-term memory: a reconsideration of mental storage capacity. Behav Brain Sci, 2001. 24(1): p. 87-114; discussion 114-85.
12.Buschman, T.J., et al., Neural substrates of cognitive capacity limitations. Proc Natl Acad Sci U S A, 2011. 108(27): p. 11252-5.
13.Fukuda, K., E. Awh, and E.K. Vogel, Discrete capacity limits in visual working memory. Curr Opin Neurobiol, 2010. 20(2): p. 177-82.
14.Zhang, W. and S.J. Luck, Discrete fixed-resolution representations in visual working memory. Nature, 2008. 453(7192): p. 233-5.
15.Luck, S.J. and E.K. Vogel, The capacity of visual working memory for features and conjunctions. Nature, 1997. 390(6657): p. 279-81.
16.Bays, P.M. and M. Husain, Dynamic shifts of limited working memory resources in human vision. Science, 2008. 321(5890): p. 851-4.
, K.A. and W. Kintsch, Long-term working memory. Psychol Rev, 1995. 102(2): p. 211-45.
18.Awh, E. and J. Jonides, Overlapping mechanisms of attention and spatial working memory. Trends Cogn Sci, 2001. 5(3): p. 119-126.
19.Pylyshyn, Z.W. and R.W. Storm, Tracking multiple independent targets: evidence for a parallel tracking mechanism. Spat Vis, 1988. 3(3): p. 179-97.
20.Gaspar, J.M., et al., Inability to suppress salient distractors predicts low visual working memory capacity. Proc Natl Acad Sci U S A, 2016. 113(13): p. 3693-8.
21.Gathercole, S.E., et al., The structure of working memory from 4 to 15 years of age. Developmental Psychology, 2004. 40(2): p. 177-190.
22.Ullman, H., R. Almeida, and T. Klingberg, Structural maturation and brain activity predict future working memory capacity during childhood development. J Neurosci, 2014. 34(5): p. 1592-8.
23.Klingberg, T., H. Forssberg, and H. Westerberg, Increased brain activity in frontal and parietal cortex underlies the development of visuospatial working memory capacity during childhood. J Cogn Neurosci, 2002. 14(1): p. 1-10.
24.Edin, F., et al., Mechanism for top-down control of working memory capacity. Proc Natl Acad Sci U S A, 2009. 106(16): p. 6802-7.
25.Zhou, X., et al., Age-dependent changes in prefrontal intrinsic connectivity. Proc Natl Acad Sci U S A, 2014. 111(10): p. 3853-8.
26.Klingberg, T., H. Forssberg, and H. Westerberg, Training of working memory in children with ADHD. J Clin Exp Neuropsychol, 2002. 24(6): p. 781-91.
27.Jaeggi, S.M., et al., Improving fluid intelligence with training on working memory. Proc Natl Acad Sci U S A, 2008. 105(19): p. 6829-33.
28.Jolles, D.D., et al., Functional brain connectivity at rest changes after working memory training. Hum Brain Mapp, 2013. 34(2): p. 396-406.
29.Meyer, T., et al., Stimulus selectivity in dorsal and ventral prefrontal cortex after training in working memory tasks. J Neurosci, 2011. 31(17): p. 6266-76.
30.Qi, X.L. and C. Constantinidis, Correlated discharges in the primate prefrontal cortex before and after working memory training. Eur J Neurosci, 2012. 36(11): p. 3538-48.
31.Constantinidis, C. and T. Klingberg, The neuroscience of working memory capacity and training. Nat Rev Neurosci, 2016. 17(7): p. 438-49.

话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 