阅读:0
听报道
撰文 | 秦曦明 (安徽大学物质科学与信息技术研究院,中国细胞生物学学会生物节律分会委员)
责编 | 徐 可
● ● ●
瑞典皇家科学院宣布将2017年诺贝尔生理学或医学奖授予杰弗里·霍尔(Jeffrey C. Hall)、迈克尔·罗斯巴什(Michael Rosbash)、迈克尔·扬(Michael W. Young),以表彰他们在近日节律(Circadian rhythms,人们通常也称其为生物钟)研究中取得的成就。他们用果蝇作为模式生物,克隆得到第一个生物钟基因,period(周期基因),并且发现周期基因所表达的周期蛋白会在晚上积累,白天则会降解,周期蛋白浓度会随着昼夜节律呈现规律性的24小时周期变化,从而提出控制近日节律的分子机制,转录翻译负反馈环路。

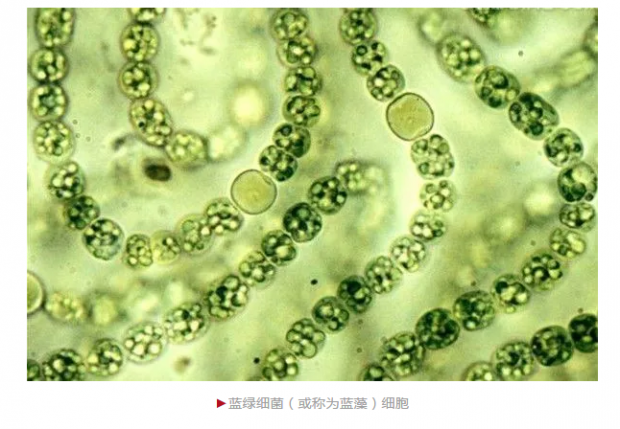
看到这个奖项的颁布,我为三位前辈高兴的同时,想起了生物钟领域中的“另类”成员,蓝绿细菌(或称为蓝藻)的生物钟,一个不以转录翻译负反馈环路驱动生物钟运行的分子机制。当然,“另类”或是凡夫俗子们对蓝绿细菌生物钟的看法。有人则视其为生物钟研究的“先驱”,一如现代遗传学之父孟德尔的遗传定律当年并不能被人理解,直到20世纪,人们才能理解“孟德尔遗传定律”的意义。
人们对自然界的生物存在一个内源的生物钟的认识由来已久,但一直认为生物钟仅存在于高等生物中,因为大多数高等生物的细胞分裂周期接近24小时,正好与生物钟的周期相近,而对于分裂时间远小于24小时的原核生物(例如大肠杆菌的分裂速度可以快至20分钟一代),人们不假思索地就排除了其存在昼夜振荡的生物钟。
但是,研究蓝绿细菌的科学家发现,固氮反应与氧气的存在是不相容的,而蓝绿细菌是地球上进行光合作用最大的物种群之一。就有人们开始推测,蓝绿细菌的固氮反应与光合作用发生于一天中不同的时间(即生物钟常常所说的相位)。不久,这个猜想得到证实,海洋蓝绿细菌聚球藻(Synechococcus)的光合作用在白天进行,而固氮作用在夜间进行,并且是内源存在的[1],这是典型的生物钟现象。
此时,卡尔·约翰逊(Carl H. Johnson) 完成了他在伍德兰德·黑斯廷斯(Woodland Hastings,美国科学院院士、海洋生物学及生物荧光领域专家)实验室的博士后研究,来到范德堡大学(Vanderbilt University)开展他的研究工作。眼光敏锐的约翰逊注意到了被人们忽视的蓝绿细菌,很快他就与世界顶尖的两位科学家,分子遗传学家苏珊·戈尔顿(Susan S. Golden)和植物生理学家近藤孝南(Takao Kondo),以蓝绿细菌为模式生物开始了合作。
他们三位1998年在Science上发表的文章中,克隆了重要的蓝绿细菌生物钟基因:kaiA,kaiB和kaiC。并且,基于霍尔和罗斯巴什在90年代初提出的转录翻译负反馈环路理论,他们提出蓝绿细菌生物钟运行的负反馈分子模型[2]。而高等哺乳动物的第一个生物钟基因,clock(钟基因),刚刚于1997年被约瑟夫·高桥(Joseph S. Takahashi)克隆得到[3]。

天下没有不散的宴席,三个合作良好的科学家选择了“分家”,一个做生物钟的输入信号,一个做生物钟的输出路径,一个做生物钟的分子机制。时间过得很快,其间生物钟领域的成果层出不穷,每年的会议报告都让听众兴奋不已。2005年,近藤孝南课题组在Science杂志发表了震动世界生物钟甚至生物学领域的成果,完全抛开了“转录翻译负反馈环路”理论,报道了一种简单至极的生物化学反应,解释了蓝绿细菌生物钟的运行本质[4]。
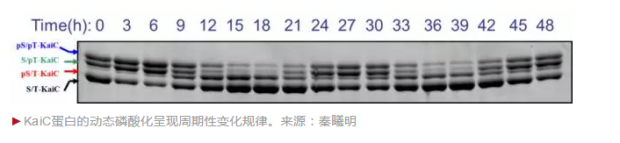
简单来说,近藤教授的课题组发现,原先认为要通过负反馈才能振荡的三个生物钟组分可以通过纯粹的生化反应产生振荡。KaiA,KaiB和KaiC三种蛋白混合在一起,无需转录和翻译过程,在能量供体(ATP)存在的情况下,KaiC蛋白的磷酸化会展现出近日节律振荡。KaiC的磷酸化位点有2个,分别是431位的丝氨酸和432位的苏氨酸。
读者可以从下面的蛋白电泳胶图中看到KaiC蛋白的动态磷酸化变化,其中KaiC蛋白的四条蛋白电泳条带的周期变化接近24小时(上面的三条带是磷酸化的KaiC)。这个发现非常完美,将没有生命的化学分子变化和生命现象(24小时的生物钟)联系在一起,体现了生命的本质。
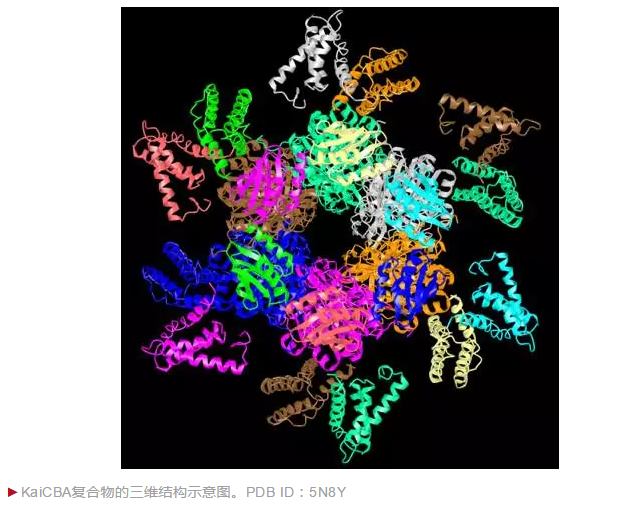
约翰逊和同在范德堡大学的马丁·艾格里(Martin Egli)展开合作,纯化并结晶了蓝绿细菌的KaiC蛋白,顺利解析其三维结构,是一个完美对称的正六聚体,从顶部看上去,像一个完美的时钟。随着近年冷冻电镜技术(2017年诺贝尔化学奖)的发展,更高分辨率的KaiC及其与KaiA和KaiB复合物的结构得到解析,为理解KaiC磷酸化的近日节律提供了清晰的注释[5]。下图的中心是正六聚体的KaiC蛋白,每个KaiC亚基结合1个KaiB单体,再结合2个KaiA单体,组成对称结构。
至此,蓝绿细菌生物钟作为一个从转录翻译负反馈环路模型的“局内人”,完全成为自成一体的“不依赖转录的生化振荡器”。本届诺贝尔生理学或医学奖得主,罗斯巴什,认为蓝绿细菌的生物钟与高等生物的进化起源不同。但是科学家基于蓝绿细菌的发现,近年在高等生物里发现了不依赖转录翻译负反馈环路的近日节律振荡[6],为生物机体生物钟的统一认识打开了一扇新的窗户。
谁又能断言,蓝绿细菌的生物钟运行的不依赖转录翻译的分子机制,会不会如同爱因斯坦在1916年所提出的引力波概念(2017年诺贝尔物理学奖,但受到物理学家几十年的质疑),在未来被发现是统一存在于所有的生物机体之中。
参考文献:
1. Mitsui A, Kumazawa S, Takahashi A, Ikemoto H, Cao S, Arai T. (1986) Strategy by which nitrogen-fixing unicellular cyanobacteria grow photoautotrophically. Nature. 323: 720-722.
2. Ishiura M, Kutsuna S, Aoki S, Iwasaki H, Andersson CR, Tanabe A, Golden SS, Johnson CH, Kondo T.(1998) Expression of a gene cluster kaiABC as a circadian feedback process in cyanobacteria. Science. 281:1519-1523.
3. King DP, Zhao Y, Sangoram AM, Wilsbacher LD, Tanaka M, Antoch MP, Steeves TD, Vitaterna MH, Kornhauser JM, Lowrey PL, Turek FW, Takahashi JS. (1997) Positional cloning of the mouse circadian clock gene. Cell. 89: 641-653.
4. Tomita J, Nakajima M, Kondo T, Iwasaki H. (2005) No transcription-translation feedback in circadian rhythm of KaiC phosphorylation. Science. 307: 251-254.
5. Snijder J, Schuller JM, Wiegard A, Lössl P, Schmelling N, Axmann IM, Plitzko JM, Förster F, Heck AJ. (2017) Structures of the cyanobacterial circadian oscillator frozen in a fully assembled state. Science. 355:1181-1184.
6. O'Neill JS, Reddy AB. (2011) Circadian clocks in human red blood cells. Nature. 469: 498-503.

话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 