阅读:0
听报道
编者按
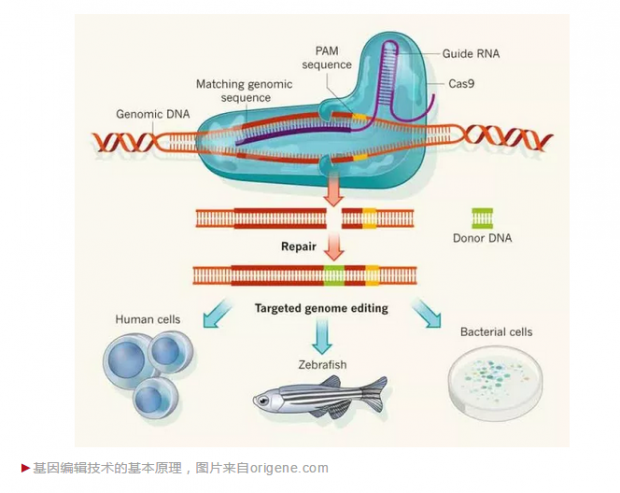
北京时间12月19日,《自然》公布了年度10大人物,Broad研究所David Liu开发出了一款全新的“碱基编辑器”而当选,2013年张锋同样因为CRISPR基因编辑技术的开发而入选。由此可见CRISPR基因编辑技术备受外界关注。事实上,对于一项重大的科学发现来说,其历程往往漫长且荆棘丛生,但一旦时机成熟,它将会快速发展并得到广泛应用,CRISPR基因编辑技术也不例外。30多年前,科学家在细菌中发现规律间隔成簇短回文重复序列,之后发现这种重复序列可让细菌对病毒有免疫抗性。但这一现象之所以能迅速引燃每个分子生物学家的实验室,主要是因为该序列衍生的RNA可引导蛋白质结合特定DNA片段,从而引起目标DNA上的双链断裂,该技术简单并且极为高效。
《知识分子》将陆续介绍基因编辑技术的前沿进展。本系列文章由上海科技大学生命科学与技术学院刘冀珑教授主持策划。
撰文 | 刘 奕 王俏琦 张波 章元兵 张子恒 周爽(上海科技大学生命科学与技术学院)
责编 | 叶水送

三十年前,实验生物学家在分析寄居于人类肠道的细菌的一个基因时,偶然发现一组重复回文密码。之后这类密码在其他细菌基因组陆续被发现。通过计算生物学家的缜密计算,判定该类密码是细菌抵制外敌入侵的关键手段。这个判定结果随后被实验生物学家在酸奶工厂得到证实。数年后,这类密码被利用,引发基因编辑领域的爆炸……这类密码的名字叫做CRISPR。
作为当今生命科学领域最火热的基因编辑技术,CRISPR因其高效、便捷、适用范围广,为科研工作者带来了福音,同时其广泛应用也促进了基础科研、农业、基础医学及临床治疗的发展。下面让我们穿越到三十年前,细数CRISPR系统的发现发展过程。
1987年,Nakata研究组在分析大肠杆菌(Escherichia coli)中基因iap及临近序列(flanking regions)时,偶然地发现在位于iap的3’端存在含有29个碱基的高度同源序列重复性出现,且这些重复序列被含32个碱基的序列间隔开,当时科学家并不清楚这种序列的生物学意义。随后的几年(1989年-1999年),陆续有相关研究指出类似的重复序列存在于多种细菌及古生菌中。2000年,Mojica和同事通过比对发现这种重复元件存在于20多种细菌及古生菌中,并将这种核酸序列命名为短规律性间隔重复序列(Short Regularly Spaced Repeats, SRSRs),因其高度保守性,猜测其一定具有重要的生物学功能。

CRISPR一词正式登上历史舞台还是2002年的事。Jansen实验室通过生物信息学分析,发现这种新型DNA序列家族只存在于细菌及古生菌中,而在真核生物及病毒中没有被发现,并将这种序列称为规律间隔成簇短回文重复序列(clustered regularly interspaced short palindromic repeats, CRISPR)。他们将临近CRISPR locus的基因命名为cas(CRISPR-associated),并发现了4个cas基因(cas1, cas2, cas3, cas4)。2005年,Mojica,Bolotin和Pourcel三个研究组指出CRISPR中的间隔序列来自于外来噬菌体或质粒,其中Mojica实验室惊喜地发现病毒无法感染携带有与病毒同源间隔序列的细胞,而易侵入那些没有间隔序列的细胞,由此他们提出CRISPR可能参与细菌的免疫功能的假说。
CRISPR能在细菌的免疫功能中起作用在2007首次得到实验证实。Horvath研究组发现嗜热链球菌被病毒入侵后整合了来自噬菌体基因组新的间隔区序列,同样的病毒再次入侵时细菌就有了抗性,使其免遭攻击。同时人为地去除或添加特定的间隔区序列,会影响细菌的抗性表型。因此,他们认为CRISPR及cas基因一起为嗜热链球菌提供了对噬菌体的抗性作用,同时抗性的特异性取决于CRISPR中的间隔区序列,细菌的这种免疫性是可以遗传的。至此,虽然科学家并不清楚CRISPR/Cas抵抗病毒的具体机制,但他们开始逐渐揭开其神秘的面纱。
2008年,Oost实验室揭示了宿主细胞中CRISPR的间隔序列如何在cas蛋白的协助下介导发挥抗病毒作用。他们发现在CRISPR转录后,cas蛋白会形成一个称为Cascade的复合物,裂解每个重复单元中的CRISPR RNA前体(pre-crRNA),但裂解产物都保留了间隔序列。在解旋酶cas3的作用下,成熟的CRISPR RNA(crRNA)发挥小向导RNA(small guide RNA)的角色,促使Cascade干预病毒的增殖。2009年,Mojica团队指出前间隔序列临近的PAM序列为原核生物中CRISPR/Cas发挥免疫识别提供了靶标。
2011年,Charpentier研究组通过对人类病原体化脓性链球菌的差异化RNA测序,揭示了反式编码crRNA(tracrRNA)参与pre-crRNA的加工成熟过程。他们指出,tracrRNA通过24个核苷酸与pre-crRNA中的重复序列互补配对,在保守的内源性RNA酶III和CRISPR相关的Csn1蛋白的参与下指导pre-cr RNA的成熟过程,这些组分对保护化脓性链球菌免受噬菌体DNA的入侵必不可少,研究揭示了crRNA成熟的新途径。
以上我们一直在介绍CRISPR/Cas的发现及细菌、古细菌如何利用该系统来沉默外来核酸以抵御病毒及质粒的入侵。CRISPR/Cas作为基因编辑系统被应用最早开始于2012年两位女神的强强联合,她们分别是来自加州大学伯克利分校的结构生物学家詹妮弗·杜德纳(Jennifer Doudna)和瑞典于默奥大学的埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)。她们通过体外实验证明:成熟的crRNA通过碱基互补配对与tracrRNA形成特殊的双链RNA结构,指导cas9蛋白在目标DNA上引起双链断裂。在与crRNA指导序列互补的位点,cas9蛋白的HNH核酸酶结构域切割crRNA的互补链,而cas9蛋白RuvC样结构域切割非互补链。当双tracrRNA:crRNA被嵌合到一条RNA时,同样可以指导cas9切割双链DNA。她们的研究证明,在双链RNA指导下切割双链DNA断裂的内切酶家族并揭示了CRISPR/Cas系统在RNA指导下进行基因编辑的巨大潜力。

之后就一发不可收拾,紧接着是2013年初的两篇Science和一篇Cell文章,它们分别由来自于哈佛大学医学院的George Church、麻省理工学院博德研究所的张锋以及加州大学旧金山分校系统及合成生物学中心的Lei S. Qi(目前就职于斯坦福大学)实验室,这三篇文章都将CRISPR/Cas系统成功应用到哺乳动物细胞中。其中Church研究组设计了II型CRISPR/Cas系统,在人类细胞中设计特定的gRNA。对于内源性AAVS1基因座,他们成功获得了293T细胞中10%至25%,K562细胞中13%至8%以及诱导多能干细胞中2%至4%的靶向率。他们同时表明这个过程依赖于CRISPR组件,是特定的序列;在同时引入多个gRNA时,可以实现对目标基因座的多重编辑。张锋实验室证实了cas9可以在小RNA的指导下在人类及小鼠细胞中对内源基因座实现精确切割,同时他们将cas9改造为缺口酶促进同源修复。Qi与同事则将II型CRISPR/Cas系统中的cas9蛋白改造成失去核酸内切酶活性的dCas9,将其与gRNA共表达,产生一种DNA识别复合物使其特异性地干扰转录延伸,RNA聚合酶或转录因子与DNA的结合达到抑制目标基因表达的目的。他们将其称为CRISPRi,实现了对大肠杆菌中基因的有效抑制,且没有明显的脱靶效应。而且可以实现同时抑制多个基因,他们表明CRISPRi也适用于哺乳动物细胞。很快人们利用CRISPR/Cas系统实现了对斑马鱼、真菌及细菌的基因编辑。2013年5月,Jaenisch研究组利用CRISPR/Cas介导的基因工程技术制造了在多个基因上含有多重突变的小鼠,极大地促进了体内多基因的功能学研究。随后,人们实现了对果蝇、线虫、大鼠、猪、羊、以及水稻、小麦、高粱等多种生物的基因编辑。
距开始利用CRISPR/Cas进行基因编辑不到一年时间里,人们就实现了用该系统来校正遗传疾病。2013年12月,李劲松研究组和Hans Clevers研究组利用CRISPR/Cas9系统分别校正了小鼠白内障及人干细胞中一种与囊肿性纤维化相关联的基因缺陷。同时,研究者通过向人类细胞转染慢病毒包装的sgRNA库,实现了对基因组范围的功能性筛选。2015年4月,黄军就和团队首次修饰人类胚胎DNA,为治疗一种在中国南方儿童中常见的遗传病——地中海贫血症提供了可能。
随着对CRISPR系统研究的不断深入,也暴露了一定的缺陷和局限性,如严重的脱靶效应。2015年9月,张锋研究组报道了一种不同于Cas9的新型2类CRISPR效应因子Cpf1。他们的研究证明,Cpf1是一种不依赖tracrRNA,由单个RNA介导的核酸内切酶。Cas9是在同一个位置同时剪切DNA分子的双链,形成的是平末端;而Cpf1剪切后形成是两个不同长度的链,被称之为黏性末端。同时Cpf1能够识别富含胸腺嘧啶(T)的PAM序列,可以扩展CRISPR的编辑范围。
已知的许多遗传疾病由点突变引起,然而目前纠正点突变的方法存在效率低或引起随机缺失或插入等缺陷。2016年4月,David R. Liu研究组报道了一种碱基编辑的新方法。他们将胞嘧啶脱氨酶与CRISPR/Cas9进行融合,在gRNA的指导下,不引起DNA双链断裂,直接实现胞嘧啶(C)到尿嘧啶(U)的转变,而DNA复制进一步使得U被T代替,从而实现C→T (or G→A)的转换。这种碱基编辑器可有效纠正多种与人类疾病相关的点突变。他们还发展了第二、第三代碱基编辑技术,进一步提高碱基编辑效率。在此基础上,上海科技大学陈佳研究组与合作者共同开发了一种增强型碱基编辑器。他们发现,将含有尿嘧啶DNA糖基化酶抑制剂(UGI)的质粒与sgRNA/BE3共同转染293FT细胞,经深度测序分析,与单独转染sgRNA/BE3相比,共转染的方法减低了错配频率并提高了C-到T-的替换效率。他们还发现UGI的表达水平与C-到T-的碱基替换效率成正相关。为了提高实验的方便性,研究者还将多个重复UGI与BE共表达在同一载体,与靶向不同基因座的多个sgRNA共同转染293FT细胞,结果表明这种增强型碱基编辑器大大提高了编辑效率。
2016年6月,张锋研究组发现一种来自纤毛菌(Leptotrichia shahii)的效应因子C2c2(现被称为cas13a),具有RNA介导的RNA酶功能。体外生化分析显示C2c2可在单个crRNA指导下剪切靶向单链RNA。细菌内,C2c2可被用来敲低特异性的mRNA,RNA酶活性依赖于HEPN结构域,C2c2是第一个被发现的靶向RNA的CRISPR效应因子。
2016年10月,第一个由CRISPR/Cas9编辑进行的临床治疗实验由Lu团队完成,研究者分离患有转移性非小细胞肺癌病人血液中的免疫细胞,特异性的敲除PD-1基因,对细胞扩增培养后输回患者体内以期抵抗癌症。
2017年10月,David R. Liu团队将编码tRNA腺嘌呤脱氨酶(TadA)的基因引入大肠杆菌内,经历了漫长的7代筛选后,开发出了一款全新的“碱基编辑器”,将进化后的TadA与CRISPR/Cas9系统融合,在不引起DNA链断裂的情况下实现了A•T到G•C的转换,且在人体细胞中,编辑效率超过了50%。这样就实现了C•G 到 T•A和A•T 到G•C的高效编辑,为多种遗传疾病的治疗提供了有效工具。
注:本文作者署名排列不分先后,按作者姓的拼音排序。

话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 