撰文 | 剪刀手
责编 | 叶水送
人类的很多疾病都是由单基因位点突变造成,通过现有的基因编辑技术能很好地对这些突变位点进行修复。Broad研究所华人学者David Liu等学者发明了一种新的基因编辑工具:碱基编辑器(Base Editing),能够在不通过DNA双链断裂的情况下,通过实现碱基的替换,从而实现对基因组点突变的修复。
凭借在Cas9碱基编辑器领域的一系列工作,David Liu成为2017年生命科学领域的热门学者,先后被评为Nature年度10大人物之一、其工作亦被Science评为10大年度科学突破之一。
近日,上海科技大学生命学院陈佳教授研究组、中国科学院-马普计算生物学研究所研究员杨力研究组与上海科技大学生命学院黄行许教授研究组通过合作研究,开发出一系列基于CRISPR/Cpf1(Cas12a)的新型碱基编辑器(Cpf1-BE),相关成果以“Base editing with a Cpf1– cytidine deaminase fusion”为题,在《自然-生物技术》(Nature Biotechnology)杂志上在线发表。

传统的CRISPR/Cas9基因编辑技术虽然具有较高的基因敲除效率,但在执行碱基替换(譬如对造成遗传性疾病的点突变进行矫正)时效率通常很低,这也限制了CRISPR/Cas9基因编辑的应用。
近年,利用将CRISPR/Cas9和APOBEC(胞嘧啶脱氨酶)整合而发展出的新型碱基编辑系统(Base Editor, BE),可在单碱基水平(如胞嘧啶向胸腺嘧啶)实现高效率的基因组靶向编辑改造。这种新型碱基编辑系统理论上可对数百种引起人类疾病的基因组点突变进行定点矫正,因此拥有巨大的临床应用潜力。
目前,已报道的碱基编辑系统均是利用Cas9蛋白(主要是Streptococcus pyogenes Cas9, SpCas9和Staphylococcus aureus Cas9, SaCas9),来执行与基因组的靶向性结合,而这种靶向性结合依赖于靶点旁侧的前间区序列邻近基序序列PAM(Protospacer Adjacent Motif, PAM)序列。SpCas9和SaCas9蛋白所识别的PAM序列多含鸟嘌呤/胞嘧啶(G/C-rich),因此利用已报导的碱基编辑系统无法在腺嘌呤/胸腺嘧啶富集(A/T-rich)区域进行高效的碱基编辑操作。
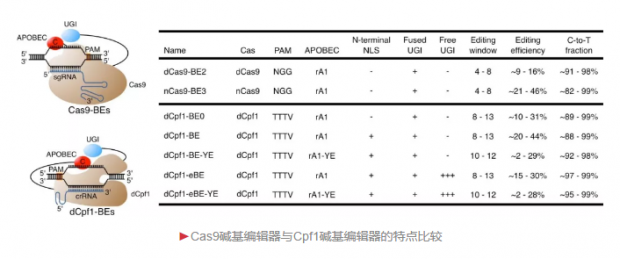
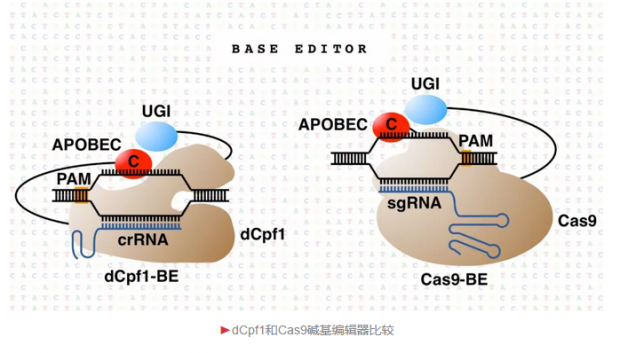
在这项最新的研究中,来自上海科技大学和中科院的科研人员通力合作,构建了一系列基于CRISPR/Cpf1蛋白的新型碱基编辑器(Cpf1-BE)。由于Cpf1 蛋白可识别富含腺嘌呤/胸腺嘧啶的PAM序列,这种基于Cpf1的新型碱基编辑器实现了在腺嘌呤/胸腺嘧啶富集区域的碱基编辑操作。在拓展编辑区域的同时,基于Cpf1的新型碱基编辑器所产生的编辑副产物也较低,因此具有更高的编辑精准度。这种基于Cpf1的新型碱基编辑器与现有的基于Cas9的碱基编辑器可实现碱基编辑的有效互补,为碱基编辑系统在基础研究及未来临床领域的全面深入应用提供了新方法、拓展了新思路。
文章链接:
Li XS et al. Base editing with a cpf1–cytidine deaminase fusion. Nat Biotech, 2018, doi:10.1038/nbt.4102.

0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 