撰文 | 中山大学中山眼科中心
血管是人体最重要的器官之一,为组织输送氧气和营养,维持其正常形态和功能。血管受严格代谢调控从而维持稳定状态,其代谢失衡会导致血管受损和病理性增生,从而引发或加剧病变,包括眼血管性疾病和肿瘤。
抗新生血管生成药物的研发一直以新生血管形成相关因子为主要靶点,如血管内皮生长因子(VEGF)。但抗VEGF药物只对部分患者有效并易产生耐药,因此亟需研究新生血管形成的新机制新通路,以利于新药研发。

目前,血管内皮细胞代谢途径的研究正在获得越来越多的关注。在病理条件下,血管由静止状态转变为激活状态,在多种促新生血管成长因子的作用下,血管内皮细胞分裂、迁移,并分化成为茎细胞和顶端细胞,从而完成血管出芽新生过程(见下图)。在这个过程中,血管细胞需要通过高水平的新陈代谢获得大量的能量和物质。因此,血管内皮细胞的新陈代谢对新生血管的生成至关重要,有可能成为新的抗新生血管的关键靶标。
今年3月,Science杂志发表的一篇文章[1]对血管内皮细胞代谢在眼及肿瘤等新生血管相关疾病中的作用和机制进行了讨论,提出了将血管内皮细胞代谢途径作为抑制病理性新生血管的关键靶标的新策略。
文章的作者为中山大学中山眼科中心眼科学国家重点实验室副主任李旭日教授和比利时鲁汶大学血管生物学及代谢实验室主任Peter Carmeliet院士。
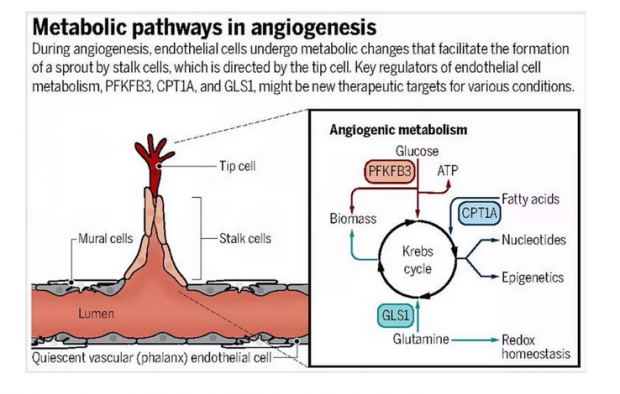
近期研究[2-10]揭示了多个血管内皮细胞的代谢途径,为抗血管新生治疗提供了新的靶点。这些代谢途径包括由PFKFB3和FGF2调节的内皮细胞糖酵解途径、CPT1A介导的内皮细胞脂肪酸氧化途径、GLS1调节的谷氨酰胺代谢途径、ASNS调节的天冬酰胺代谢途径等。尽管血管内皮细胞代谢领域的研究目前仍处于萌芽阶段,但对血管内皮细胞代谢作用和机理的进一步研究将会揭示血管性疾病的新机制,为研发血管性疾病的诊疗方法带来新的希望。
最新研究表明[2],[3],血管内皮细胞代谢在血管形成和功能中起关键作用,深入研究其作用与机理将有助于揭示血管性疾病的新机制,为研发新的诊疗方法奠定基础。靶向调控血管内皮细胞代谢对血管生长、稳态和功能至关重要,有巨大研究价值和临床应用潜力。
References
1 Li, X. &Carmeliet, P. Targeting angiogenic metabolism in disease. Science 359, 1335-1336,(2018).
2 Wong, B. W. et al. The role of fatty acid beta-oxidation in lymphangiogenesis. Nature 542, 49-54, (2017).
3 Cantelmo, A. R. et al. Inhibition of the GlycolyticActivator PFKFB3 in Endothelium Induces Tumor Vessel Normalization, ImpairsMetastasis, and Improves Chemotherapy. Cancer Cell 30, 968-985, (2016).
4 Quaegebeur, A. et al. Deletion or Inhibition of the Oxygen Sensor PHD1 Protects against Ischemic Stroke via Reprogramming of Neuronal Metabolism. Cell Metabolism 23, 280-291, (2016).
5 Rafii, S. &Carmeliet, P. VEGF-B Improves Metabolic Health through Vascular Pruning of Fat. Cell Metabolism 23, 571-573, (2016).
6 Schoors, S. et al. Fatty acid carbon is essential for dNTP synthesis in ECs. Nature 520, 192-197, (2015).
7 Ghesquiere, B.,Wong, B. W., Kuchnio, A. & Carmeliet, P. Metabolism of stromal and immune cells in health and disease. Nature 511, 167-176, (2014).
8 Schoors, S. et al. Partial and transient reduction of glycolysis by PFKFB3 blockade reduces pathological angiogenesis. Cell Metabolism 19, 37-48, (2014).
9 De Bock, K.,Georgiadou, M. & Carmeliet, P. Role of EC Metabolism in Vessel Sprouting. Cell Metabolism, (2013).
10 De Bock, K. et al. Role of PFKFB3-Driven Glycolysisin Vessel Sprouting. Cell 154, 651-663, (2013).

0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 