阅读:0
听报道
撰文 | 廖俊棋(中科院古脊椎动物与古人类研究所)
责编 | 惠家明
6600万年前,一颗直径10公里的小行星撞击地球,其威力连百万枚核弹都望尘莫及。如此飞来横祸引起地震、海啸、森林大火以及火山的高度活跃,扬起的尘土遮天蔽日。辉煌的恐龙王朝被这一连串剧变终结,仅剩下一支后裔幸存至今——鸟类。
鸟类起源于1.65亿~1.5亿年前的侏罗纪时期,是兽脚类恐龙的后代,至今仍有超过10000个现生种广布全球。人们也许会好奇,同样是经历了小行星撞击,凭什么恐龙灭绝消失,鸟类反而繁衍昌盛了呢?
实际上,这是一个误解。人们往往忽略了这样一个事实:白垩纪末期的大灭绝也造成了部分鸟类的绝种。其中,只有“今鸟类”(Neornithes)这一类群熬过了生物大灭绝事件[1]。
那么,今鸟类为何能一枝独秀地幸存下来?学者们有各种推测,这其中包括了快速生长素率假说、高代谢率假说。还有研究认为,这要归因于今鸟类拥有更强大的肌肉骨骼系统,以及它们的喙部更适合吃种子[2-6]。而Current Biology杂志最新的封面文章则指出:地栖生活也许才是这些鸟类躲过灭绝的真正原因[7]。

消失的森林
在我们的印象中,多数鸟类的生活是和树木分离不开的。但是发表上述封面文章的巴斯大学等机构的研究团队则发现,在地球遭受行星撞击后,鸟类几乎“无树可居”。
小行星撞击地面的瞬间,光是冲击波就铲平了方圆1500公里的森林,高温更造成大火蔓延。雪上加霜的是,灰烬所带来的酸雨、粉尘所带来的日光遮蔽,最终引发了植物生态系统的崩盘[8-10]。而该研究团队进一步指出,此次森林灾难不仅是全球性的,更维持了将近一千年的时间。
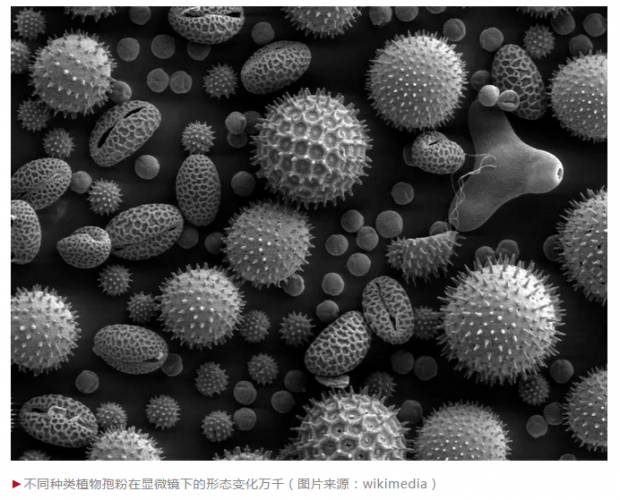
他们之所以敢下如此结论,其证据来自孢粉化石。孢粉,指的是植物的孢子及花粉。不同种类植物的孢粉形态殊异,好比人的指纹一样。植物体大多非常脆弱,能形成化石的少之又少。但是孢粉有着坚实的外壁,易于形成化石,且数量众多。举例来说,欧亚槭(Acer pseudoplatanus)的一朵花里就含有约9万粒花粉,林山毛榉(Fagus silvestris)甚至超过了63万粒,数量极为惊人。所以,在植物死亡消失后,我们根据岩石中遗留下的孢粉化石,就能反推出当时的植被面貌。此外,它们的分布非常广泛。从热带雨林到寒带苔原,从高山、湖泊到海洋,孢粉化石如尘土般无处不在,这样的丰富程度让孢粉完全能适用于定量统计。
因此,该团队远赴美国、新西兰等地,搜集了世界各地生物大灭绝时期岩层的孢粉数据。鉴定结果显示,在小行星撞击后很长一段时间里,各地岩层中保存的孢粉构成出奇地相似,其70%以上的孢粉化石都来源于两种蕨类植物。而裸子、被子植物则处于衰退状态,遗留下的孢粉很少,直到千年之后才开始复苏[7]。
这种由蕨类植物主导的植被组合有个专门的名字——灾害植物群(disaster flora)。今天,在火山爆发后的夏威夷也能看到蕨类植物灾后称霸一地的光景。我们知道,蕨类植物普遍低矮,而在裸子和被子植物中多见比较高大的树木种类。这意味着,在灾害植物群延续的一千年时光里,可能全球的鸟类几乎都找不到合适的树梢栖息。
地栖的鸟类祖先们
既然没有像样的树林,树栖的物种显然会处于劣势,而地栖的生物反而更有优势。
虽然现今的鸟类绝大部分是树栖,但演化系统分析的结果却告诉我们,今鸟类的祖先其实是个地栖的原始类群。人们熟知的鸵鸟,以及既能飞又适应树栖的䳍鸟都是这个原始类群关系最近的后裔。所以说,今鸟类祖先在灾难发生前就已经适应了地面生活。灾难发生后,它们不会因为树林的消失而无处繁衍、觅食,从而得以逃过此劫。而新的化石发现也进一步证明,灾后幸存下来的鸟类只有今鸟类,其后肢的比例、身体结构都是适应地栖生活的[7]。

相比之下,反鸟类(Enantiornithes)本是恐龙时代最为常见的鸟类,但它们却在那场灭绝事件中惨遭淘汰。研究者认为,反鸟类的灭绝可能与树栖的习性密不可分。想要适应树栖的生活,后肢必须有许多形态学的特化。例如,树栖生活要配备善于抓握的长指爪[7],这会对陆地行走或栖息造成不便。更遑论,长久以来的树栖习性有不少行为学的影响,比如要在树上筑巢、哺育后代等等。研究者指出,反鸟类大多都高度适应树栖生活,然而小行星撞击所带来森林生态系崩坏,导致反鸟类的栖息环境全面消失,最终断绝了这种鸟类存续的活路。

总的来说,孢粉学、现代鸟类演化谱系、鸟类化石等多方面研究结果都显示:灾难后幸存的现代鸟类祖先应该是小型的、能飞的,且最重要是能适应地栖生活的物种。这场浩劫中,今鸟类祖先的地栖习性救了它们一命。而现在窗外那些盘踞树梢,百啭千声的鸟类,则是在森林环境恢复之后,才学会跃上枝头的。
参考文献
1. Brusatte, S. L., O'Connor, J. K., & Jarvis, E. D. (2015). The origin and diversification of birds. Current Biology Cb, 25(19), 888-98.
2. Brusatte, S. (2016). Evolution: how some birds survived when all other dinosaurs died. Current Biology Cb, 26(10), R415.
3. Erickson, G.M., Rauhut, O.W., Zhou, Z., Turner, A.H., Inouye, B.D., Hu, D., and Norell, M.A. (2009). Was dinosaurian physiology inherited by birds? Reconciling slow growth in Archaeopteyrx. PLoS One 4, e7390.
4. Chinsamy, A. (2002). Bone microstructure of early birds. In Mesozoic Birds: Above the Heads of Dinosaurs, L.M. Chiappe, and L.M. Witmer, eds. (Berkeley: Univ. of California Press), pp. 421–431.
5. Padian, K., and Horner, J.R. (2004). Dinosaur physiology. In The Dinosauria, 2nd Edition, D.B. Weishampel, P. Dodson, and H. Osmo´ lska, eds. (Berkeley: Univ. of California Press), pp. 660–671.
6. Grady, J.M., Enquist, B.J., Dettweiler-Robinson, E., Wright, N.A., and Smith, F.A. (2014). Evidence for mesothermy in dinosaurs. Science 344, 1268–1272.
7. D.J. Field et al. (2018). Early evolution of modern birds structured by global forest collapse at the end-Cretaceous mass extinction. Current Biology. Vol. 28, doi: 10.1016/j.cub.2018.04.062.
8. Anders, E., Wolbach, W.S., and Gilmour, I. (1991). Major Wildfires at the Cretaceous-Tertiary Boundary. In Global Biomass Burning: Atmospheric, Climatic and Biospheric Implications, J.S. Levine, ed. (MIT Press), pp. 485–492.
9. Ohno, S., Kadono, T., Kurosawa, K., Hamura, T., Sakaiya, T., Shigemori, K., Hironaka, Y., Sano, T., Watari, T., and Otani, K. (2014). Production of sulphate-rich vapour during the Chicxulub impact and implications for ocean acidification. Nat. Geosci. 7, 279–282.
10. Vellekoop, J., Esmeray-Senlet, S., Miller, K.G., Browning, J.V., Sluijs, A., van de Schootbrugge, B., Damste, J.S.S., and Brinkhuis, H. (2016). Evidence for Cretaceous-Paleogene boundary bolide ‘‘impact winter’’ conditions from New Jersey, USA. Geology 44, 619–622.

话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 