阅读:0
听报道

本文将解读2021年诺贝尔生理学或医学奖:温度和触觉感受器的发现 | 图源:
导 读
对感觉系统的探索,一直颇受诺奖的青睐,1914年内耳罗伯特·巴拉尼在前庭器官的生理和病理方面的工作,1967年瓦尔德对视黄醛参与视觉形成机制的诠释,2004年理查德·阿克塞尔和琳达·巴克对人体气味受体和嗅觉系统组织方式的研究…… 每一种感觉的揭秘,都是人类与客观世界一次意义重大的握手。
今日文章,将深入解读2021年诺贝尔生理学或医学奖工作:温度和触觉感受器的发现。
撰文|付小雨 褚刘薇 沈伟(上海科技大学生命科学与技术学院)
人类如何感知、理解和重建外部世界?从新生儿第一次睁开双眼,听到母亲第一声温柔的呼唤开始,庞大而精妙的感觉系统就开始一刻也不停歇地运作起来,让我们得以欣赏美景,嗅闻花香,聆听音乐,品尝美食。
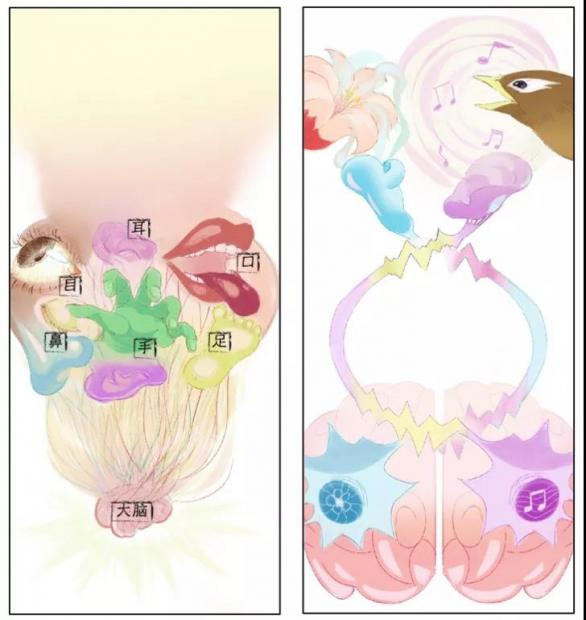
图1 感觉系统原理图(褚刘薇)
2021年10月4日,诺贝尔生理学或医学奖宣布授予美国研究者大卫·朱利叶斯(David Julius)和阿登·帕塔普蒂安(Ardem Patapoutian),以奖励他们关于 “发现温度和触觉受体” 的突破性成就,在人类理解自身与外部世界交互的历史上写下了弥足轻重的一笔。

今天,我们就来谈谈这两种分别源于 “能尝出辣味的细胞” 和 “失去触觉的细胞” 的非典型感觉受体的发现。
1 能尝出辣味的细胞
人们满头大汗,龇牙咧嘴,却仍然不断地把筷子伸进漂浮着辣椒的通红火锅,边吃边直喊 “辣得爽”。“辣” 为何让他们着迷?“辣-热-痛” 之间到底存在什么样的神秘联系?“辣”能够为人类与客观世界交互打开什么样的独特窗口?

图2 人们在吃辣时会感到痛和热 | 褚刘薇
“辣” 的故事,要从一只 “失明” 的果蝇讲起。1969年,在爱丁堡大学这所有着500多年历史的古老大学里,动物学系的两名研究者 D. J. Cosens 和 Aubrey Manning 正忙碌观察着一只 “失明” 的果蝇。这只果蝇,基因发生了突变,病症十分奇特,在低环境光下有着像正常果蝇一样的趋光性,但当给予连续光刺激时,却表现出失明症状,无法像正常果蝇一样调整姿势而趋向有光的一侧,只能毫无方向、跌跌撞撞地飞行。在医院里,医生通常用心电图仪监测病人心脏。而在实验室里,两位研究者利用神经场电位记录技术(filed potential)监测这只生病的果蝇的视网膜。果然,在视网膜电流图(ERG)的记录中,他们发现这只突变体果蝇表现出了畸形的样式,不能像野生型那样在受到光刺激时维持持久的视网膜电位变化(图3)[1]。随后,根据视网膜电流图中出现的瞬时电位的特征,这个突变基因被命名为trp(transient receptor potential)[2]。
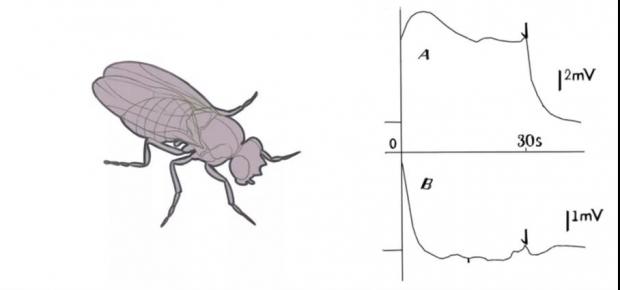
图3 TRP突变体果蝇视网膜电流图 [1] 注:A,30s连续光照下野生型果蝇视网膜电流;B,30s连续光照下TRP突变体果蝇无法维持持久的视网膜电位变化。
不过随后十几年,受分子生物学的发展所限,始终不见关于trp 基因的新研究。直到20世纪80年代生物学进入风起云涌的基因克隆时代,才有相关的研究进展。当时,美国加州大学伯克利分校 Gerald Rubin 实验室的博士后 Craig Montell 利用该实验室刚刚开发出的果蝇转基因技术 [3,4],将疑似含有trp 的DNA片段通过转基因技术导入 “失明” 果蝇的基因组,“失明” 症状果然消失了 [5]。随后,他又利用分子生物学克隆出了trp 的DNA序列,并预测这可能是一个离子通道蛋白基因 [6](图4)。
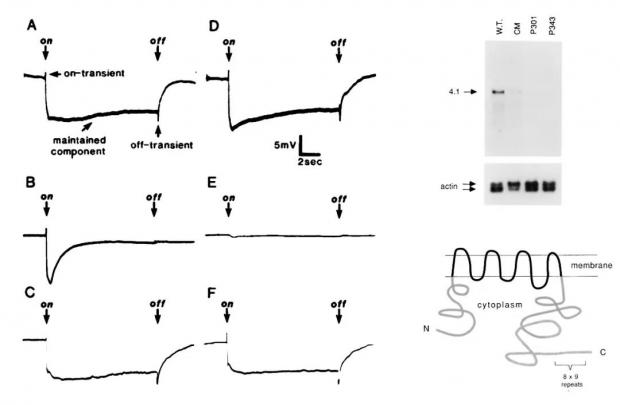
图4 挽救trp基因突变性状trp基因的克隆 [5,6] 注:左,通过转基因技术使trp基因突变果蝇可以重新维持持久的视网膜电位变化;右上,对突变等位基因trp的RNA分析;右下,TRP蛋白预测结构。
随着基因组学的发展,人们很快发现在哺乳动物中有超过30个TRP通道家族成员,包含7个亚族 [7]。但是这些蛋白到底有什么生理作用呢?是否具有保守的视觉传导功能?在上个世纪末,这一切都还是未知的,直到本次诺奖得主、加州大学旧金山分校(UCSF)的朱利叶斯成功克隆辣椒素受体,才掀起了TRP研究的热潮。现在人们知道,TRP家族蛋白不仅参与光感应,还感应温度和刺激性化学物质,并参与肿瘤迁移等,具有非常丰富的生物学功能。
朱利叶斯自研究生时代就对植物的天然产物,如辣椒素、薄荷醇、芥末等等,是如何被人类感知的充满巨大的好奇。他说,“当我走在超市里,货架上一排排辣椒酱简直是在乞求我去探索它们被感知的奥秘。” 1990年代后期,他进行了一项鉴定辣椒素受体的项目。基于上世纪中叶科学家们对吃辛辣食物时会产生灼烧感这一现象的关注,朱利叶斯认为,了解辣椒素的作用机制有助于促进人们对疼痛信号的理解。
值得一提的是,朱利叶斯的博士和博士后导师均为诺奖获得者。其博士导师之一 Randy Schekman(另一位为Jeremy Thorner)因揭示突触传导机制而获奖;其博士后导师 Richard Axel 因克隆嗅觉受体而获奖。Julies在博后期间通过表达克隆与电生理分析相结合的方式,成功分离出了编码5-羟色胺受体1C的基因(图5)[8]。这为他后期克隆辣椒素受体奠定了基础。
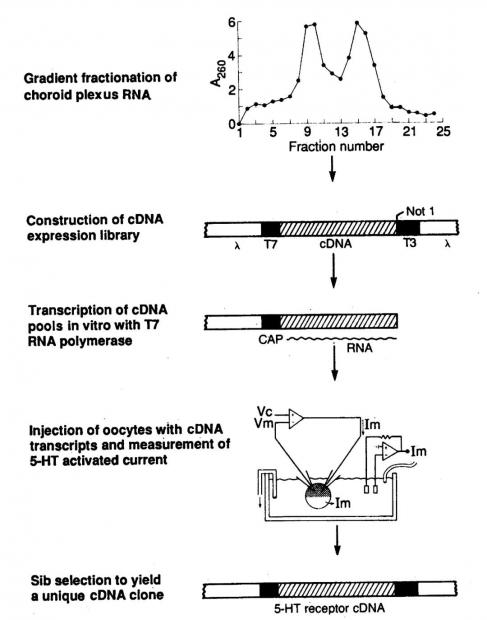
图5 5-羟色胺受体1c的表达克隆[8]
朱利叶斯在UCSF获得独立教职后,决定与博士后研究员 Michael J. Caterina 采用他博后期间开发的这套克隆方法,对辣椒素受体进行无偏见的功能筛选,其假设是单个基因可以在通常对辣椒素不敏感的细胞中赋予辣椒素敏感性。为了找到这个假定的基因,Julius和同事从啮齿动物背根神经节——其中包含辣椒素激活的感觉神经元的细胞体——中制作了一个cDNA文库。用这些cDNA批次转染对辣椒素不敏感的细胞,期待最终找到能 “尝出辣味” 的单个cDNA克隆。可是细胞不会说话,科学家是怎么知道它们能尝出辣来呢?幸好,有钙成像这项强大的技术。钙成像技术是指利用钙离子指示剂(如Fura2等)监测细胞内钙离子浓度的方法,允许细胞使用荧光强度作为自己的语言。有了这项技术,原本悄无声息的离子浓度变化就变成了一幅可视影像。
经过两三年对实验技术的艰难摸索,Caterina和Julius惊喜地发现,加入辣椒素后,一盘原本在显微镜视野里毫无波澜的细胞开始闪烁,像黑夜里的星星一般散发出迷人的光芒(图6,A)。这正是上面所提到的TRP蛋白家族的一员——TRPV1蛋白的功劳 [9]:辣椒素与V1受体(当时被叫做V1)结合,打开离子通道,引起钙离子胞内浓度的迅速增加。Caterina和Julius还发现,TRPV1通道也能被高温激活而开放,其激活阈值为~40°C,接近热痛的心理物理阈值。此外,为了证明TRPV1蛋白自身可被热刺激激活,Julius实验室将纯化后的TRPV1蛋白重构于人工脂质体上,发现其仍然具有温度感受功能 [10]。于是,TRPV1的发现完美解释了为何吃辣椒总是感到热的现象。至此,一个由好奇心驱动的研究,意外揭开了TRP蛋白在哺乳动物中功能的神秘面纱。
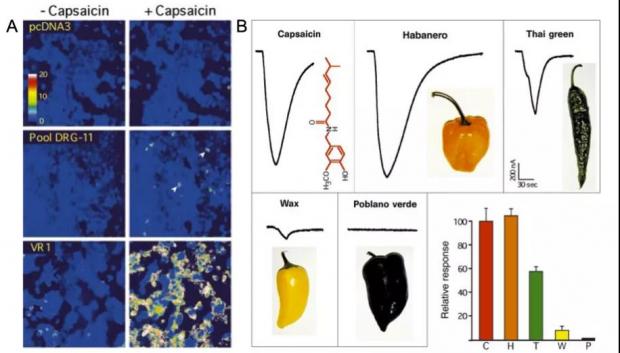
图6 辣椒素受体TRPV1的发现 [9] 注:A,用cDNA克隆库转染的HEK293细胞。在DRG-11池中,一些细胞对辣椒素有反应。经过反复试验,鉴定了一个对应于TPRV1(VR1)的克隆;B,表达VR1的卵母细胞对辣椒素(10 M)和四种辣椒提取物的反应
在生理意义上,作为唯一被辣椒素激活的受体—TRPV1,在转导辣椒素的伤害性、炎症和高热效应方面的重要作用,在小鼠中得到证实[10,51]。缺乏Trpv1 基因的动物仅表现出对急性伤害性热刺激的痛觉反应下降,并降低了对炎症性痛觉过敏(hyperalgesia)的热敏感性 [11]。不过,Trpv1 的缺乏并没有导致这些感觉完全消失,说明必然有其他热敏蛋白存在。科学家把目光转向其他TRP通道蛋白,最终在18年之后鉴定出TRPM3和TRPA1与TRPV1共同介导了伤害性热刺激的感受 [12-14]。
最初寻找辣椒素受体的时候,人们并没有想到它同时是感受热的受体,在这一关联建立之后,Julius实验室对被视作清凉剂的薄荷醇的受体克隆充满信心。果然,Julius实验室和此次另一位诺贝尔奖得主Ardem Patapoutian实验室在2002年分别独立发现了薄荷醇的受体TRPM8,并证明这个TRP通道是寒冷的感觉传感器 [15,16]。Trpm8 缺失会导致小鼠对无害寒冷感觉的明显缺失 [17-19]。这些研究说明在进化上TRP通道具有通用的温度感受作用,并在果蝇、线虫、蚊子、蛇等多种动物中得到了验证 [7,20]。
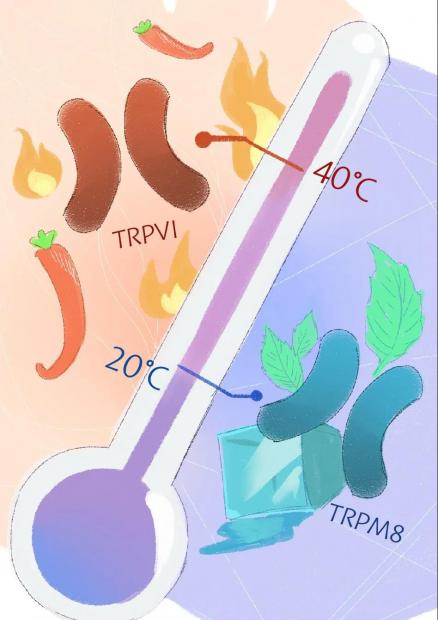
图7 热刺激与冷刺激感受器及对应的激动剂 | 褚刘薇
生物分子的结构对阐明结构与功能关系及药物开发至关重要,TRPV1结构的解析由Julius和程亦凡实验室在2013年合作通过冷冻电子显微镜解析 [21,22],是第一个通过冷冻电镜解析的膜蛋白结构。从冷冻电镜结果上看,TRPV1有两个控制离子通过的位点,在阳离子传导孔的两端形成两个突出的物理结构,辣椒素的结合位点位于靠近细胞质侧的膜深处的口袋。最近的一项结构研究表明,有害热量会在辣椒素结合的TRPV1 通道中产生两种构象门控转变:第一个过渡态为通道打开做好准备,而第二个过渡态导致通道打开 [23]。TRPV1通道的结构研究提供了对其离子渗透、配体识别和门控机制的重要见解,但尚未完全解释其热激活机制。
以TRPV1通道为代表的温度感受器的发现,不仅在基础生理理解上有突破性的意义,也为开发新型镇痛药物提供了靶点。除了作为疼痛感受器,TRP通道也在呼吸系统和心血管系统疾病如哮喘、心衰等方面发挥关键作用,在前列腺癌等多种癌症以及中风、皮肤病等多种疾病中被报道有所参与。目前靶向TRPV1和TRPM8等离子通道蛋白的镇痛小分子化合物,已有多个在进行临床试验 [24]。国内科学家浙江大学杨巍、郭江涛、杨帆,南昌大学张进等在TRP通道的结构研究和药物研发上取得很多成果 [25-31]。
2 失去触觉的细胞
如前所述,Ardem Patapoutian 作为寒冷感受器TRPM8的共同发现者,活跃在感觉受体研究领域。值得一提的是,这位出生于黎巴嫩的亚美尼亚裔美国神经科学家,经历比Julius坎坷许多。他在战火的阴影下生活了19年后,于1986年移居美国,辗转之后于1990年获得加州大学洛杉矶分校细胞与发育生物学学士学位,就此开启了他此前未敢想象的科学家生涯。他不满足仅仅是跟踪者的角色,决定挑战更加复杂的人类的机械力感受机制。
机械力感受无处不在。路人的摩肩接踵,来自朋友的拥抱,恋人之间的肌肤相亲,父母落在孩童额上的吻…… 新冠疫情期间的隔离,让很多人意识到这些原本司空见惯的来自他人的 “机械力” 弥足珍贵;当我们困在钢筋森林,拂面的清风,滴落在手心的雨点,粗糙的树干和娇嫩的花瓣,大自然给予我们的 “机械力” 也变得令人想念。然而,感知机械力对我们的重要性远远不止这些。我们身体也在每时每刻给予自己机械力——站立、行走、排尿、血压、呼吸、细胞分化运动等等生理活动都与机械力感受密不可分,这也就意味着体内几乎所有细胞都有一定程度的感受机械力的能力。因此,很难找到一种原本对触觉毫无响应的细胞,发现TRPV1的那套方法也就很可能行不通。对机械力感知受体的探索无疑是困难的,Patapoutian将其称为 “房间里的大象”,重要却无人敢碰。
面对这个艰巨的任务,Patapoutian与其博士后 Bertrand Coste 勇敢地做出了自己的尝试,他们从一种小鼠神经瘤母细胞(N2A)入手。当被移液管用极微小的力轻戳时,这种细胞会释放一个可测量的电流。然后,Coste和Patapoutian依次敲除300多个候选基因,通过观察哪批细胞突然失去了机械力敏感性,确定相关基因。经过长时间不懈努力,最终确定清单上的72号候选基因具此功能(图8)。他们把这个基因取名为Piezo1 ——在希腊语里是压力的意思。由于与Piezo1 基因的相似性,课题组发现的第二个基因被命名为Piezo2 [32]。随后,Coste和另外一个博士后肖百龙(现在清华大学任职)通过单通道膜片钳证明这两个蛋白的确是机械力敏感的离子通道 [33]。
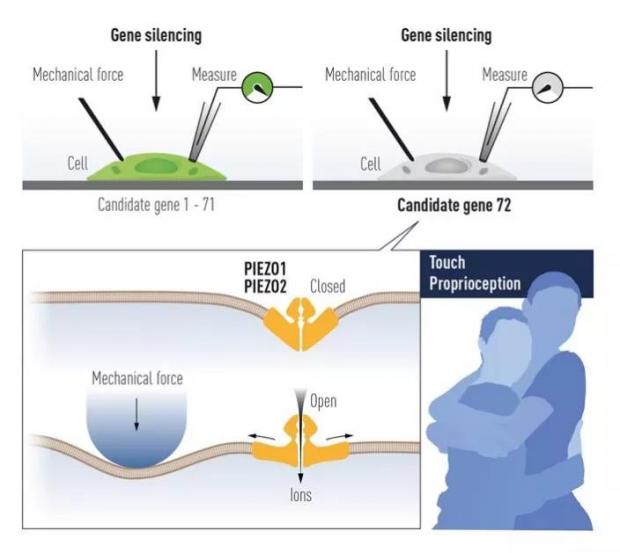
图8 通过在机械敏感细胞系中敲除候选基因来寻找机械感受受体| 图源: 注:上图,当敲除的基因为机械感受受体时,机械力敏感的细胞将不会再产生电流;下图,PIEZO通道蛋白结构示意图。
PIEZO蛋白代表了一类全新的脊椎动物机械敏感通道,与之前已知的离子通道家族没有任何相似之处。它们是迄今为止鉴定出的最大的跨膜离子通道亚基。肖百龙、Patapoutian、杨茂君、李雪明、Roderick MacKinnon等实验室的工作揭示了PIEZO1和PIEZO2的高分辨率结构,并表明这些通道形成具有中心离子传导孔和三个外围大型机械传感螺旋桨形叶片的同三聚体结构 [34,35],当对膜施加机械力时,弯曲的叶片变平并导致中心孔的开口,带有弯曲叶片的螺旋桨状结构产生较大的平面内膜面积膨胀,从而感知到精细机械力 [36,37]。
然而,机械力打开中心孔的确切机制仍未完全了解。目前已经知道的是,通过其机械敏感性,PIEZO通道在许多细胞类型中充当多功能机械传感器,并将机械力转换为电化学信号。Patapoutian很快确认了PIEZOs为哺乳动物体内压力感应的必需基因。他的研究表明,PIEZOs可形成离子通道,它们直接负责皮肤内默克尔细胞(Merkel cells)和触觉终端,以及本体感受器(感觉神经末梢位于肌肉内的感受器,可以感受身体在空间的位置、姿势和运动并做出反应)的压力感测 [38,39](图9)。PIEZOs还能通过分布在血管和肺部的神经末梢感知压力 [40],并影响红细胞体积、血管生理 [41-43],引发多种人类遗传疾病。PIEZOs的发现打开了力学生物学的大门,这是一个与生物学、工程学和物理学交叉的新兴科学领域,侧重于研究细胞和组织的物理作用力和力学特性的变化如何对健康和疾病造成影响。
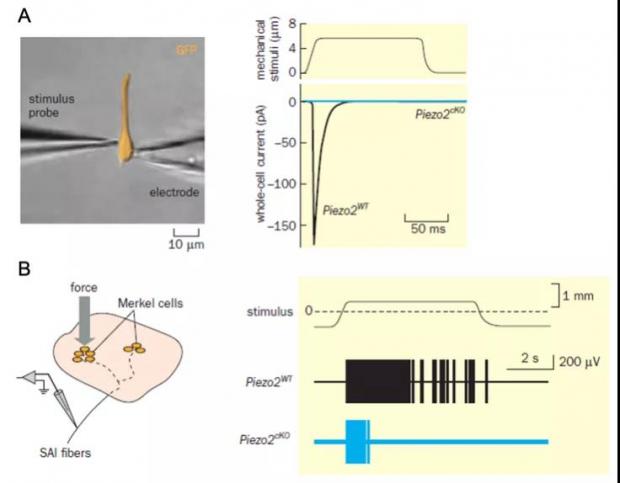
图9 默克尔细胞和感觉神经元中的机械力转导 [38-44]
注:A,左,实验图示。对一个分离培养的GFP标记的默克尔细胞进行全细胞膜片钳记录,同时用玻璃探针施加机械刺激。右,当Piezo2被在默克尔细胞中条件性敲除时,内向电流消失(蓝线);B,左,皮肤-神经连接示意图。用玻璃电极刺激荧光标记的默克尔细胞,同时记录来自与之相连的SA I纤维的动作电位。右,机械刺激又刺激探针到皮肤的距离来衡量。在0处(虚线),探针刚碰到皮肤;大于0时,探针使皮肤下陷。Piezo2被在默克尔细胞中条件性敲除后,SA I纤维不再持续发放。
结 语
Patapoutian在采访里说,“正因为人们太视本体感觉为理所当然了,所以导致如此重要的问题近一二十年才被解答。” 然而一旦PIEZO2发生突变,其重要性就难以被忽视。PIEZO2缺乏综合征患者的本体感觉、触觉和振动显著减弱。这会导致感觉性共济失调、测距障碍、步态困难、肌肉无力和萎缩、脊柱侧弯、髋关节发育不良和进行性骨骼挛缩。这些患者还存在肺部内感受缺陷导致围产期呼吸窘迫和膀胱导致排尿障碍 [45]。PIEZO1的突变则会损害红细胞的生理功能和淋巴系统的发育 [46-50]。

图10 温度和触觉受体(褚刘薇)
如Julius在诺奖公布后的采访中所说:“感觉系统是伟大的,正是有了它,我们才能感知到我们所生活的世界的一切。”温度和触觉受体的发现,是继视觉、嗅觉、味觉、听觉之后人类与客观世界又一次激动人心的握手。我们的身体正通过小小的受体蛋白努力感知着我们所生活的世界的一切,我们怎么能视周遭的一切为理所当然,让点滴微妙但珍贵的生命体验白白流逝呢?
- 致 谢 -
感谢浙江大学王立铭、清华大学肖百龙、加州大学旧金山分校张凯华、以及上海科技大学王绛、高瑄、吴松辉和李秋凝等在写作过程中提供的指导和帮助。感谢上海科技大学综合办公室、科技处与生命科学与技术学院的支持。
参考视频:
参考文献:
1.Cosens, D.J. & Manning, A. Abnormal electroretinogram from a Drosophila mutant. Nature 224, 285-287 (1969).
2.Minke, B., Wu, C. & Pak, W.L. Induction of photoreceptor voltage noise in the dark in Drosophila mutant. Nature 258, 84-87 (1975).
3.Spradling, A.C. & Rubin, G.M. Transposition of cloned P elements into Drosophila germ line chromosomes. Science 218, 341-347 (1982).
4.Rubin, G.M. & Spradling, A.C. Genetic transformation of Drosophila with transposable element vectors. Science 218, 348-353 (1982).
5.Montell, C., Jones, K., Hafen, E. & Rubin, G. Rescue of the Drosophila phototransduction mutation trp by germline transformation. Science 230, 1040-1043 (1985).
6.Montell, C. & Rubin, G.M. Molecular characterization of the Drosophila trp locus: a putative integral membrane protein required for phototransduction. Neuron 2, 1313-1323 (1989).
7.Venkatachalam, K. & Montell, C. TRP channels. Annu Rev Biochem 76, 387-417 (2007).
8.Julius, D., MacDermott, A.B., Axel, R. & Jessell, T.M. Molecular characterization of a functional cDNA encoding the serotonin 1c receptor. Science 241, 558-564 (1988).
9.Caterina, M.J., et al. The capsaicin receptor: a heat-activated ion channel in the pain pathway. Nature 389, 816-824 (1997).
10.Cao, E., Cordero-Morales, J.F., Liu, B., Qin, F. & Julius, D. TRPV1 channels are intrinsically heat sensitive and negatively regulated by phosphoinositide lipids. Neuron 77, 667-679 (2013).
11.Caterina, M.J., et al. Impaired nociception and pain sensation in mice lacking the capsaicin receptor. Science 288, 306-313 (2000).
12.Vriens, J., et al. TRPM3 is a nociceptor channel involved in the detection of noxious heat. Neuron 70, 482-494 (2011).
13.Bandell, M., et al. Noxious cold ion channel TRPA1 is activated by pungent compounds and bradykinin. Neuron 41, 849-857 (2004).
14.Jordt, S.E., et al. Mustard oils and cannabinoids excite sensory nerve fibres through the TRP channel ANKTM1. Nature 427, 260-265 (2004).
15.McKemy, D.D., Neuhausser, W.M. & Julius, D. Identification of a cold receptor reveals a general role for TRP channels in thermosensation. Nature 416, 52-58 (2002).
16.Peier, A.M., et al. A TRP channel that senses cold stimuli and menthol. Cell 108, 705-715 (2002).
17.Bautista, D.M., et al. The menthol receptor TRPM8 is the principal detector of environmental cold. Nature 448, 204-208 (2007).
18.Colburn, R.W., et al. Attenuated cold sensitivity in TRPM8 null mice. Neuron 54, 379-386 (2007).
19.Dhaka, A., et al. TRPM8 is required for cold sensation in mice. Neuron 54, 371-378 (2007).
, H. & Siemens, J. TRP ion channels in thermosensation, thermoregulation and metabolism. Temperature (Austin) 2, 178-187 (2015).
21.Cao, E., Liao, M., Cheng, Y. & Julius, D. TRPV1 structures in distinct conformations reveal activation mechanisms. Nature 504, 113-118 (2013).
22.Liao, M., Cao, E., Julius, D. & Cheng, Y. Structure of the TRPV1 ion channel determined by electron cryo-microscopy. Nature 504, 107-112 (2013).
23.Kwon, D.H., et al. Heat-dependent opening of TRPV1 in the presence of capsaicin. Nat Struct Mol Biol 28, 554-563 (2021).
24.Moran, M.M., McAlexander, M.A., Biro, T. & Szallasi, A. Transient receptor potential channels as therapeutic targets. Nat Rev Drug Discov 10, 601-620 (2011).
25.Yu, P., et al. Direct Gating of the TRPM2 Channel by cADPR via Specific Interactions with the ADPR Binding Pocket. Cell Rep 27, 3684-3695 e3684 (2019).
26.Yu, P., et al. Identification of the ADPR binding pocket in the NUDT9 homology domain of TRPM2. J Gen Physiol 149, 219-235 (2017).
27.Guo, J., et al. Structures of the calcium-activated, non-selective cation channel TRPM4. Nature 552, 205-209 (2017).
28.Yang, F., et al. Structural mechanism underlying capsaicin binding and activation of the TRPV1 ion channel. Nat Chem Biol 11, 518-524 (2015).
29.Xu, L., et al. Molecular mechanisms underlying menthol binding and activation of TRPM8 ion channel. Nat Commun 11, 3790 (2020).
30.Xu, L., et al. De Novo Design of Peptidic Positive Allosteric Modulators Targeting TRPV1 with Analgesic Effects. Adv Sci (Weinh) 8, e2101716 (2021).
31.Duan, J., et al. Structure of the mouse TRPC4 ion channel. Nat Commun 9, 3102 (2018).
32.Coste, B., et al. Piezo1 and Piezo2 are essential components of distinct mechanically activated cation channels. Science 330, 55-60 (2010).
33.Coste, B., et al. Piezo proteins are pore-forming subunits of mechanically activated channels. Nature 483, 176-181 (2012).
, J., et al. Architecture of the mammalian mechanosensitive Piezo1 channel. Nature 527, 64-69 (2015).
35.Zhao, Q., et al. Structure and mechanogating mechanism of the Piezo1 channel. Nature 554, 487-492 (2018).
, L., et al. Structure and mechanogating of the mammalian tactile channel PIEZO2. Nature 573, 225-229 (2019).
37.Jiang, Y., Yang, X., Jiang, J. & Xiao, B. Structural Designs and Mechanogating Mechanisms of the Mechanosensitive Piezo Channels. Trends Biochem Sci 46, 472-488 (2021).
38.Maksimovic, S., et al. Epidermal Merkel cells are mechanosensory cells that tune mammalian touch receptors. Nature 509, 617-621 (2014).
39.Ranade, S.S., et al. Piezo2 is the major transducer of mechanical forces for touch sensation in mice. Nature 516, 121-125 (2014).
40.Nonomura, K., et al. Piezo2 senses airway stretch and mediates lung inflation-induced apnoea. Nature 541, 176-181 (2017).
41.Min, S., et al. Arterial Baroreceptors Sense Blood Pressure through Decorated Aortic Claws. Cell Rep 29, 2192-2201 e2193 (2019).
42.Zeng, W.Z., et al. PIEZOs mediate neuronal sensing of blood pressure and the baroreceptor reflex. Science 362, 464-467 (2018).
43.Rode, B., et al. Piezo1 channels sense whole body physical activity to reset cardiovascular homeostasis and enhance performance. Nat Commun 8, 350 (2017).
44.Woo, S.H., et al. Piezo2 is required for Merkel-cell mechanotransduction. Nature 509, 622-626 (2014).
45.Marshall, K.L., et al. PIEZO2 in sensory neurons and urothelial cells coordinates urination. Nature 588, 290-295 (2020).
46.Fotiou, E., et al. Novel mutations in PIEZO1 cause an autosomal recessive generalized lymphatic dysplasia with non-immune hydrops fetalis. Nat Commun 6, 8085 (2015).
47.Lukacs, V., et al. Impaired PIEZO1 function in patients with a novel autosomal recessive congenital lymphatic dysplasia. Nat Commun 6, 8329 (2015).
48.Albuisson, J., et al. Dehydrated hereditary stomatocytosis linked to gain-of-function mutations in mechanically activated PIEZO1 ion channels. Nat Commun 4, 1884 (2013).
49.Andolfo, I., et al. Multiple clinical forms of dehydrated hereditary stomatocytosis arise from mutations in PIEZO1. Blood 121, 3925-3935, S3921-3912 (2013).
50.Zarychanski, R., et al. Mutations in the mechanotransduction protein PIEZO1 are associated with hereditary xerocytosis. Blood 120, 1908-1915 (2012).
51.Davis, John B., et al. "Vanilloid receptor-1 is essential for inflammatory thermal hyperalgesia." Nature 405.6783 (2000): 183-187.
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 