
老人及基础病人群能否打新冠灭活疫苗?| 图源:
知识分子编者按:
香港地区奥密克戎疫情的相关研究揭示,没有接种过疫苗或者未完成全程免疫接种的老年人群,是感染新冠后重症和死亡风险最高的人群。新西兰的经验也证实,在最高危人群当中实现新冠疫苗的全面接种可以大大降低了感染新冠的重症和死亡风险。
然而,由于对疫苗在老年人和慢性病人群中安全性和有效性,特别是安全性有所顾虑,我国现阶段特殊人群的疫苗覆盖率远低于全人口疫苗接种率。
2022年5月2日,本文作者团队在预印本网站发表了论文《新冠灭活疫情在基础疾病人群中的免疫原性和安全性回溯研究》[17],分析了约1000名包含6种基础疾病受试者在接种新冠灭活疫苗后的保护效力和安全性数据。本文通过综述国内外多项针对特殊人群接种新冠疫苗的真实数据研究,旨在通过科学数据打消特殊人群接种疫苗的顾虑,帮助提升疫苗犹豫人群接种疫苗信心,尽快提高我国高年龄段和高风险人群的疫苗接种率。
撰文 | 李春梅 张子杰
责编 | 刘楚
新冠疫情仍在全球肆虐,特别是奥密克戎变种的出现以极高的传播率席卷全球。当前,接种疫苗仍然是全球主要经济体用来控制新冠疫情所带来的消极影响的一个主要手段。
前期各国已通过大量的临床试验证明了疫苗预防感染、重症及死亡的效用 [1-6]。由于疫苗诱导的新冠中和抗体随时间逐渐减退以及新冠变异株的免疫逃逸不断加强,各国也相继推出了加强针策略进一步提高群体免疫屏障 [7,8]。
截至2022年3月17日,我国已实现超过87.6%人口的全程接种率,此外还有相当大量的人群已接种第三针加强针,疫苗接种率在全球主要经济体中处于前列。
然而我国有超过2.6亿60岁以上的老年人群,他们中相当部分还合并了各种各样的慢性基础疾病。
一方面由于对疫苗在老年人和慢性病人群中安全性和有效性,特别是安全性有所顾虑;另一方面我国前期在疫情防控方面做得较好,受病毒感染的几率很小,接种动力不足。这样一个背景下,我国当前老年人群接种疫苗的覆盖率非常低,截至2022年3月,全程接种率不足40%。
当前,在疫情传播的威胁下,这部分没有接种疫苗的特殊人群构成了一个巨大的免疫屏障漏洞。
1、特殊人群接种新冠疫苗的必要性
近期在我国吉林、上海以及香港等地暴发的局部疫情又一次给我们敲响了警钟,新冠疫苗在老年人群中接种的重要性不言而喻。
香港针对近期感染的死亡病例公布了详细数据及分析,该数据显示死亡病例中,92%是合并基础疾病人群、95%是60岁以上老年人;并且一个重要的特点是大部分是没有接种过疫苗或者只接种过一剂疫苗,没有完成免疫程序 [9]。这部分人群构成了在新冠传播流行时感染后重症和死亡风险最高的人群,特别是70-79岁、80岁以上的人群中,如果没有接种新冠疫苗,其死亡风险比起已接种疫苗的人群高了10倍左右(图1)。
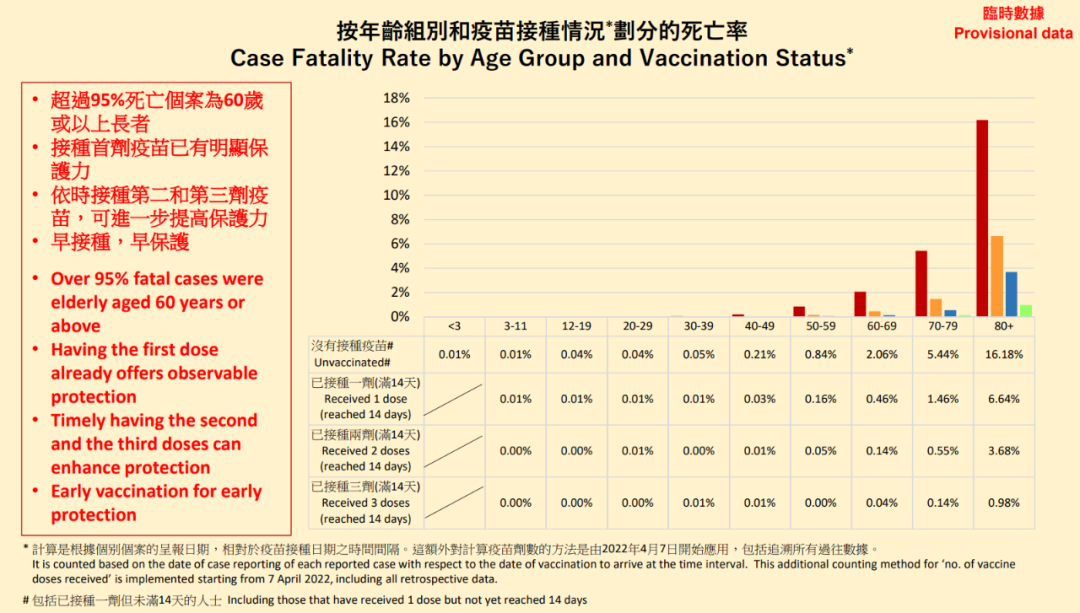
图1 香港关于新冠感染死亡人群分析 | 文献[9]
另一方面,我们也能从全世界新冠病死率最低的国家总结一些经验。新西兰新冠总病死率仅0.03%,相较于全球病死率1.32%低了很多。其中一个重要的经验是新西兰75岁以上老年人(风险最高的人群)新冠疫苗接种率是100% [10]。在最高危人群当中实现了新冠疫苗的全面接种很大程度上降低了该人群在感染时候的重症和死亡风险。
综上,在我国推动60岁以上及合并基础病人群中的新冠疫苗接种,对于降低感染时的重症和病死率,减缓疫情暴发对我国社会的冲击将会起到至关重要的作用。
充分开展老年人及合并基础疾病等特殊人群中的新冠疫苗应用安全性和有效性研究,充分宣传特殊人群疫苗应用研究结果,通过科学数据打消特殊人群接种疫苗的顾虑是提高特殊人群接种率的关键。
2、新冠灭活疫苗应用于慢病人群的安全性和免疫原性研究
为此,云南生物资源保护与利用国家重点实验室前期和海南省疾病预防控制中心合作,围绕我国社会常见的6类基础疾病人群进行了免疫原性(保护效果)研究和安全性回溯[17]。本研究关注的基础病包括高血压、糖尿病、冠心病、慢性呼吸系统疾病、癌症以及肥胖。
研究筛选了按照标准免疫程序接种了两剂科兴灭活疫苗的健康对照和基础病人群,在完成第二剂接种后的14-28天范围招募志愿者进行血样采集,检测他们体内的新冠中和抗体;同时访问调查他们在每剂接种后14天内出现的不良反应事件。
此外,研究还分别在完成免疫接种后3个月、6个月对志愿者进行了血清中和抗体检测,由此来评估合并基础病人群相对健康人群接种新冠疫苗的安全性、有效性和免疫持久性(图2)。
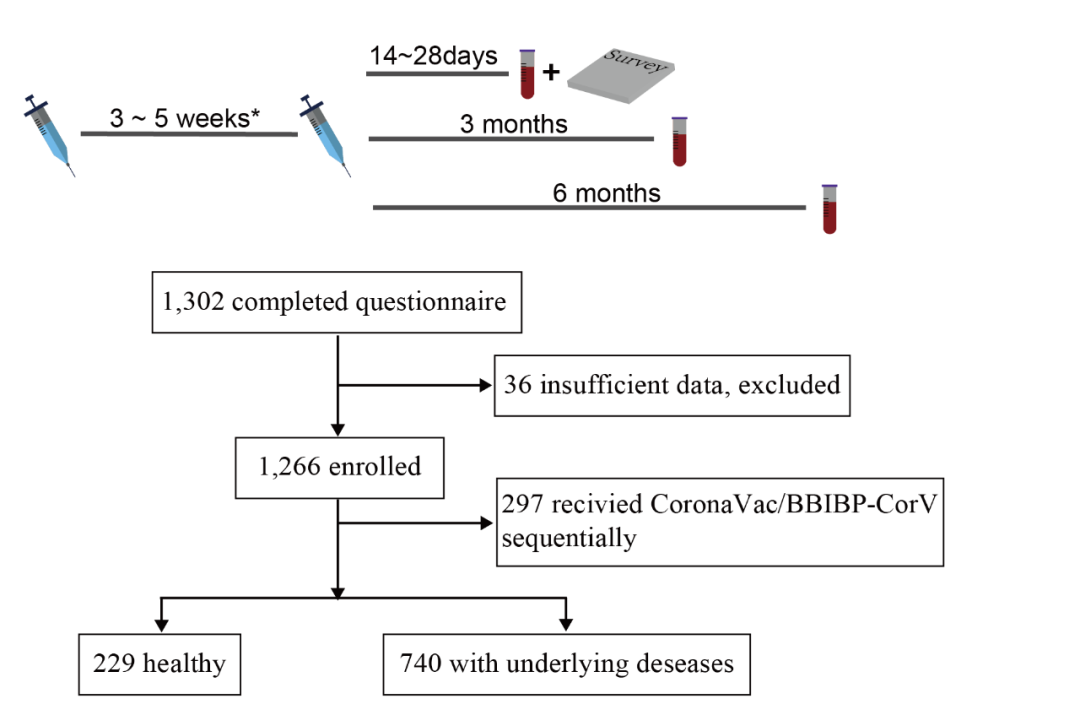
图2 研究流程示意图|文献[17]
在年龄段上,该研究分为了60岁及以上的老年人群,以及40-59岁的成年人群两个亚组。这两个年龄段是合并慢性基础病最多的人群,尤其60岁以上的人群是我国接种覆盖率较低的人群,需重点关注(图3)。
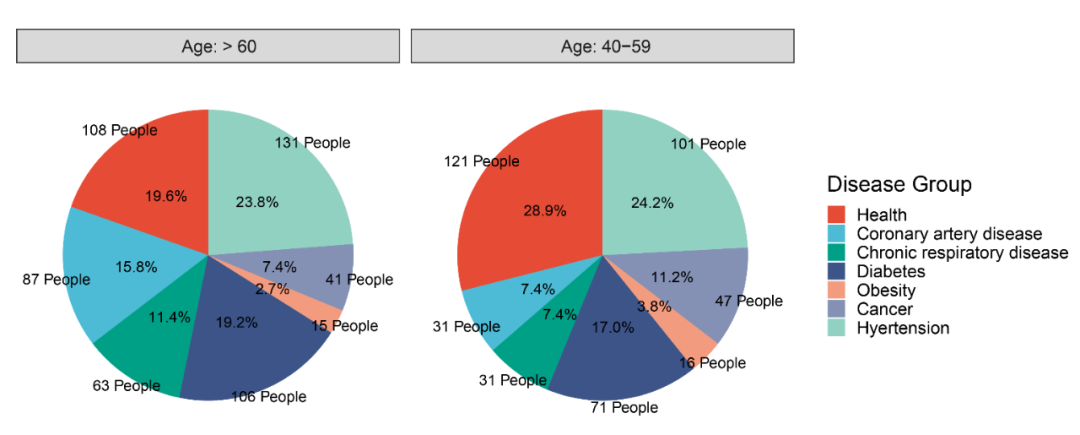
图3 入组人数概要|文献[17]
首先需要关注的是有效性的数据,本次研究采用了新冠抗体检测最高标准真病毒(原型株)攻毒实验检测。前期已有大量研究指出新冠中和抗体水平和临床保护率高度关联 [11],因此抗体水平高低可作为临床保护效果的替代评价标准。
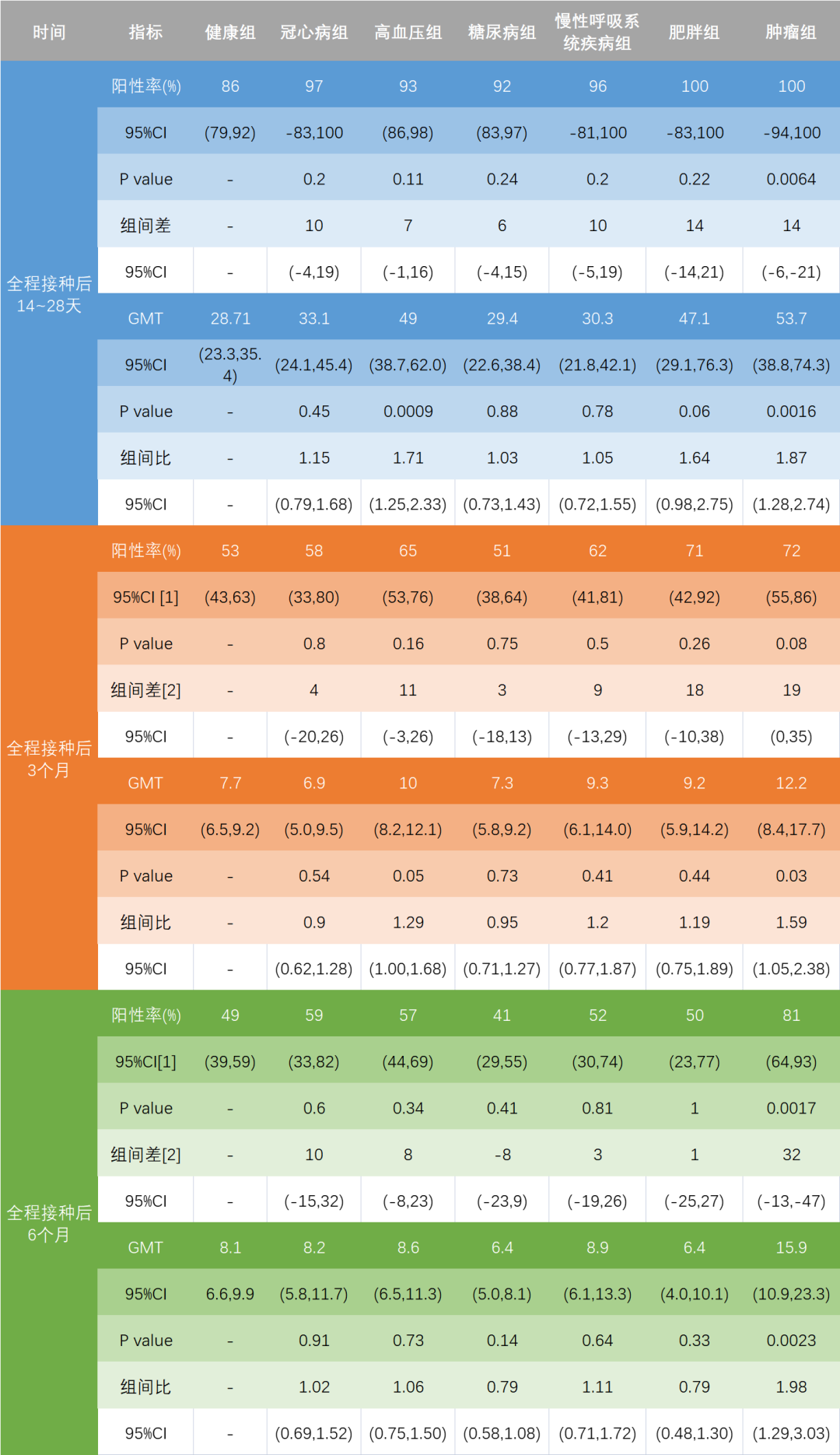
通过检测志愿者体内的中和抗体数据显示,在完成全程免疫后(14-28天),血清里中和抗体在大部分慢性病人群中和健康人群相当,仅60岁以上冠心病、慢性呼吸系统疾病人和肿瘤病人中观察到相较于健康人群的显著降低;阳性率降幅为12-22%,几何平均滴度降幅约40%(表1)。
在40-59岁年龄段,高血压和肿瘤患者抗体应答较健康对照显著上升(表2)。3个月和6个月后,健康和基础病人群抗体水平均大幅下降,提示抗体水平随时间有较快衰减。但3和6个月后,除了高血压和肿瘤患者仍然比健康人群高之外,疾病组和健康组抗体水平不再有差异(表2)。
表1 老年人组(≥60岁)受试者中和抗体分析(点击查看大图)
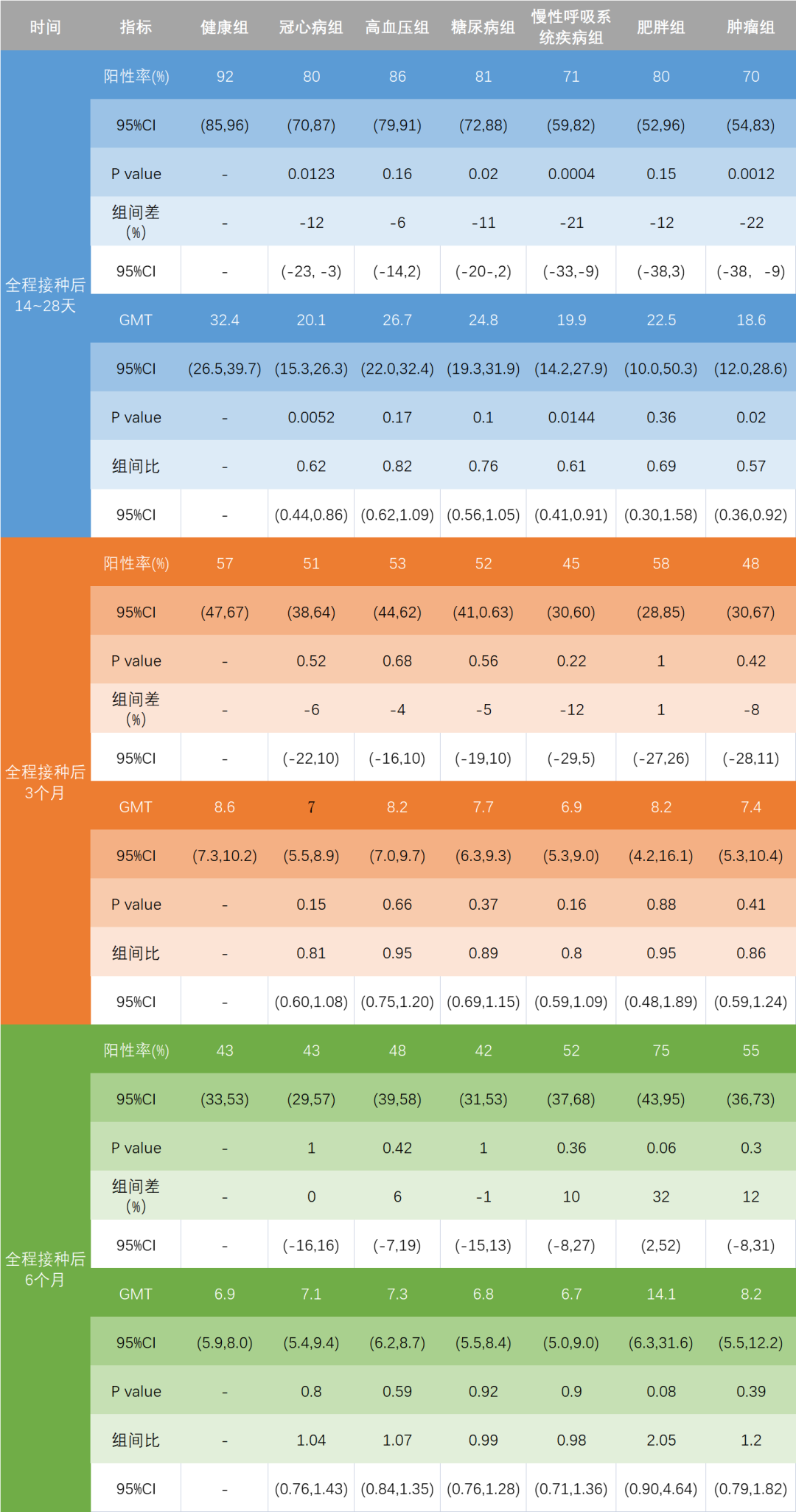
表2 成年人组(40~59岁)受试者中和抗体分析(点击查看大图)
综上,抗体应答水平仅在患有部分基础疾病60岁以上老人中观察到统计学显著的下降,但其中大部分仍然显示抗体阳性(可测)且能达到一定的水平(图4)。
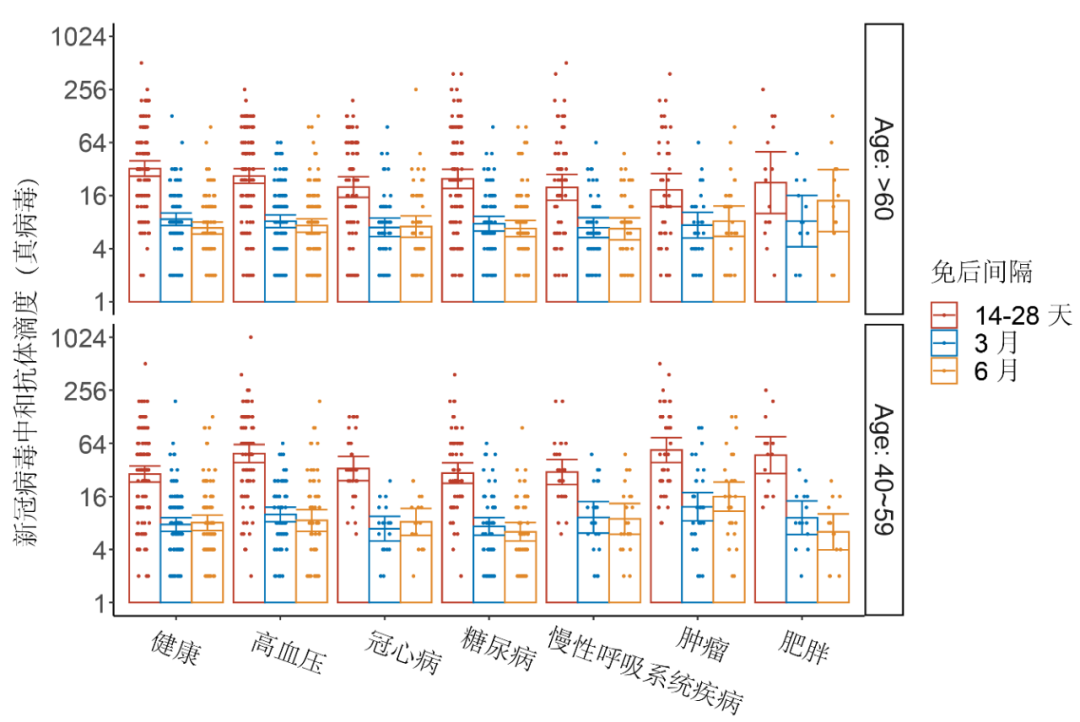
图4 6种基础疾病人群接种灭活疫苗后新冠病毒中和抗体滴度分布|文献[17]
此外,研究还通过回溯性(问卷)调查统计了受试者在完成每一剂疫苗接种后1-14天时间内所出现的不良反应事件,通过不良事件(及严重不良事件)发生率的统计来评估接种疫苗的安全性。
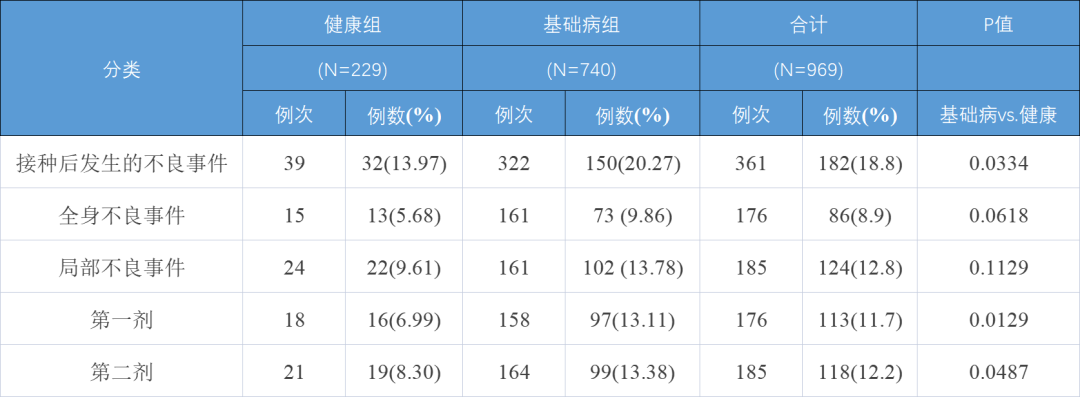
本次研究主要统计了17种与疫苗接种相关的常见不良反应,包括:接种部位疼痛等局部不良反应和疲劳乏力、发热等全身性不良反应。表3中显示,合并基础疾病人群接种疫苗总体不良事(统计学)显著高于健康人群,异幅度约为6%。
表格3 总体不良事件统计(点击查看大图)
然而,如果比较这些显著不良反应的分布会发现,不良事件主要集中在接种部位疼痛和疲劳乏力这两类症状。第1剂和第2剂相当,60岁以上老年人不良事件少于40-59岁成年人。
具体而言,不良事件大多是1级(短时或轻微不适,不影响活动,无需治疗)或2级(轻度或中度活动首先,可能需要就诊、不需要或仅需轻度治疗)不良反应(图5)。
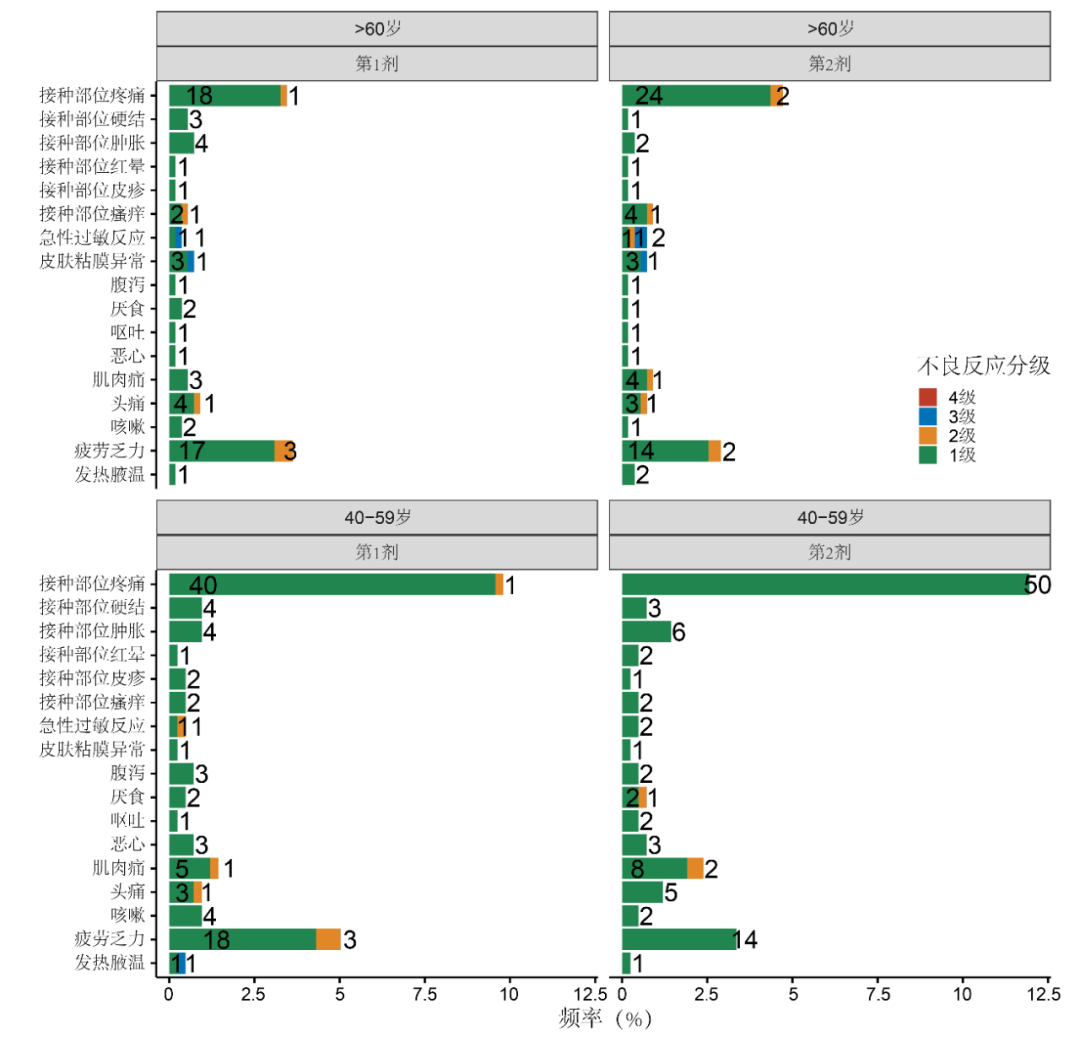
图5 不良事件在不同剂次、年龄段的分布,图中数字为例次|文献[17]
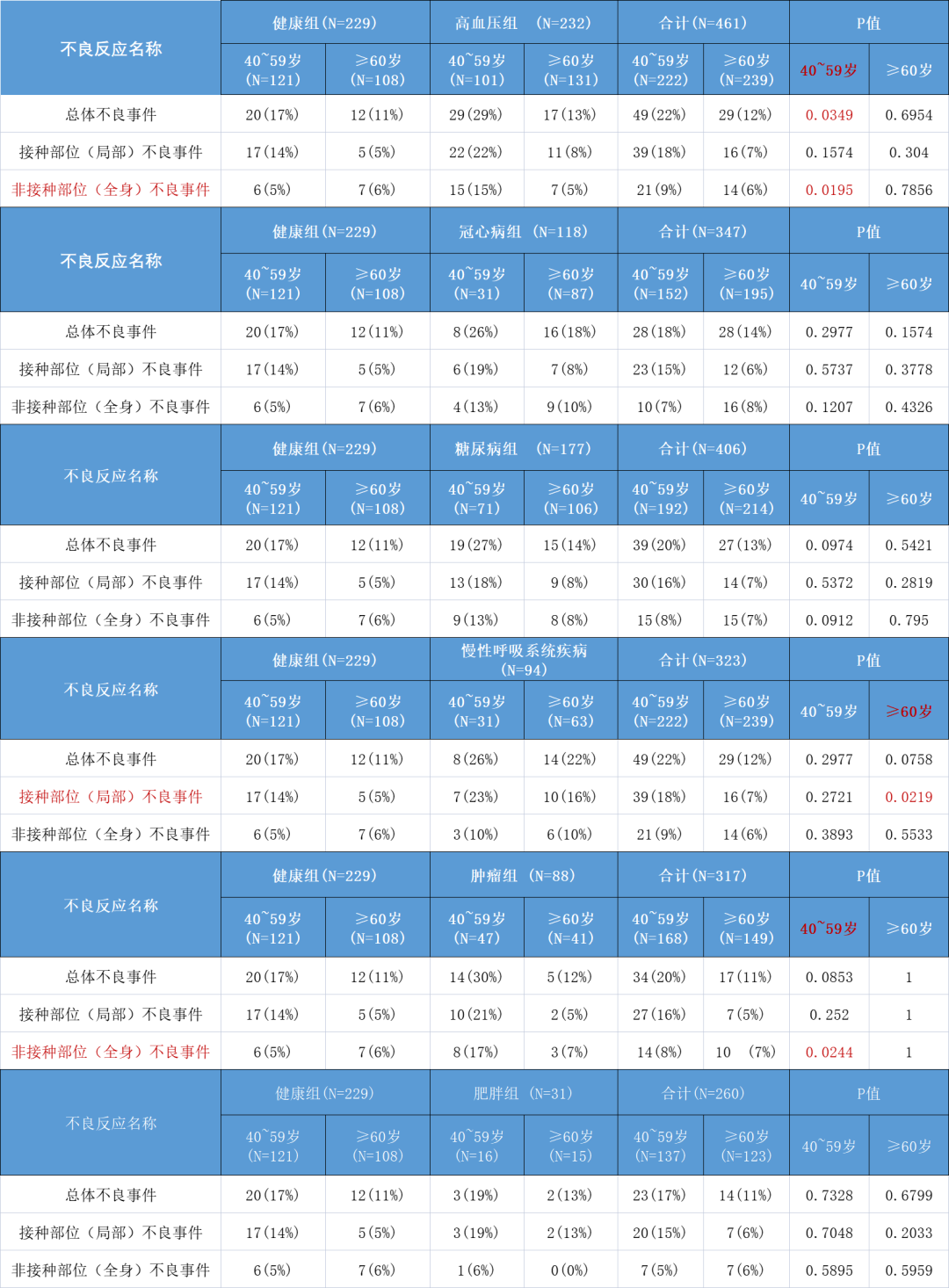
研究还单独分析每一种基础病人群和健康人群的不良事件发生率是否有统计学显著的差别(表4)。在6类基础病当中,40-59岁高血压和肿瘤患者非接种部位(全身)不良事件发生率显著高于健康人群(表中用红色标注)。进一步分析发现,主要是 “疲劳乏力” 这一症状在高血压和肿瘤患者中出现频次较高,主导了这两类病人和健康人群的差异(图6)。
表格4 各疾病组不良事件对比(点击查看大图)
在60岁以上的老年人中,仅有慢性呼吸系统疾病人群接种部位(局部)不良事件显著高于健康对照,进一步分析各类具体不良反应发现,“接种部位疼痛” 这一症状在慢性呼吸系统病人中更常出现导致了上述差异(图6)。
上述分析中主导基础疾病人群和健康人群差异的不良事件主要为接种部位疼痛和疲劳乏力症状,且主要为1级不良反应,在不需要干预的情况下可在1-2天内恢复。这两类症状均属于疫苗接种后的常见正常反应,对接种者健康没有附加的健康风险。
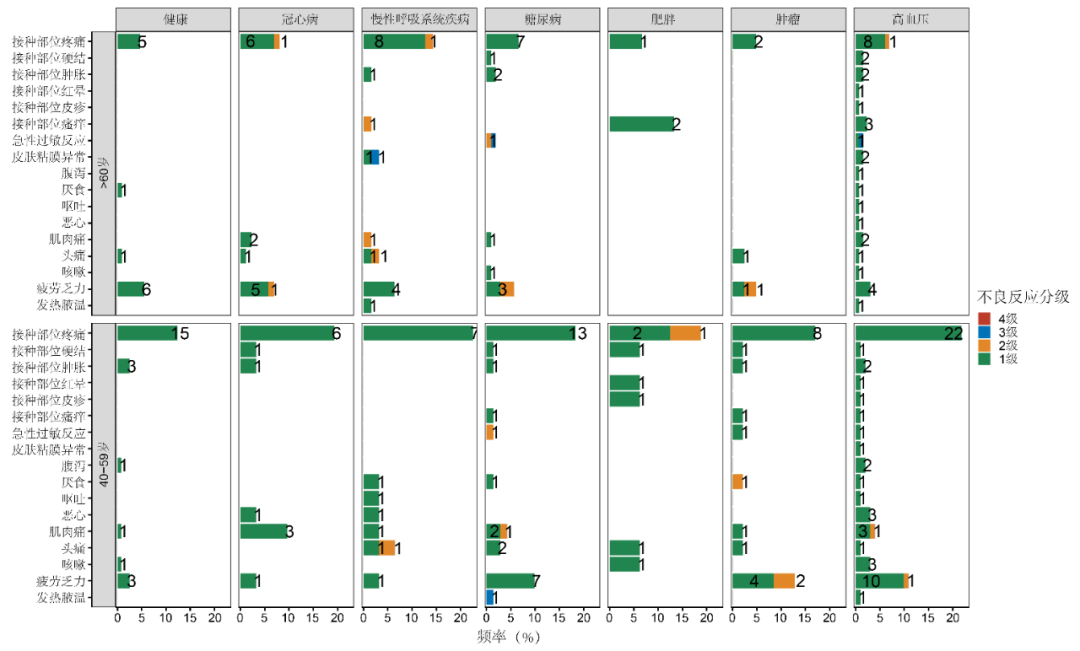
图6 不良事件在不同组别、年龄段的分布,图中数字为例次|文献[17]
综上所述,在研究纳入的6种基础疾病人群当中,大部分疾病和年龄亚组中基础病人群和健康人群不良反应发生率并无统计学差异。在个别与健康对照有统计学显著差异的亚组中,导致差异的症状均为无健康风险的常见疫苗后反应。
因此,在这些合并基础疾病的人群中,尤其是60岁以上的老年人当中,接种新冠灭活疫苗的安全性与健康人群无异。
在有效性方面,同样的大部分疾病及年龄亚组与健康对照没有显著差异,虽然也是在部分疾病的特定年龄段当中出现了统计学显著差异,但差异幅度不超过40%。因此总体来看,在合并基础疾病的人群当中,特别是60岁以上合并基础病人群中接种新冠疫苗和健康人群接种有效性也是相当的。
上述结论可以从有效性和安全性两个方面排除60岁以上老年人,特别是合并了基础疾病的老年人接种新冠疫苗的顾虑。再考虑到老年人和合并基础疾病人群感染新冠后较高的死亡和重症风险,权衡利弊,我们非常推荐老年人及合并基础疾病人群尽快完成新冠疫苗的接种。
只有这部分人群达到了较高的疫苗接种率,在我国或者其他地区发生新冠疫情局部暴发的时候才能最大程度抵御新冠感染带来的生命健康风险,减少疫情对社会的冲击。
3、新冠灭活疫苗在其他特殊人群应用的研究结果汇总
国际上一些其他接种新冠灭活疫苗的国家也开展了特殊人群接种新冠疫苗的安全性和有效性研究,我们在此介绍一些重要研究进展,便于帮助读者了解更多特殊人群接种疫苗的安全性和有效性。
科兴的灭活疫苗在巴西有大量的应用,一项巴西开展的孕产妇接种包括灭活疫苗在内的新冠疫苗的安全性研究统计了252430名接种了新冠灭活疫苗的孕产妇报告的不良事件 [12]。该研究数据显示,科兴灭活疫苗在各类参与研究的疫苗当中不良事件报告率最低,展现了在孕产妇群体中接种良好的安全性。
另一项对巴西约2万名孕妇的真实世界研究 [13] 显示,科兴灭活疫苗对新冠病毒有症状感染的保护率为41%,对于新冠重症的保护率为85%。
上述这两项研究提示,我国的新冠灭活疫苗在孕产妇中有较好的安全性和一定的有效性。
巴西一项HIV病毒的携带者的研究 [14] 比较了HIV阳性和HIV阴性人群接种新冠灭活疫苗的安全性。研究收集数据期间,HIV阳性人群与阴性对照报告的不良事件没有统计学差异,提示该人群接种新冠灭活疫苗有较好的安全性。
同样由巴西开展的另一项研究,对自身免疫性风湿性疾病患者使用新冠灭活疫苗的安全性进行了研究并报道在自免疫性风湿疾病患者中新冠灭活疫苗展现了较好的安全性;免疫原性方面,在自免疫性风湿病人较健康人群有所降低但仍在可接受范围 [15,16]。
最后,我们汇总了一些世界各地开展的研究进展(图7),发现在众多特殊人群当中,比如说孕产妇、器官移植病人、接受治疗当中的肿瘤患者、还有各类自身免疫相关的疾病当中接种新冠疫苗,特别是灭活疫苗,具有相当的安全性,和健康人群并没有显著的安全性差别。

图7 特殊人群新冠灭活疫苗安全性研究汇总 | 文献[12-16]
值得注意的是,在免疫应答方面,一部分疾病人群当中,接种新冠疫苗的抗体应答水平会有不同程度降低,因为其中相当部分的疾病涉及到免疫系统的紊乱,患者免疫应答能力低于健康人群。
但正因如此,这些免疫抑制特殊人群面对感染时也承受更高的重症和死亡风险;所以特殊人群研究的结论均为建议有健康状况的人群优先接种新冠疫苗,甚至是接种更多针剂的新冠疫苗以达到保护水平。
最后,希望通过上述在国内开展的我国常见慢病人群的研究数据的解析,以及世界各地特殊人群研究数据的回顾,帮助大家了解老年人以及合并基础疾病人群接种新冠疫苗的安全性,加强我国特殊人群接种疫苗的信心,尽快完成我国高年龄段和高风险人群的疫苗接种,提高我们社会应对疫情冲击的能力。
作者简介:
李春梅 助理研究员张子杰 研究员云南生物资源保护与利用国家重点实验室,云南大学
参考文献:
1.Baden LR, El Sahly HM, Essink B, et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. New England Journal of Medicine 2020; 384(5): 403-16.2.Hodgson SH, Mansatta K, Mallett G, Harris V, Emary KRW, Pollard AJ. What defines an efficacious COVID-19 vaccine? A review of the challenges assessing the clinical efficacy of vaccines against SARS-CoV-2. Lancet Infect Dis 2021; 21(2): e26-e35.3.Polack FP, Thomas SJ, Kitchin N, et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. New England Journal of Medicine 2020; 383(27): 2603-15.4.Tanriover MD, Doğanay HL, Akova M, et al. Efficacy and safety of an inactivated whole-virion SARS-CoV-2 vaccine (CoronaVac): interim results of a double-blind, randomised, placebo-controlled, phase 3 trial in Turkey. The Lancet 2021; 398(10296): 213-22.5.Voysey M, Clemens SAC, Madhi SA, et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. The Lancet 2021; 397(10269): 99-111.6.Zhang Y, Zeng G, Pan H, et al. Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine in healthy adults aged 18–59 years: a randomised, double-blind, placebo-controlled, phase 1/2 clinical trial. The Lancet Infectious Diseases 2021; 21(2): 181-92.7.Pan H, Wu Q, Zeng G, et al. Immunogenicity and safety of a third dose, and immune persistence of CoronaVac vaccine in healthy adults aged 18-59 years: interim results from a double-blind, randomized, placebo-controlled phase 2 clinical trial. medRxiv 2021: 2021.07.23.21261026.8.Zeng G, Wu Q, Pan H, et al. Immunogenicity and safety of a third dose of CoronaVac, and immune persistence of a two-dose schedule, in healthy adults: interim results from two single-centre, double-blind, randomised, placebo-controlled phase 2 clinical trials. The Lancet Infectious Diseases 2021.9. DS, Cromer D, Reynaldi A, et al. Neutralizing antibody levels are highly predictive of immune protection from symptomatic SARS-CoV-2 infection. Nature Medicine 2021; 27(7): 1205-11.12. AC, Aikawa NE, Saad CGS, et al. Immunogenicity and safety of the CoronaVac inactivated vaccine in patients with autoimmune rheumatic diseases: a phase 4 trial. Nature Medicine 2021; 27(10): 1744-51.16.Aikawa NE, Kupa LVK, Pasoto SG, et al. Immunogenicity and safety of two doses of the CoronaVac SARS-CoV-2 vaccine in SARS-CoV-2 seropositive and seronegative patients with autoimmune rheumatic diseases in Brazil: a subgroup analysis of a phase 4 prospective study. The Lancet Rheumatology 2022; 4(2): e113-e24.17.https://
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 