- 编者按 -
随着新冠肺炎的全球流行,无论是科研人员、医生、患者还是普通大众,对新冠肺炎的药物和疗法都产生了空前的关注。当人们逐渐接受没有 “特效药” 的存在,一个新的问题是,我们是否真的了解当前的新冠肺炎治疗处于什么程度?那些曾经受过关注的药物,还有多少值得期待抑或已被放弃,本文希望用循证的方式来展现人类为解决上述问题所做的努力。
全文分为四个部分:
1. 新冠肺炎16种疗法追踪表
2. 抗病毒药物篇
3. 症状缓解治疗
4. 中药篇
撰文 | 汤佩兰 计永胜 瑾言 思敏 李砺
审阅 | 许俊才 李浩然 商周 王宇歌
责编 | 汤佩兰 陈晓雪
在与新冠斗争的数月中,全球已有超过2400万感染者。虽然医生们努力救治患者,但仍有80多万人离世。在等待有效疫苗诞生之前,人们想知道:新冠肺炎有特效药了吗?现有的临床试验都找到了哪些可用的药物?
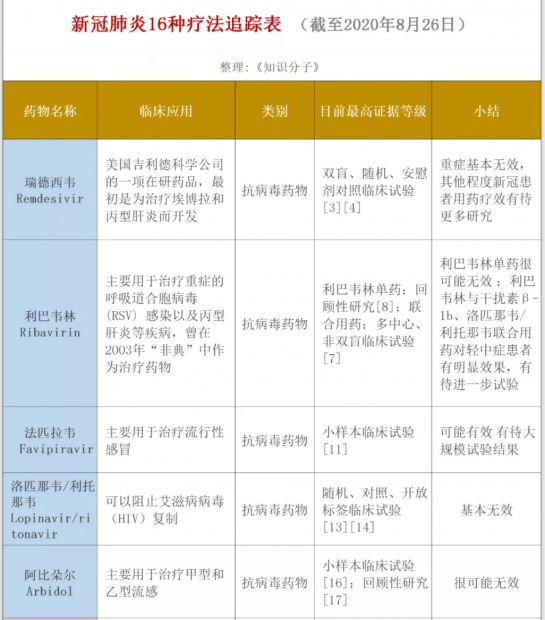
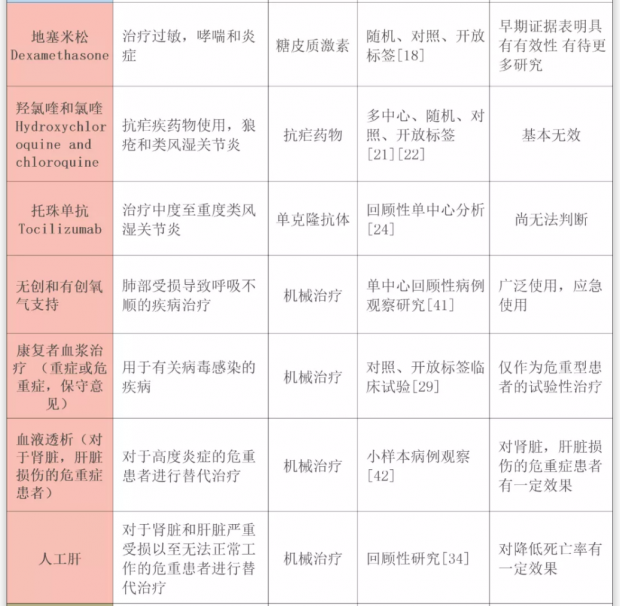
过去四周,《知识分子》和几位生物或医学领域的小伙伴,从媒体报道以及国内《新型冠状病毒感染的肺炎诊疗方案》中,梳理了当前的新冠治疗方法,通过现有的研究证据,对16种新冠病毒治疗的药物或疗法进行了追踪。
在回顾这些研究的过程中,我们发现疫情的动态变化本身有许多不可控的因素,对于新冠治疗的临床试验普遍存在试验设计不够严格、样本量小等问题。随着一些地区疫情的好转,一些临床试验无法招募到计划中足够的受试者,造成了样本量较小的问题。有的临床试验并不是随机双盲,也在一定程度上降低了结论的可信度。即便同为对照试验,不同研究对照的设计也各异。有的是两种不同的药物对照,有的是单一用药与联合用药的对照,有的是将支持治疗作为对照组。
需要说明的是,本文不是也无意于作为新冠治疗方法指南,而是便于公众对这场人类正在共同面对的、并深入改变我们现在和未来生活的疫情,能够有基于科学证据的、阶段性的了解。
为了阅读的便利,我们根据牛津大学循证医学中心的证据等级,将证据可靠性分为五个等级。证据的可靠性根据研究设计、方案实施的严谨性、统计方法的应用进行衡量,证据水平越高则证据的推荐级别越高。
本文尽可能将目前最高证据等级的研究作为参考,对每种疗法做了小结。如有不尽之处还请读者朋友指教。
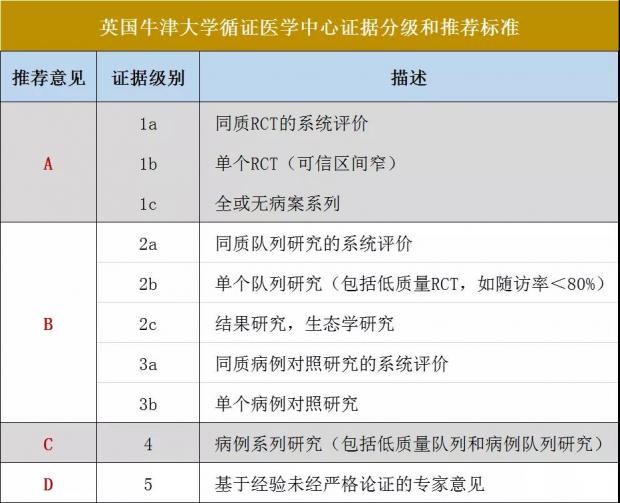
牛津大学循证医学中心证据分级。该标准根据证据的性质将证据分为A~D4个推荐级别。
全文共10542字
一图先带你了解报告概要
PART 01 抗病毒药物篇
瑞德西韦
小结:重症基本无效,其他程度新冠患者用药疗效有待更多研究
瑞德西韦(Remdesivir)是美国吉利德科学公司(Gilead Sciences)的一项在研抗病毒药物,尚未经美国FDA批准上市。
最初,瑞德西韦是为治疗埃博拉和丙型肝炎开发的,2019年的临床研究显示其治疗效果不佳 [2]。
2020年4月29日,《柳叶刀》杂志发表了在中国武汉进行的双盲、随机、安慰剂对照临床试验,原计划入组453名患者,最终实际入组237名,该试验由北京中日友好医院副院长曹彬和北京协和医学院校长王辰团队负责,数据显示与安慰剂对照组相比,未观察到瑞德西韦可以加快住院新冠肺炎患者的病情恢复或降低死亡率 [3]。不过,由于入组人数过少,最后提前终止了临床试验。
2020年5月22日,美国国立卫生研究院(NIH)发布了瑞德西韦的临床研究初步数据,在这项全球多家医院参与,双盲、随机、安慰剂对照的临床试验中,共有1063人参加,显示瑞德西韦可以将因 COVID-19 住院,且需要额外氧气治疗的病人的恢复时间从15天缩短到11天,降低呼吸道感染 [4]。
2020年8月21日,《美国医学会杂志》(JAMA)发布了随机,开放标签的3期临床试验研究,共584名中度 COVID-19 病人参与,随机分为5天和10天两个疗程,通过评估第11天的临床状态,接受5天疗程的患者较标准治疗显著更好,接受10天疗程的患者与标准治疗相比无显著差异 [5]。
2020年8月10日,吉利德向FDA提交瑞德西韦用于治疗 COVID-19 的新药申请。吉利德对外宣称已经拥有可靠的数据,支持对 COVID-19 住院患者人群使用瑞德西韦的评估 [6]。
目前,针对瑞德西韦的研究仍在继续,当前证据显示出一定效果,但尚需更多的临床证据证实是否安全有效。
利巴韦林
小结:单药很可能无效,联合用药显示对轻中症患者有明显效果。仍需进一步试验验证。
利巴韦林(Ribavirin)是一款广谱抗病毒药物,主要用于治疗重症的呼吸道合胞病毒(RSV)感染以及丙型肝炎等疾病,在2003年暴发的 “非典” 中曾作为治疗药物出现。
2020年2月,利巴韦林在国内《新型冠状病毒感染的肺炎诊疗方案》试行第五版中被列为治疗药物,后续更新的版本中对剂量和用法进行了调整。
《柳叶刀》今年5月发表的一项临床试验研究了利巴韦林与干扰素β-1b、洛匹那韦/利托那韦的三联抗病毒疗法的作用。在2020年2月至3月间,香港六所医院招募了127例新冠患者,86例患者使用这种三联抗病毒疗法在发病早期进行治疗,与仅使用洛匹那韦/利托那韦的41例对照组进行了比较。结果显示,这种联合用药可以安全且高效地缩短轻中症患者病毒量转阴的持续时间并减轻症状,且副作用较轻微 [7]。不过该试验还需要进一步开展扩大规模双盲试验进行验证。
此外,华中科技大学同济医学院附属协和医院的一项回顾性研究发现,对于2020年1月至2月间确诊的134名重症患者,利巴韦林单药并没有改善转阴时间,也没有降低死亡率 [8]。
值得注意的是,利巴韦林的安全性一直受到争议 [9],已经报告的不良反应包括致畸、溶血性贫血等。美国FDA明确将利巴韦林列为孕妇禁用的药物。
综上,目前对于利巴韦林的临床试验较少,已经完成的研究基本在国内,但并不能表明利巴韦林是治疗新冠有效且安全的药物。
法匹拉韦
小结:小规模试验显示有效,有待大规模试验验证
法匹拉韦(Favipiravir)是一种抗病毒药物,能靶向作用于对病毒 RNA 的转录和复制所依赖的 RNA 聚合酶,从而阻断病毒 RNA 的复制,抑制病毒的产生。其最初于2014年在日本上市,主要用于治疗流行性感冒,在埃博拉病毒、拉沙病毒等病毒的体外实验中也表现出了一定的抗病毒活性 [10]。2020年2月,法匹拉韦因抗流感获得中国国家药品监督管理局批准在国内上市。
已有的小规模试验研究显示,法匹拉韦有较好的疗效和轻微、可控的不良反应,如2020年2月在深圳进行的临床试验中,法匹拉韦组的35例非重症新冠患者相较于40例对照组病毒的清除时间更短,胸部 CT 也显示出明显的改善 [11]。
但目前已经完成的临床试验规模较小,更大规模的临床试验正在进行或在计划之中。如美国麻省总医院计划在当前的临床试验顺利完成后,将开展更大规模的临床试验 [12]。
未来的大规模临床试验将有助于验证法匹拉韦作为新冠治疗药物的有效性及安全性。
洛匹那韦/利托那韦
小结:基本无效
洛匹那韦/利托那韦(Lopinavir/ritonavir)是抗病毒药物,可以阻止艾滋病病毒(HIV)复制。二十年前,美国FDA批准了这两种药物组合来治疗 HIV。但是这两种药物在新冠患者的临床试验上,显示对治疗 COVID-19 没有明显效果。
2020年3月18日,国家呼吸疾病临床研究中心王辰、中国医学科学院曹彬及武汉金银潭医院张定宇在《新英格兰医学杂志》发表了评估口服洛匹那韦-利托那韦对新冠感染的疗效和安全性的研究结果,这是一项随机,对照,开放标签的试验,共有199名确诊的 COVID-19 感染患者接受了随机分组。在住院的重症 COVID-19 成人患者中,洛匹那韦–利托那韦的治疗未见超出标准治疗的益处[13]。
2020年6月29日,英国的 “康复试验” 纳入了近5000名新冠患者的随机,对照,开放标签的临床试验,显示洛匹那韦/利托那韦对新冠患者没有效果 [14]。
同时,世界卫生组织发起的 “团结试验” 的中期试验结果表明,与标准治疗相比,使用洛匹那韦/利托那韦几乎没有降低 COVID-19 住院患者的死亡率。7月初,世界卫生组织暂停了 “团结试验” 中洛匹那韦/利托那韦对 COVID-19 住院患者的试验 [15]。
阿比朵尔
小结:很可能无效
阿比朵尔(Arbidol)是由前苏联研发的一款抗病毒药物,在俄罗斯广泛使用,主要用于甲型和乙型流感的治疗。它能阻止流感病毒外壳与人体细胞的细胞膜进行融合,同时还有免疫调节的作用。
2020年2月,根据体外细胞实验的结果,阿比朵尔被纳入国家卫健委《新型冠状病毒感染的肺炎诊疗方案(试行第六版)》。随后,多项临床试验在重庆、上海等地区展开。
在 、WHO ICTRP 搜索 “Arbidol+COVID-19” 以及 “Umifenovir+COVID-19”(盐酸阿比朵尔+COVID-19),阿比朵尔对新冠肺炎的临床试验主要在中国、伊朗等地区,但已有的临床试验并未发现其对治疗新冠有显著的疗效。
2020年5月发表的一项在广州进行的针对轻中度新冠住院患者的临床试验,比较了阿比朵尔单药方案、洛匹那韦/利托那韦与无抗病毒治疗的对照组,并未发现这些组间患者的退热、咳嗽缓解、CT 胸片等指标的差异 [16]。上海市公共卫生临床中心在2020年1月到2月初对134例患者的临床资料进行回顾性研究,也没有发现阿比朵尔对治疗新冠肺炎有效 [17]。
PART 02
症状缓解治疗
地塞米松(Dexamethasone)
小结:早期证据表明其减少重症死亡
地塞米松是一种类固醇,能够减轻炎症(部分免疫反应)。长期以来,临床上一直用地塞米松治疗过敏,哮喘和炎症。
目前,在所有试验中的治疗 COVID-19 药物中,地塞米松是唯一一个被证明,可以拯救生命的药物。2020年6月22日,英国的 “康复试验” 有6000多位新冠病人参与的,随机、对照、开放标签临床试验,研究结果发表在《新英格兰医学杂志》上,发现地塞米松的使用让呼吸机患者的死亡人数减少了三分之一,而吸氧患者的死亡人数减少了五分之一;但是,对于处于 COVID-19 感染初期的患者,地塞米松没有作用 [18]。
美国NIH在其 COVID-19 治疗指南中建议,仅在使用呼吸机或正在接受氧气补充的 COVID-19 患者上使用地塞米松 [19]。
关于地塞米松对新冠患者的效果,英国 “康复试验” 表明了其有效性,但是仍然需要更多的研究重复验证其临床效果和潜在副作用的风险。
羟氯喹和氯喹
小结:基本无效
19世纪30年代,德国化学家合成了氯喹,主要作为抗疟疾药物使用。后来,开发了毒性更小的羟氯喹,后来被批准用于其他疾病,例如狼疮和类风湿关节炎。
2020年2月4日,中国科学院武汉病毒肖庚富团队在《细胞研究》上报道,氯喹在体外有效抑制新型冠状病毒 [20]。但是目前,尚无临床研究证实羟氯喹/氯喹(Hydroxychloroquine and chloroquine)对治疗新冠存在临床疗效。多项随机临床试验发现羟氯喹不能治疗 COVID-19。
4月24日,美国FDA发出警告,羟氯喹用于治疗 COVID-19 时,会对心脏和其他器官造成许多严重的副作用。
5月7日,上海交通大学医学院附属瑞金医院牵头的多中心、平行、随机对照临床研究发表在《英国医学杂志》上,研究表明,与标准治疗相比,联合羟氯喹的治疗不能带来病毒转阴的额外效果,且存在一定以消化道症状为主的不良事件的几率 [21]。6月15日,美国FDA撤销了氯喹和羟氯喹的紧急使用授权。
7月15日,提交到预印本 Medrxiv 的英国 “康复试验” 研究结果显示,随机、对照、开放标签临床试验结果显示,羟氯喹对治疗 COVID-19 无效 [22]。世界卫生组织、美国NIH和诺华制药公司已经停止了羟氯喹对新冠的临床试验。
不过,尽管已有结果呈现阴性,许多羟氯喹试验仍在继续。
托珠单抗
小结:尚无法判断
托珠单抗(Tocilizumab)是第一个获得批准的抗白细胞介素6(IL-6)受体的生物制剂,用于治疗中度至重度类风湿关节炎的患者。
在 COVID-19 患者中,大量T淋巴细胞和单核巨噬细胞被激活,产生IL-6等细胞因子,它们与靶细胞上的IL-6受体结合,引起细胞因子风暴和肺和其他组织器官中的严重炎症反应。
托珠单抗是一种重组的人源化抗人IL-6受体单克隆抗体,可以与IL-6受体高亲和力结合,从而阻止IL-6自身与其受体结合,使其无法对靶细胞进行免疫损伤,并减轻炎症反应。
4月29日,中国科技大学生命科学学院魏海明团队在《美国科学院院刊》发布的论文显示,观察21人被诊断为重症或微重症的 COVID-19 患者,给予托珠单抗后的治疗效果。初步数据显示,重症或危重症的新冠患者进行托珠单抗治疗可立即改善临床疗效,是降低死亡率的有效方法 [23]。
7月8日,《传染病研究》(Journal of Infection)杂志上报道了一项回顾性单中心分析,发现托珠单抗可以降低 COVID-19 患者的死亡率, 但存在暂时性呼吸恶化和细菌感染的严重的不良事件 [24]。但目前缺乏随机对照临床试验,因此尚无法判断改善是否由于托珠单抗本身的作用。
无创和有创氧气支持
小结:广泛使用,应急使用
新冠病毒一般高度累积在肺部,而肺又是交换氧气的重要器官。当炎性分泌物充斥于肺间质和肺泡里时,会阻断新鲜空气进入肺泡与体内的二氧化碳进行交换,导致机体缺氧甚至多脏器功能失调、衰竭或死亡。
目前市面上没有对抗新冠病毒的特效药或疫苗,氧气支持是对抗新冠病毒至关重要且在临床上最为广泛使用的一个治疗手段[25]。
轻症新冠肺炎患者,会在医生指导下通过与制氧机相连的鼻管或氧气面罩等无创方式来获取氧气,缓解新冠病毒造成的轻中度急性呼吸窘迫综合症(ARDS)。该治疗方式可以改善患者的氧合,降低呼吸负荷和插管率,提升舒适度 [25]。
但是,无创氧气治疗在重症或危重症新冠患者身上可能会由于患者过强的自主呼吸造成气压差异,引起相关性肺损伤。所以对于重症和危重症患者,医生通常会改为有创通气(呼吸机或者人工心肺)来保护肺细胞,也为病人创造宝贵的治疗时间来帮助患者唤醒自身的免疫系统。如果重症和危重症新冠患者延迟从无创通气到有创通气的转变,病死率则会明显地增加 [26]。
总体而言,结合国内外多个临床实践和报道的氧气治疗结果,可以看出:无创氧疗适用于治疗轻中症新冠患者,改善临床症状和氧合的同时也能增加舒适度。但对于重症新冠患者来说,过多依赖无创呼吸氧疗会导致插管延迟,病死率增高 [27]。
康复者血浆治疗
小结:仅作为危重型患者的试验性治疗
从一个世纪之前的西班牙大流感到非典、甲型流感、埃博拉和MERS,医生都使用过患者康复后的血浆对患者进行传统的输血治疗。康复者血浆治疗的其原理在于当病人感染病毒后,血浆中会产生大量的特异性抗体,用于消灭病毒。当把恢复期病人的血浆输入到另一个患者体内,抗体也能有同样的效果。
目前来看,康复者血浆治疗仅作为危重型患者的试验性治疗。
2020年6月发表在 JAMA 的研究在2月在武汉招募了103名新冠肺炎重症与危重症志愿者。试验组重症患者和危重症患者(总共52人)在接受血浆治疗后,临床改善时间和72小时核酸转阴率与对照组(51人)相比有显著性差异 [28]。
8月23日,美国FDA通过将恢复期血浆用于新冠住院患者治疗的紧急使用授权。不过,这项决定在科学界看来是受到了来自特朗普方面的政治压力,仍未有有力证据支持该疗法的安全性和有效性[29]。
现有的血浆治疗对于新冠患者有效的研究,多数都是小样本临床试验,缺乏高质量双盲随机对照组的临床试验。因为一个危重病人可能需要7-10个同血型的康复者提供血浆,所以就算之后大样本分析显示血浆治疗对于新冠患者有效,有限的血浆也无法满足大量新型肺炎患者的需求。
血液透析
小结:对肾脏,肝脏损伤的危重症患者有一定效果
对于新冠肺炎患者来说,从轻症变为重症,或是重症和危重症最终死亡的一个重要节点,就是病毒入侵引起的细胞因子风暴和肾脏损害。细胞因子风暴是人体免疫系统反应过激的一种现象。研究表明,细胞因子风暴和疾病的严重程度相关,也能作为预测死亡的指标之一。在因为新冠病毒住ICU的患者体内,其细胞因子的表达远高过于没有住进ICU的患者 [30]。
为了降低新冠重症患者的病死率,对于高炎症反应的患者,有些临床治疗采用了针对细胞因子风暴而导致的过度炎症以及脏器衰竭的症状。血浆置换,吸附,灌流,血液/血浆过滤等体外血液净化技术可以清除血液里部分细胞因子的浓度,组织这群“讯息传递员”的过度传讯,并纠正代谢紊乱,改善心功能不全等症状[31]。该疗法于今年4月得到美国FDA的紧急批准,可以用来治疗重症新冠肺炎。
人工肝
小结:对降低死亡率有一定效果
新冠病毒感染会引发急性肾损伤,导致人体自身的代谢能力和脏器功能显著下降。数据显示,在新冠肺炎患者中,急性肾损伤的整体发生率不高,约5-10%,但是在重症患者中的发生率较高,约55%,并和死亡率有显著关联 [32]。
多个临床报道显示血液净化治疗是对于新冠患者出现肾脏和肝脏损伤时的治疗方法之一。其中持续肾脏替代治疗(CRRT)或者人工肝的血液净化疗法,对于重症新冠患者能有效地清除血液里多余的细胞因子,从而稳定免疫系统。同时,血液疗法还能改善水电解质和酸碱的平衡,清除代谢产出的垃圾,达到降低死亡率的效果 [33]。2020年6月,一项来自浙江大学医学院回顾性研究显示,在23名新冠危重症患者中, 人工肝显著地减少了炎症因子的表达水平,并延长了病人的存活时间 [34]。
因此,对于新冠患者来说,住院后随时监控肾脏与肝脏功能,并在需要的时候使用干预措施是降低死亡率的关键。
PART 03
中药篇
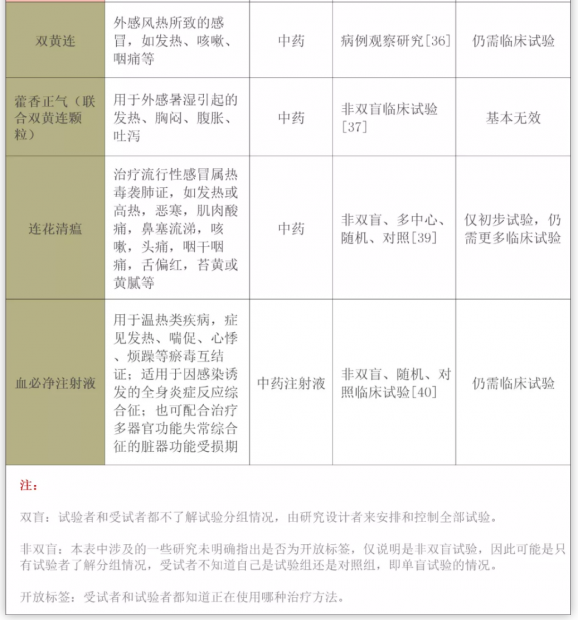
双黄连
小结:仍需更多临床试验
双黄连主要成分为金银花、黄芩、连翘,辅料为蔗糖,主要用于外感风热所致的感冒,如发热、咳嗽、咽痛等。临床上常用的双黄连药物包括双黄连口服液和双黄连注射剂。
2020年7月31日,中科院武汉病毒研究所、中科院上海药物研究所和上海科技大学联合科研团队关于双黄连抑制新冠病毒的体外实验结果发表于《中国药理学报》(Acta Pharmacologica Sinica)[35]。该报道指出,双黄连口服液和注射剂都能抑制 SARS-CoV-2 在 Vero E6 细胞的复制,其中的黄芩苷和黄芩苷起主要作用。
华中科技大学同济医院心血管内科汪道文课题组在《医学前沿》(Frontiers of Medicine)杂志发表了双黄连联合西药治疗促进3例新冠肺炎患者康复的病例报告 [36]。该报告最后指出,“双黄连可能对治疗新冠肺炎有效,而应用到临床还需要后续的临床试验以获得足够的证据”。
目前,双黄连对新冠病毒的抑制作用停留在实验室体外研究阶段,临床试验验证病例数量较少,能否治疗新冠肺炎还有待更多依据。
双黄连+藿香正气联合西药治疗
小结:基本无效
2020年8月8日,《药理学研究》(Pharmacological Research)杂志刊发了北京广安门医院和湖北中医药大学共同完成的双黄连加藿香正气联合西药治疗(中西医联合治疗)新冠肺炎的非双盲临床试验结果:双黄连和藿香正气的加入对改善患者临床症状,抑制病情加重没有明显的作用 [37]。
连花清瘟
小结:仅初步试验,仍需更多临床试验。
连花清瘟主要成分为连翘、金银花、炙麻黄、炒苦杏仁、石膏、板蓝根、绵马贯众、鱼腥草、广藿香、大黄、红景天、薄荷脑、甘草,可清瘟解毒,宣肺泄热,用于治疗流行性感冒属热毒袭肺证,如发热或高热,恶寒,肌肉酸痛,鼻塞流涕,咳嗽,头痛,咽干咽痛,舌偏红,苔黄或黄腻等。
2020年3月发表在《药理学研究》(Pharmacological Research)体外实验表明,连花清瘟可以抑制新冠病毒的复制,降低炎性细胞因子的转录水平 [38]。但该项研究的实验设计缺乏药物溶剂对照,并且研究结果显示连花清瘟对宿主细胞的毒性作用要高于瑞德西韦。
2020年5月16日,《植物医学》(Phytomedicine)杂志发表钟南山团队的一项非双盲多中心随机对照临床试验结果:连花清瘟胶囊联合常规治疗可以显著缩短新冠肺炎患者的康复时间,有效缓解临床症状 [39]。不过,参与该临床试验的均为无基础病的轻症患者,在14日恢复率上仅有不到十个百分点的差异。更重要的是,该临床试验是开放式试验(Open-label trial),病人和医生均明确知道分组情况,很容易给治疗组造成安慰效应,影响试验的客观性。因此该文章最后结论部分指出,“完全评价连花清瘟治疗新冠肺炎的疗效需要未来更大规模的双盲随机临床试验”。
血必净注射剂
小结:小样本高剂量显示有效,仍需更多临床试验。
血必净主要成分为红花、赤芍、川芎、丹参和当归,用于温热类疾病,症见发热、喘促、心悸、烦躁等瘀毒互结证;适用于因感染诱发的全身炎症反应综合征;也可配合治疗多器官功能失常综合征的脏器功能受损期。
4月14日,血必净注射液获得新冠肺炎适应症审批,“功能主治”新增“可用于新型冠状病毒肺炎重症、危重症的全身炎症反应综合征或/和多脏器功能衰竭”。其时关于血必净有效抑制新冠病毒的体外实验和动物实验结果尚未见研究报道。
2020年4月28日,《中华危重病急救医学》一篇前瞻性随机对照临床试验文章称,常规治疗联合血必净注射液可有效改善重型新冠肺炎患者的炎症指标及病情转归,参与该项临床试验的患者共60例 [40]。
目前,血必净注射液是否能够治疗新冠肺炎有待更多临床试验数据。
总 结
到目前为止,并没有哪一种疗法或者药物可以称为治疗新冠肺炎的特效药,但这并不影响医生的救治和患者的痊愈。纵观全文可以发现,一些新冠疫情期间受到关注的药物至今尚未出现具有说服力的临床证据。尽管有些试验中能够看到患者情况出现了一定改善,但治疗新冠肺炎的最终效果 “仍有待更多临床试验结果”。
人们期待疫苗和药物能够帮助我们回到正常生活,也不得不接受科学过程中的沮丧和曲折。科学史上从不缺少受政治、经济或人们的期待出现的 “奇迹”,最终造成了无尽的悔恨。面对病毒,怀抱希望,但能够用多大的勇气迎接现实,或许是摆在人类眼前的一大考验。
对于这一专题,《知识分子》将定期更新最新进展。期待读者朋友们共同关注。
参考文献
[1] Thorlund K, Dron L, Park J, Hsu G, Forrest JI, Mills EJ. A real-time dashboard of clinical trials for COVID-19. The Lancet Digital Health. 2020;2(6):e286-e7.
[2] Mulangu, Sabue, Lori E. Dodd, Richard T. Davey Jr, Olivier Tshiani Mbaya, Michael Proschan, Daniel Mukadi, Mariano Lusakibanza Manzo et al. "A randomized, controlled trial of Ebola virus disease therapeutics." New England Journal of Medicine 381, no. 24 (2019): 2293-2303.
[3] Wang, Yeming, Dingyu Zhang, Guanhua Du, Ronghui Du, Jianping Zhao, Yang Jin, Shouzhi Fu et al. "Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial." The Lancet (2020).
[4] Beigel, John H., Kay M. Tomashek, Lori E. Dodd, Aneesh K. Mehta, Barry S. Zingman, Andre C. Kalil, Elizabeth Hohmann et al. "Remdesivir for the treatment of Covid-19—preliminary report." New England Journal of Medicine (2020).
[5] JAMA. Effect of Remdesivir vs Standard Care on Clinical Status at 11 Days in Patients With Moderate COVID-19A Randomized Clinical Trial. [6] Hung IF, Lung KC, Tso EY, Liu R, Chung TW, Chu MY, et al. Triple combination of interferon beta-1b, lopinavir-ritonavir, and ribavirin in the treatment of patients admitted to hospital with COVID-19: an open-label, randomised, phase 2 trial. Lancet. 2020;395(10238):1695-704.
[6]
[7] Hung IF, Lung KC, Tso EY, Liu R, Chung TW, Chu MY, et al. Triple combination of interferon beta-1b, lopinavir-ritonavir, and ribavirin in the treatment of patients admitted to hospital with COVID-19: an open-label, randomised, phase 2 trial. Lancet. 2020;395(10238):1695-704.
[8] Song T, Yuan S, Yuan Y, Chuangyan W, Jiuling C, Sihua W, et al. Ribavirin Therapy For Severe COVID-19: A Retrospective Cohort Study. Int J Antimicrob Agents. 2020:106114.
[9] Chiou HE, Liu CL, Buttrey MJ, Kuo HP, Liu HW, Kuo HT, et al. Adverse effects of ribavirin and outcome in severe acute respiratory syndrome: experience in two medical centers. Chest. 2005;128(1):263-72.
[10] Shiraki K, Daikoku T. Favipiravir, an anti-influenza drug against life-threatening RNA virus infections. Pharmacol Ther. 2020;209:107512.
[11] Cai Q, Yang M, Liu D, Chen J, Shu D, Xia J, et al. Experimental Treatment with Favipiravir for COVID-19: An Open-Label Control Study. Engineering. 2020.
[12]
[13] Cao, Bin, Yeming Wang, Danning Wen, Wen Liu, Jingli Wang, Guohui Fan, Lianguo Ruan et al. "A trial of lopinavir–ritonavir in adults hospitalized with severe Covid-19." New England Journal of Medicine (2020).
[14]#:~:text=studied%20in%20RECOVERY-,No%20clinical%20benefit%20from%20use%20of%20lopinavir%2Dritonavir%20in%20hospitalised,19%20patients%20studied%20in%20RECOVERY&text=21.3%25%20usual%20care%3B%20relative%20risk,in%20different%20subgroups%20of%20patients.
[15]
[16] Li Y, Xie Z, Lin W, Cai W, Wen C, Guan Y, et al. Efficacy and safety of lopinavir/ritonavir or arbidol in adult patients with mild/moderate COVID-19: an exploratory randomized controlled trial. Med. 2020.
[17] 陈军, 凌云, 席秀红. 洛匹那韦利托那韦和阿比多尔用于治疗新型冠状病毒肺炎的有效性研究. 中华传染病杂志. 2020;38(00):E008-E.
[18] RECOVERY Collaborative Group. "Dexamethasone in hospitalized patients with Covid-19—preliminary report." New England Journal of Medicine (2020).
[19]
[20] Wang, Manli, Ruiyuan Cao, Leike Zhang, Xinglou Yang, Jia Liu, Mingyue Xu, Zhengli Shi, Zhihong Hu, Wu Zhong, and Gengfu Xiao. "Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro." Cell research 30, no. 3 (2020): 269-271.
[21] Tang, Wei, Zhujun Cao, Mingfeng Han, Zhengyan Wang, Junwen Chen, Wenjin Sun, Yaojie Wu et al. "Hydroxychloroquine in patients with mainly mild to moderate coronavirus disease 2019: open label, randomised controlled trial." bmj 369 (2020).
[22]
[23] Xu, Xiaoling, Mingfeng Han, Tiantian Li, Wei Sun, Dongsheng Wang, Binqing Fu, Yonggang Zhou et al. "Effective treatment of severe COVID-19 patients with tocilizumab." Proceedings of the National Academy of Sciences 117, no. 20 (2020): 10970-10975.
[24] Rossotti, Roberto, Giovanna Travi, Nicola Ughi, Matteo Corradin, Chiara Baiguera, Roberto Fumagalli, Maurizio Bottiroli et al. "Safety and efficacy of anti-il6-receptor tocilizumab use in severe and critical patients affected by coronavirus disease 2019: A comparative analysis." Journal of Infection (2020).
[25] Lyons, C. & Callaghan, M. The use of high‐flow nasal oxygen in COVID‐19. Anaesthesia 75, 843-847 (2020).
[26] Meng, L., Qiu, H., Wan, L., Ai, Y., Xue, Z., Guo, Q., ... & Liu, H. (2020). Intubation and Ventilation amid the COVID-19 OutbreakWuhan’s Experience. Anesthesiology: The Journal of the American Society of Anesthesiologists, 132(6), 1317-1332.
[27] Whittle, J. S., Pavlov, I., Sacchetti, A. D., Atwood, C. & Rosenberg, M. S. Respiratory support for adult patients with COVID‐19. Journal of the American College of Emergency Physicians Open 1, 95-101 (2020).
[28] Li, L. et al. Effect of Convalescent Plasma Therapy on Time to Clinical Improvement in Patients With Severe and Life-threatening COVID-19: A Randomized Clinical Trial. JAMA, doi:10.1001/jama.2020.10044 (2020).
[29]
[30] Huang, C., Wang, Y., Li, X., Ren, L., Zhao, J., Hu, Y., ... & Cheng, Z. (2020). Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. The lancet, 395(10223), 497-506.
[31] Zhang, Y. et al. A Promising Anti-Cytokine-Storm Targeted Therapy for COVID-19: The Artificial-Liver Blood-Purification System. Engineering (Beijing), doi:10.1016/j.eng.2020.03.006 (2020).
[32] Cheng, Y., Luo, R., Wang, K., Zhang, M., Wang, Z., Dong, L., ... & Xu, G. (2020). Kidney disease is associated with in-hospital death of patients with COVID-19. Kidney international.
[33] Yang, X. H. et al. Expert recommendations on blood purification treatment protocol for patients with severe COVID-19: Recommendation and consensus. Chronic Dis Transl Med, doi:10.1016/j.cdtm.2020.04.002 (2020).
[34] Liu, J., Dong, Y. Q., Yin, J., He, G., Wu, X., Li, J., ... & He, X. (2020). Critically ill patients with COVID-19 with ECMO and artificial liver plasma exchange: A retrospective study. Medicine, 99(26).
[35] Hai-Xia Su, Sheng Yao, Wen-Feng Zhao, et al,. Anti-SARS-CoV-2 activities in vitro of Shuanghuanglian preparations and bioactive ingredients. Acta Pharmacol Sin. 2020 Jul 31;1-11. doi: 10.1038/s41401-020-0483-6.
[36] Li Ni, Ling Zhou, Min Zhou, et al,. Combination of western medicine and Chinese traditional patent medicine in treating a family case of COVID-19. Front Med 2020 Apr;14(2):210-214. doi: 10.1007/s11684-020-0757-x.
[37] Xiao M, Tian J, Zhou Y, et al,. Efficacy of Huoxiang Zhengqi dropping pills and Lianhua Qingwen granules in treatment of COVID-19: A randomized controlled trial, Pharmacological Research (2020), doi:
[38] Runfeng L, Yunlong H, Jicheng H, et al,. Lianhuaqingwen exerts anti-viral and anti-inflammatory activity against novel coronavirus (SARS-CoV-2). Pharmacol Res. 2020 Jun;156:104761. doi: 10.1016/j.phrs.2020.104761.
[39] Hu K, Guan WJ, Bi Y, et al,. Efficacy and safety of Lianhuaqingwen capsules, a repurposed Chinese herb, in patients with coronavirus disease 2019: A multicenter, prospective, randomized controlled trial. Phytomedicine. 2020 May 16:153242. doi: 10.1016/j.phymed.2020.153242.
[40] 文隆, 周志国, 姜迪譞, 等. 血必净注射液对重型新型冠状病毒肺炎患者炎症指标及病情转归的疗效观察.中华危重病急救医学,2020,32 (04): 426-429.
[41] Wang, D., Hu, B., Hu, C., Zhu, F., Liu, X., Zhang, J., ... & Zhao, Y. (2020). Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus–infected pneumonia in Wuhan, China. Jama, 323(11), 1061-1069.
[42] Ma, J., Xia, P., Zhou, Y., Liu, Z., Zhou, X., Wang, J., ... & Qin, Y. (2020). Potential effect of blood purification therapy in reducing cytokine storm as a late complication of critically ill COVID-19. Clinical Immunology (Orlando, Fla.), 214, 108408.
制版编辑 | 皮皮鱼
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 