阅读:0
听报道

“每年得到诺奖的科学家只有几位,但不能因此否定其他科研工作者不重要” | 图源:
编者按
一般认为,一个研究领域获得诺奖,这个领域的其他科学家获得诺奖的几率就会大大减少。那么,你是会继续从事这个领域的研究,还是会换个赛道?
今年诺奖得主 Ardem Patapoutian 曾经的博士后、如今在清华大学药学院任职的肖百龙教授认为,一个领域是由很多科研工作者的工作共同推进的,每年得到诺奖的科学家只有几位,但不能因此否定其他科研工作者的重要性。“如果这样想(只想得诺奖),很多问题可能都会研究不清楚。”
访谈 | 陈晓雪
整理 | 陈晓雪 刘楚 李可
2021年诺贝尔生理学或医学奖颁给了美国的两位科学家,分别是加州大学旧金山分校的大卫·朱利叶斯(David Julius)和Scripps研究所的阿德姆·帕塔普蒂安(Ardem Patapoutian),奖励他们发现了温度和触觉的受体。

具体来说,David Julius 利用辣椒素(一种从辣椒中提取的刺激性化合物,能产生灼烧感)来识别皮肤神经末梢上对热做出反应的感受器(TRP通道)。而 Ardem Patapoutian 利用压力敏感细胞发现了一种对皮肤和内部器官的机械刺激作出反应的新型感受器(PIEZO通道)。
清华大学药学院教授肖百龙曾在 Ardem Patapoutian 实验室做博士后研究,对于确立PIEZO蛋白是机械门控阳离子通道的核心孔道蛋白作出了重要贡献。他随后在清华大学独立开展工作,其实验室在PIEZO通道的后续研究中做出了系列突破性成果。

图1 2019年,肖百龙(右一)与博士后导师Ardem Patapoutian(左二)在一个学术会议上 | 本图由受访者提供
例如,与本次诺奖直接相关的介导触觉、本体觉感知的PIEZO2通道,其三维结构就由他与清华大学李雪明实验室合作解析出来 [1]。诺奖官网介绍此次诺奖工作的科学背景时,引用了肖百龙实验室5篇论文,配图亦源自其所解析的PIEZO2通道的结构。
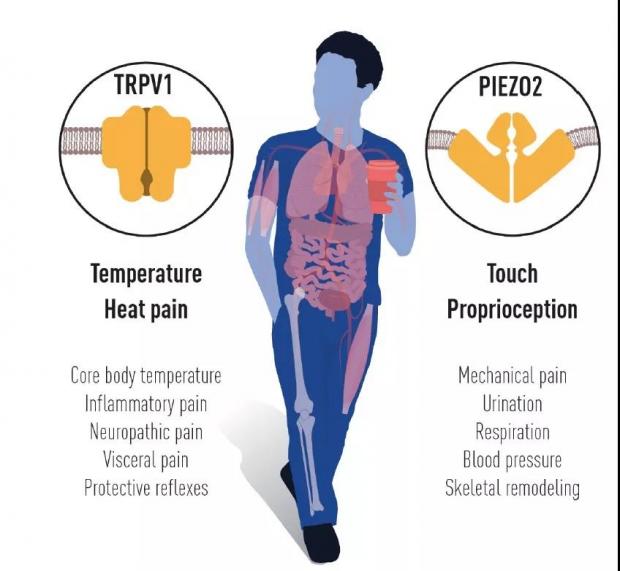
图2 诺奖官网关于TRPV1 和 PIEZO2 通道功能的介绍。PIEZO2结构由肖百龙实验室与其合作者解出 | 图源:
10月4日晚,《知识分子》在第一时间联系到了肖百龙,邀请他对Ardem Patapoutian因PIEZO通道获得诺奖进行评论。
在与《知识分子》的对谈中,他回忆了与Ardem Patapoutian一起工作的情况,还谈到了当前TRPV1通道和PIEZO通道研究尚未解决的重要科学问题,同时对此次获得诺奖的两类重要离子通道在今后成药方面的展望。
以下是《知识分子》和肖百龙的对话文字整理:
知识分子:去年Ardem Patapoutian和David Julius获得科维理奖,今年又同获诺奖,你有什么评论吗?
肖百龙:Ardem实验室鉴定发现了介导脊椎动物机械力感知的首类机械力分子受体PIEZO1与PIEZO2,对于我们理解机械力感知的分子机制具有开创性意义。因此,他因这个工作获得今年的诺贝尔奖我觉得一点不surprised,PIEZO通道的工作完全值得一个诺奖。
温度和机械力是我们的环境中非常基本的一些因素,影响到我们的生物机体,包括人体或其他哺乳动物。我们到底怎么去感知这样的环境因素,这样的问题,我觉得是非常基础,也是非常重要的。
PIEZO通道是负责感知机械力的。对于我们的每一个拥抱,我们使用每一种工具,包括我们天天刷手机,可能大家平时对这些行为的发生都习以为常了,但这些行动都依赖于对力的感觉,它实际上就是由PIEZO来介导。
从另外一个角度,它跟很多疾病有重要的相关性,PIEZO通道的一些基因突变可以导致多种人类遗传疾病,PIEZO通道正常有比较重要的生理功能,异常会导致很多的人类遗传疾病,说明它对人体的功能有不可或缺的重要作用。
所以,就不难理解它为什么能够获诺贝尔奖。
知识分子:关于TRPV1通道的研究,其透彻程度现在比PIEZO通道更深一些吗?
肖百龙:TRPV1通道是1997年发现的,经过大概24年的研究,对于其如何被辣椒素等化学刺激激活已经有很深入的理解。然而,TRPV1如何被温度激活这个核心问题到现在也还没有被解决。
PIEZO通道是2010年发现的,到现在有11年的时间。由于研究方式的改变,我们对PIEZO通道的结构功能机制也有了很好的进展,对于其如何感知机械力已经提出了比较明确可以测试的假说,希望接下来我们的研究工作能从根本上解答这一核心问题。
知识分子:有观点认为,相对于TRP通道来说,PIEZO通道的诺奖发早了,还需要后续的实验工作来进一步验证。对此你怎么看?
肖百龙:对此我完全不认同。虽然PIEZO通道晚于TRPV1通道被发现,但近10年来对PIEZO通道的生理病理功能、结构功能机制方面的研究取得了大量进展,现在非常明确PIEZO通道作为机械力分子受体在哺乳动物,包括人类自身,承担广泛而不可或缺的重要生理功能。
譬如,缺失PIEZO2的病人会丧失触觉、本体觉、内脏觉的机械力感知。在PIEZO通道的结构机制研究方面,我课题组做了系列重要突破性工作,譬如与合作者首次解析报导了PIEZO1(Nature 2015, Nature 2018)[2,3] 与PIEZO2(Nature 2019)[1] 的三维结构,并提出了其感受机械力的分子机制模型(Neuron 2016; Neuron 2020)[4,5]。我认为这对PIEZO通道被授予诺贝尔奖起到了重要的推动作用。确实,在诺奖官网介绍这次诺奖工作的科学背景介绍中,我们实验室有5篇论文被引用,配图中的PIEZO通道的结构模型也源自我课题组与合作者所首次解析的三维结构。
但需要指出的是,TRPV1如何感知温度以及PIEZO通道如何感知机械力的分子机制迄今都还未完全研究清楚,我认为这是需要解决的根本性问题。这也许是这次诺奖工作的美中不足之处。
知识分子:除了PIEZO,在感知压力和感觉方面,目前还有发现别的蛋白吗?
肖百龙:应该还有。比如在听觉里面,我们对声音的感知,也是靠机械敏感的离子通道来实现的,但这个现在还有争论,没有特别明确。另外,包括触觉系统的感受,像钉子砸在手上这种机械疼是什么来介导的也还有待去发现。
知识分子:肖教授,你是怎么开始研究 PIEZO通道的?
肖百龙:实际上我很早就参与了PIEZO相关的工作。我去Ardem实验的时候是2007年,当时Ardem实验室也是在做温度敏感TRP通道。David Julius发现第一个TRPV1通道分子,但Ardem实验室后续发现了一系列对温度敏感的分子受体,包括感受凉爽的,感受温热的,还有别的一些通道感受冷的。
与此同时,当时领域内的科学家都想去找机械门控离子通道,但是在技术方法上非常难找,因为它研究的手段是非常有挑战的。
2007年,Ardem招了来自法国的博士后 Bertrand Coste,他博士阶段的工作主要是利用电生理的方法记录感觉神经元里的机械敏感电流,因此具备非常好的技术背景去寻找哺乳动物细胞里的机械敏感离子通道。通过3年多的努力,他最终成功鉴定出 PIEZO 基因介导哺乳动物细胞的机械力刺激诱发的阳离子电流。该工作于2010年发表在《科学》杂志 [6]。
PIEZO蛋白是非常独特且难研究的一类大型膜蛋白,包含2500多个氨基酸和30-40次预测跨膜区,是哺乳动物蛋白中含预测跨膜次数最多的膜蛋白,且与任何已知离子通道或其它蛋白家族都不具备序列同源性。因此,PIEZO蛋白自身是否作为机械门控阳离子通道的核心孔道蛋白并不清楚。
因为我有很好的大型膜蛋白分子生化的研究背景,我博士的研究就做了很好的技术上的铺垫。所以,我在Ardem实验室的第二个工作,就是证明了PIEZO蛋白是机械门控通道的核心孔道亚基。
当时,我率先开展了PIEZO蛋白的理化特性研究,成功建立起这一大型膜蛋白的分子克隆及哺乳动物细胞表达纯化体系,并获得鼠源全长 PIEZO1(2547个氨基酸)的重组表达纯化蛋白。结合生化、人工脂质体重组及单通道电生理记录等方法,证实纯化的PIEZO1蛋白形成多聚体、且重组到人工脂双层膜后能介导阳离子电流,为PIEZO1蛋白自身形成离子通道提供了关键实验证据。该研究成果于2012年以长文形式发表在《自然》(Nature 2012),我是该论文的共同第一作者 [7]。这篇文章现在已经被收录进由2000年诺贝尔生理学或医学奖得主 Eric Kandel 等主编的第6版《神经科学原理》(Principles of Neural Science),以及美国斯坦福大学教授、美国科学院院士骆立群主编的《神经生物学原理》(Principles of Neurobiology)教科书。
机械门控PIEZO通道的发现确立开辟了神经科学、生理学、药理学、生物力学等领域新的研究方向,并迅速成为前沿研究热点。
知识分子:听你介绍,Ardem原来也可以看作早期在追随David Julius研究温度敏感TRP通道,但后来发现了PIEZO通道。你觉得原始创新发生在什么时候?
肖百龙:Ardem除了找温度分子受体,也在找机械力的受体,但实际上大家可能有的时候需要这样的机会,和合适的人去做,也需要一定的运气。
有些科学发现也还是有一些幸运的成分在里面。我觉得Bertrand Coste鉴定出PIEZO蛋白有一定的偶然性,但也有必然性。他在法国做的博士训练,就是一个非常适合于去找这个通道的人,他会利用电生理技术在细胞上去计录机械力产生的电流,正好借助他的技术和Ardem实验室的资源和支持,能开展这样的工作。所以发现也是必然的。
知识分子:Coste有继续研究PIEZO通道吗?
肖百龙:他在法国建立了自己的实验室。据我所知,他还在继续找新的机械门控通道。从他最近的报道,可能也还没有成功。
知识分子:Ardem很早就研究TRP离子通道,并且有不错的结果,11年前又发现了PIEZO蛋白,他现在的工作状态是怎么样的?
肖百龙:Ardem是非常创新性的科学家,TRP通道是在1997年发现的,他进入的是非常早的,之后lead了PIEZO通道的工作。
现在,他还在找一些新的通道 ,从动物转向植物,因为植物也有一些机械敏感通道,比如说含羞草,碰一下就会有反应,他最近有一篇报告就是介绍这个工作的。
我从他身上学到很多,他永远不是停滞在一个地方,而是总在探索下一个领域,是非常优秀的科学家。
知识分子:你在清华现在的工作主要是做什么呢?
肖百龙:2013年到清华以后,基于我们在生化方面的优势,结合冷冻电镜技术的突破,当时我们就跟清华这边做结构的老师合作,首次报道了第一个PIEZO1通道的三维结构(Nature 2015)[2]。我们后面进一步报道了PIEZO通道的一系列的结构 [3,1,5]。
与本次诺奖直接相关的PIEZO2通道介导触觉、本体觉,它的三维结构是我们实验室跟李雪明老师实验室合作解析出来的(Nature 2019)[1],世界上也只有我们解析了PIEZO2的结构,因为其分子生化非常困难。
总结而言,近10年来我及我课题组一直在致力于探究哺乳动物包括人类自身如何感知机械力这一生命科学本质问题,聚焦于从分子、细胞及动物水平解答机械力分子受体-机械门控PIEZO通道如何将机械力刺激转化为电化学信号并决定其生理病理功能这一关键科学问题,并致力于开发PIEZO通道新型药物和技术。
知识分子:什么样的情况下,关于PIEZO通道去感知力的问题算是完全解决了?
肖百龙:力看不见摸不着,很难直接研究。但我们从初中物理教科书就知道,力的表现形式为受力对象的形变。所以我认为PIEZO通道作为机械力分子受体应该也会在受力后发生形变。因此,我们希望能够在后续研究中获取PIEZO通道在接受机械力刺激后从关闭态到开放态的动态构象变化。
知识分子:你回到清华研究PIEZO通道,跟Ardem工作是不是也形成一定竞争?
肖百龙:刚回来是有一定竞争。但我很清楚自己的研究基础和特长,在PIEZO通道分子机制的研究上有竞争力,我们在这方面应该处于领域里的前沿。现在我们保持很好的沟通,都希望对这个领域有一个健康的推动,把关键的科学问题解决掉。即使有竞争也不一定是坏事,可以是良性的竞争。
知识分子:Julius最早发现了TRPV1通道,可能很多科学家会考虑,别人第一个做出来了自己再去接着做,在获得诺奖上不是很有优势,你在做研究的时候会怎么考虑?
肖百龙:我个人更希望是关注重要的科学问题,而不是关注所做的工作是不是可以得诺贝尔奖。科研工作者那么多,每年得诺奖的毕竟就那么几位,不能因此就否定其他科研工作者的重要。如果这样想(只想得诺奖),很多问题可能都会研究不清楚。
比如PIEZO通道的发现实际上带来大量问题,如何解释其生理和病理功能不是一个实验室能做完的,比如分子机制可能就不是Ardem实验室最擅长的。我自己觉得把PIEZO通道如何将机械力转化成电信号这一问题,重要性不一定比发现PIEZO通道差。譬如,发明一个通道之后如何做药物开发,就需要知道它怎么工作。
科学研究需要延承,需要大量的科学家去持之以恒开展深入系统的工作。
知识分子:诺贝尔奖经常发给已经显现出医疗价值的成果,比如青蒿素和丙肝药物,但TRPV1和PIEZO好像都还没有明显的直接应用?
肖百龙:对,我们现在工作的一个重要方向就是对PIEZO通道机制进行深入了解,进而帮助药物开发,意义也是非常重要的。
参考文献:
1. Wang, Li, Heng Zhou, Mingmin Zhang, Wenhao Liu, Tuan Deng, Qiancheng Zhao, Yiran Li, Jianlin Lei, Xueming Li, and Bailong Xiao. "Structure and mechanogating of the mammalian tactile channel PIEZO2." Nature 573, no. 7773 (2019): 225-229.
2. Ge, Jingpeng, Wanqiu Li, Qiancheng Zhao, Ningning Li, Maofei Chen, Peng Zhi, Ruochong Li, Ning Gao, Bailong Xiao, and Maojun Yang. "Architecture of the mammalian mechanosensitive Piezo1 channel." Nature 527, no. 7576 (2015): 64-69.
3. Zhao, Qiancheng, Heng Zhou, Shaopeng Chi, Yanfeng Wang, Jianhua Wang, Jie Geng, Kun Wu et al. "Structure and mechanogating mechanism of the Piezo1 channel." Nature 554, no. 7693 (2018): 487-492.
4. Zhao, Qiancheng, Kun Wu, Jie Geng, Shaopeng Chi, Yanfeng Wang, Peng Zhi, Mingmin Zhang, and Bailong Xiao. "Ion permeation and mechanotransduction mechanisms of mechanosensitive piezo channels." Neuron 89, no. 6 (2016): 1248-1263.
5. Geng, Jie, Wenhao Liu, Heng Zhou, Tingxin Zhang, Li Wang, Mingmin Zhang, Yiran Li, Bo Shen, Xueming Li, and Bailong Xiao. "A plug-and-latch mechanism for gating the mechanosensitive Piezo channel." Neuron 106, no. 3 (2020): 438-451.
6. Coste, Bertrand, Jayanti Mathur, Manuela Schmidt, Taryn J. Earley, Sanjeev Ranade, Matt J. Petrus, Adrienne E. Dubin, and Ardem Patapoutian. "Piezo1 and Piezo2 are essential components of distinct mechanically activated cation channels." Science 330, no. 6000 (2010): 55-60.
7.Coste, Bertrand, Bailong Xiao, Jose S. Santos, Ruhma Syeda, Jörg Grandl, Kathryn S. Spencer, Sung Eun Kim et al. "Piezo proteins are pore-forming subunits of mechanically activated channels." Nature 483, no. 7388 (2012): 176-181.
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 