导 读
随着CRISPR-cas9为代表的新一代基因编辑技术的日趋成熟,人类基因编辑的全球治理已经被提上日程。然而,一个受到忽视的深层次问题是:传统的全球科技治理模式仍然适用吗?
2021年11月23日,浙江大学公共管理学院百人计划研究员俞晗之,清华大学公共管理学院/苏世民书院教授薛澜,美国北卡罗莱纳州立大学教授鲁道夫·巴兰古(Rodolphe Barrangou),湖南大学公共管理学院教授陈少威和武汉大学信息管理学院副教授黄颖在《美国科学院院刊》(Proceedings of the National Academy of Sciences of the United States of America,PNAS)发表评论文章,从跨学科的视角出发,分析了当前备受国际瞩目的人类基因编辑治理面临的挑战,指出现有人类基因编辑全球治理模式的局限性,并提出了具有现实可行性的全球治理改进方案。
该研究基于文献计量和全球调查的实证数据,发现相较于20世纪70年代重组-DNA技术的科学社群,当前人类基因编辑领域的科研工作者群体数量极为庞大,并且呈现高度的地域和文化多样化,从而导致现有的治理模式难以容纳科学界内外不同利益相关者的观点和意见。文章指出,人类基因编辑的全球治理应该超越由发达国家少数科学家群体主导的传统科技治理模式,从更广泛的全球治理实践中汲取经验,力争实现包容性的全球治理:首先,知名的学术期刊以及具有国际影响力的专业会议应更加开放和包容,为人类基因编辑相关的争议性治理问题搭建对话平台;其次,为人类基因编辑制定标准和规则的国际专业组织应该扩大其网络,从而涵盖更多历史上曾被忽略的国家/地区;此外,全世界科学和医学界的公共和私人资助机构应共同努力,推动集体行动来管理人类基因编辑。本研究对其他新兴技术的全球治理具有借鉴意义。《知识分子》获原文作者和PNAS授权,转载该文的中文译文。
撰文 | 俞晗之 薛澜
鲁道夫·巴兰古(Rodolphe Barrangou)
陈少威 黄颖
论文截图来自PNAS
近年来,许多人都在考虑如何更好地管理日益强大的基因编辑技术。自2015年以来,国际组织和科学机构已经发表了60多份声明、宣言和行为准则 [1]。2018年双胞胎露露和娜娜的出生引发了科学界、公众甚至法律机构的广泛关注,因为生物物理学研究者贺建奎改变了她们的艾滋病毒受体(CCR5)。此后,世界卫生组织成立了制定人类基因编辑治理和监督全球标准的专家咨询委员会(世界卫生组织委员会),科学界成立了人类生殖系基因编辑临床应用国际委员会(国际委员会)。
上述很多声明、宣言和行为准则报告都提出了针对人类基因编辑核心问题的治理方案,例如有关是否应该暂停人类可遗传基因编辑的基础研究和临床研究与应用。此外,这些报告还在一些议题上达成了共识,例如鼓励公众参与,对人类可遗传基因编辑的临床前和临床研究实施监管——尤其是要求透明披露实验进展、负责任地记录临床方案和病人的知情同意书。
尽管这些报告中讨论的大多数意见、准则和议题都值得重视,我们认为它们在指导人类基因编辑全球治理方面的有效性依然有限。由于基因编辑技术的发展速度迅猛,这项技术所涉及的利益相关者非常多元,现有的治理模式无法建立一个强有力、可信和持久的全球监管体系。我们认为,实现人类基因编辑有效全球治理的重要基础是承认并认真考虑来自世界各地科研工作者的差异化观点。
1 新兴生物技术全球治理的历史经验
当前人类基因编辑的全球治理模式与1975年的阿西洛玛声明(Asilomar statement)有诸多类似特征,后者被普遍认为实现了针对重组DNA技术的有效监管 [2]。阿西洛玛声明所体现的治理模式特点包括:
1. 治理主体是一个或几个国家的少数重要专家组成的委员会,并得到有影响力的国际组织或专业组织的支持;
2. 专家委员会提议的治理文本没有法律约束效力;
3. 治理文本的实施路径有两类,一是直接影响和限制科研工作者的行为,二是被政府法律监管采纳和纳入研究资助机构的政策体系。
上述治理模式的确有其优点。少数重要专家可以快速有效地达成治理共识,并且如果学术期刊和资助机构采用并遵守这样的指导方针,科学家也自然会遵守。此外,重要专家的强大关系网络通常能够使他们制定的治理文本影响政府的法律监管政策 [3]。例如,阿西洛玛会议的最终声明后来成为美国国家卫生研究院重组DNA咨询委员会的政策模板 [4]
然而,针对人类基因编辑的全球治理,全世界还远未在关键问题上达成共识,这从现有不同治理文本的内容分歧中就能够得到印证 [1]。例如,针对是否应该暂时禁止可遗传基因编辑这一问题,一些治理文本(如欧洲科学和新技术伦理小组制定的准则)建议广泛禁止 “人类胚胎或配子的基因编辑,因为这将导致人类基因的改变” [5],而另一些准则(如美国国家科学、工程和医学研究院制定的准则)则支持在某些特定条件下进行生殖系编辑 [6]。相关的讨论和争议不断,尤其在贺建奎基因编辑婴儿事件出现以后,该议题更是受到了国际社会的广泛关注 [7]。
值得注意的是,目前科学界内部对于是否应该暂停可遗传人类基因编辑也出现了不同意见。例如,埃里克·兰德(Eric Lander)[8] 等一些国际知名的科学家呼吁在国际层面出台完备的国际监管之前,在全球范围内暂停人类可遗传基因编辑的临床应用。相反,另一些著名的研究者则对此类建议表示反对,认为没有明确期限的暂停研究可能会阻碍科学的发展和技术的进步,这对于那些急迫需要依赖于此技术拯救生命的患者来说尤为重要 [9]。
尽管当年在制定阿西洛玛声明时,科学界就如何监管重组DNA技术也展开过激烈的辩论,但是这与目前全球科学界针对人类基因编辑技术的争论无法相提并论。确切地说,由少数科学家和科学组织领导的全球治理模式在人类基因编辑技术时代已经过时,现有的治理模式难以容纳科学界内外不同利益相关者的观点和意见,这同构建包容性治理框架的目标相悖。
阿西洛玛声明在1975年被提出之时,全世界仅有大约30名科研工作者在学术期刊上公开发表重组DNA技术相关的论文,这一数量远远少于出席阿西洛玛会议140名与会者的人数。此外,虽然发表有关重组DNA技术相关论文的作者人数在1978年增长到约900人,但他们从属的科研机构有70%以上都在美国。这反映了当时重组DNA技术的科学界规模小且集中,因此在阿西洛玛会议上的讨论相对来说易达成共识,进而更易说服科学界内部的其他人。
当前,人类基因编辑领域的科研工作者群体无论是在地理维度还是文化维度都非常多元。在2012年至2018年期间,超过8,000篇关于基因编辑的学术论文发表,其作者人数超过36,000位。来自全世界各大洲的94个国家/地区的约4,000个机构参与了基因编辑领域的研究(见表1)。随着基因编辑领域研究的推进,基因编辑技术在伦理层面的问题也加剧了利益相关者之间的意见分歧,尤其是对于具有不同文化背景、宗教观点和商业诉求的利益相关者。
表1 重组DNA(1972-1978)和基因编辑(2012-2018)的论文、国家/地区、机构和作者的全球分布情况
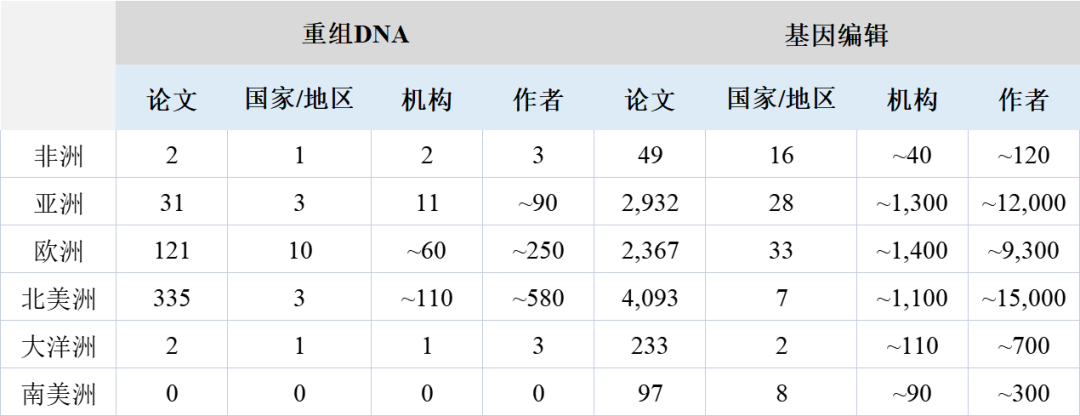
注:相关文献检索细节请参见附录信息。
2 来自全球调查的发现
进而我们对已经发表人类基因编辑技术相关学术论文的部分通讯作者进行了全球在线调查。我们向全球3,326名作者发出了调查问卷,收到了201份有效答复。诚然,我们的调查存在局限性,包括只调查通讯作者而可能带来的偏见以及相对较低的回复率(6%)。尽管如此,我们还是收集到了一些全球该领域科研工作者对现有治理文本的态度以及他们对人类体细胞和生殖细胞基因编辑以及增强功能编辑的基础研究和临床研究的意见。此外,我们还询问了他们对这一领域全球治理模式的偏好。
具体而言,我们选择了最具权威性的国际组织和专业组织制定的五项治理文本,调查全球科研工作者对这些文本的熟悉程度。大约40%的受访者说他们从未听说过这些文本,只有不到20%的受访者说他们详细阅读过。值得注意的是,我们发现科研工作者对一些关键问题的态度差异较大,大约30%的受访者希望暂停人类可遗传基因编辑领域的基础研究,而大约56%的受访者不希望暂停相关研究,还有14%的受访者持中立态度。科研工作者在这一问题上的态度也存在明显的地区差异,来自北美和欧洲的科研工作者态度最不保守,倾向于不希望暂停相关研究,来自亚洲的科研工作者多采取中立立场,而来自其他地区(如非洲和南美洲)的科研工作者则比较保守,倾向于主张暂停基础研究。
我们认为没有必要在全球范围内暂停所有的可遗传基因编辑基础研究,但的确需要对人类基因编辑的基础研究和临床试验施加具体限制。尤为重要的是,何时以及如何实施这些限制需要在全球范围内进行讨论,并在来自不同地区的多元利益相关者之间达成共识。
值得注意的是,多元利益相关者也包括许多在私营部门工作的科研工作者,这使得当前人类基因编辑的全球治理背景与阿西洛玛时期有很大差异。20世纪70年代大多数从事重组DNA技术研究的科研工作者都隶属公共科研机构,而如今许多从事基因编辑的科研工作者在知识产权方面存在利益冲突,或在商业公司担任顾问 [10],这些利益冲突并未在他们参与制定的治理指南中系统性的公开。
3 有关公众参与的探讨
现有关于人类基因编辑的全球治理探索都强调公众参与的重要性,例如国际委员会建议 “一个国家针对是否允许可遗传人类基因编辑做出决定之前,应当进行广泛的社会对话”,并认识到公众可以努力在全球范围内推进“负责任发展的国际合作” [11]。我们也赞同上述建议,即世界卫生组织和联合国教科文组织等国际组织应当肩负起评估责任,并提供公众如何参与的建议。我们特别赞赏世卫组织委员会制定的最新框架 [12],该框架强调了各种工具、机构和程序在人类基因编辑治理中的作用。然而,实现这些目标的关键性前提是全球科学界更具包容性的参与。
其一,有效的公众参与和讨论需要有关这一主题的基本信息,如体细胞和生殖细胞人类基因编辑之间的差异。这一条件在欠发达国家/地区尤其难以满足,因为这些国家/地区的教育和信息获取渠道比较有限。如果这些国家/地区的科研工作者能有更多机会在全球治理平台上开展对话,那么他们可以为本国或本地区带回国际前沿信息,从而为这些国家/地区的公共讨论提供参考。
其二,国际组织和专业组织建议的大多数治理准则和框架不具有法律权威或管辖权,因此,这些治理文本能否有效落实取决于国家监管机构是否愿意自愿遵循这些全球规则。如果能够有更多来自不同国家/地区的科研工作者和专业机构的代表参与全球政策制定,基于他们在全球平台上获得的一手信息和经验,他们可以作为政策制定的参与者为本国的政策制定提供信息,从而有助于形成更具权威性的本土治理框架。
其三,建立严格的全球治理规则需要全世界的利益相关者达成高度的共识。因此,全球科学界内部的包容性对话和达成全球共识的努力是不可或缺的。
4、迈向包容性全球治理
基于上述原因,我们认为人类基因编辑的全球治理应该超越生物技术领域的传统治理模式,从更广泛的全球治理实践中汲取经验。具体可以通过下列途径实现。
第一,知名的学术期刊以及具有国际影响力的专业会议应更加开放和包容,为人类基因编辑相关的争议性治理问题搭建对话平台。应邀请更多来自欠发达国家/地区的科研工作者在这些期刊上发表观点并在国际会议上发言,他们的意见需要得到认真的倾听和考虑。值得注意的是,目前CRISPRcon会议为分享不同意见提供了一个包容性平台,但是全世界大部分科研工作者和利益相关者还没有机会发表他们的真知灼见。以往全球治理的经验表明,确保声音被听到是改善全球治理的关键第一步。一个经典案例是联合国可持续发展目标(SDGs)的决策过程。为了就2015年至2030年期间实施的一套新的全球可持续发展目标达成共识,联合国为世界各地的机构和个人开发了各种沟通平台,获取他们的意见。例如,联合国可持续发展解决方案网络(UNSDSN)的建立是为了汇集来自所有地区和所有部门的全球专家,提出促进可持续发展的实际解决方案 [13]。联合国还发起了 “联合国——我的世界” 调查,邀请世界各地公众参与全球层面的政策制定 [14]。
第二,为人类基因编辑制定标准和规则的国际专业组织应该扩大其网络,从而涵盖更多历史上曾被忽略的国家/地区。例如,人类生殖系基因编辑临床应用国际委员会目前正在该领域发挥重要作用,但迄今为止只有10个国家的科学和医学研究院参与。当前国际干细胞研究学会等有影响力的国际专业组织的领导者大多来自发达国家,类似的国际专家委员会应该努力从欠发达国家吸引更多的顶尖专家加入。一个较好的模式是世界医学协会,它由110多个国家/地区的国家医师协会联合组成。多年来,该协会已经制定了许多成功的、具有包容性的标准和规则,包括具有影响力的研究伦理规范《赫尔辛基宣言》。
第三,全世界科学和医学界的公共和私人资助机构应共同努力,推动集体行动来管理人类基因编辑。如果有影响力的资助者能够认可加强伦理审查、问责制和透明度的基本原则和标准,那么全世界大量已经获得或希望获得资助的科研工作者就有动力去关注这些原则和标准。人类基因计划说明了资助机构在打造领域精神方面的重要影响 [15]。1996年,维康基金会(Wellcome Trust)赞助了一个由美国医学研究院协调的人类基因计划各国工作组专家参与的会议。这次会议的结果是著名的《百慕大协议》,其中科学家们承诺 “尽快” 发布实验室获得的人类DNA序列数据,并将他们的数据提交到一个公共数据库。由于这些研究资助者拥有巨大权力,在没有任何法律授权的前提下,这一规则成功地重塑了该领域的数据政策实践 [16]。
当前,新兴生物技术正在迅猛发展。技术发展不再是少数领先的学术机构和少数创业先驱的专利,CRISPR技术兴起所推动的基因编辑技术应用普遍化,就是一个例证。因此,由少数人治理所有人的做法不再适用,也不可接受。上述建议的每一种全球治理路径都取得了一些历史性成功,并有可能改善人类基因编辑的全球治理。我们需要将这些工具形成组合拳。由学术期刊、资助机构和国际专业组织各自推动的标准和协议可以相互强化。个人和组织在其中发挥关键作用,成为连接不同治理路径的桥梁。人类基因编辑的全球治理迫切需要全球科学界的智慧,以及相关领域和感兴趣的公众参与。
“ 作者简介
本文的共同第一作者为浙江大学公共管理学院百人计划研究员俞晗之,清华大学公共管理学院/苏世民学院教授薛澜,共同通讯作者为湖南大学公共管理学院教授陈少威,武汉大学信息管理学院副教授黄颖,北卡罗来纳州立大学食品、生物加工和营养科学系教授鲁道夫·巴兰古(Rodolphe Barrangou)对本文亦有贡献。
利益冲突声明:
鲁道夫·巴兰古(Rodolphe Barrangou)是 Intellia Therapeutics、Locus Biosciences、TreeCo、Ancilia Biosciences 和 CRISPR Biotechnologies 的联合创始人,并且是 Caribou Biosciences 和 Inari Ag 的股东。
版权声明
原文2021年11月23日发表于《美国科学院院刊》第118卷47期,原标题为“Toward inclusive global governance of human genome editing”。中文版由作者翻译,PNAS不为翻译的准确性负责。
引用链接:Yu, H., Xue, L., Barrangou, R., Chen, S., & Huang, Y., (2021). Toward inclusive global governance of human genome editing. Proceedings of the National Academy of Sciences, 118 (47), e2118540118;
参考文献:(上下滑动可浏览)
1. C. Brokowski, Do CRISPR germline ethics statements cut it? CRISPR J. 1, 115-125 (2018).
2. P. Berg, D. Baltimore, S. Brenner, R. O. Roblin, M. F. Singer, Summary statement of the Asilomar conference on recombinant DNA molecules. Proc. Natl. Acad. Sci. U.S.A. 72, 1981-1984 (1975).
3. D. Gregorowius, N. Biller-Andorno, A. Deplazes-Zemp, The role of scientific self-regulation for the control of genome editing in the human germline: The lessons from the Asilomar and the Napa meetings show how self-regulation and public deliberation can lead to regulation of new biotechnologies. EMBO Rep. 18, 355-358 (2017).
4. D. S. Fredrickson,"Asilomar and recombinant DNA: The end of the beginning" in Biomedical Politics, K. E. Hanna, Ed. (The National Academies Press, Washington, DC, 1991), pp. 258-298.
5. European Group on Ethics in Science and New Technologies, Opinion on the Ethics of Genome Editing (Publications Office of the European Union, Luxembourg, 2021)
6. National Academies of Sciences, Engineering and Medicine, Human Genome Editing: Science, Ethics, and Governance (The National Academies Press, Washington, DC, 2017).
7. H. C. O'Neill, Clinical germline genome editing: When will good be good enough? Perspect. Biol. Med. 63, 101-110 (2020).
8. E. S. Lander et al., Adopt a moratorium on heritable genome editing. Nature 567, 165-168 (2019).
9. E. Y. Adashi, I. G. Cohen, Heritable genome editing: Is a moratorium needed? JAMA 322, 104-105 (2019).
10. P. Berg, Meetings that changed the world: Asilomar 1975: DNA modification secured. Nature 455, 290-291 (2008).
11. National Academy of Medicine, National Academy of Sciences, and the Royal Society , Heritable Human Genome Editing (The National Academies Press, Washington, DC, 2020).
12. WHO Expert Advisory Committee on Developing Global Standards for Governance and Oversight of Human Genome Editing, Human Genome Editing: A Framework for Governance (World Health Organization, Geneva, Switzerland, 2021).
13. Council of the Sustainable Development Solutions Network (SDSN), An Action Agenda for Sustainab le Development. stainable-Development-FINAL.pdf. Accessed 24 September 2021.
14. Sustainable Development Goals Partnerships Platform, My World 2030. https://sustainabledevelopment. Accessed 24 September 2021.
15. E. Marshall, Bermuda rules: Community spirit, with teeth. Science 291, 1192 (2001).16. J. Kaye, C. Heeney, N. Hawkins, J. de Vries, P. Boddington, Data sharing in genomics—Re-shaping scientific practice. Nat. Rev. Genet. 10, 331-335 (2009).
附录材料
“迈向包容性的人类基因编辑全球治理”
俞晗之,薛澜,鲁道夫·巴兰古(Rodolphe Barrangou),陈少威,黄颖
本研究中使用的两个数据集按照下列两个步骤来收集。首先,我们收集了Medline和Web of Science的科学引文索引扩展版(SCIE)与社会科学引文索引(SSCI)收录的所有与基因编辑和重组DNA有关的文献数据,基于此我们可以了解基因编辑研究和重组DNA领域的研究现状。其次,我们通过提取基因编辑论文的通讯作者信息来进行在线问卷调查,问卷调查结果构成了另一个数据集,用以分析科学家对现有指南的了解以及他们对指南中广泛涉及的特定问题的态度。
● 人类基因编辑和重组DNA相关文献的检索策略
我们首先从PubMed ()上检索相关文献数据作为初步数据集,PubMed可以访问MEDLINE这一权威的生物医学文献数据库,它涵盖了生命科学和生物医学中的基因编辑和重组DNA的相关研究。而科睿唯安(Clarivate Analytics)下属的Web of Science()中的文献著录数据相对更为全面且质量更高。因此,我们从初步数据集中提取了PubMed IDs,并利用这些IDs在Web of Science平台上进行二次搜索,以补充和完善数据信息。因此,最终的数据集只包括同时被PubMed和Web of Science中的SCIE/SSCI收录的文献记录。
不同于先前研究(Huang et. al, 2019)中使用文本主题词来检索文献,此次我们使用医学主题词(Medical Subject Headings,MeSH)来获取相应的文献数据。MeSH是由美国国家医学图书馆(NLM)创建和更新,用以辅助在PubMed中的搜索。具体的检索策略与结果如附表1中所示。值得一提的是,我们没有在搜索查询中引入“人类”一词来加以限定,这主要是基于如下两个考虑:其一,由于我们将搜索范围限制在生命科学和生物医学主题上,在我们目标范围之外的大多数文献记录已经被排除。其二,关于动物基因编辑的研究部分包括了人类基因的研究,或者说未来能够被扩展到人类基因的研究,这使得我们难以准确区分人类和动物基因编辑的研究。
此外,在文献著录数据中,一些文献缺少作者的机构归属等字段信息,尤其是2008年以前的出版物,因此重组DNA的相关统计数值可能会高一些,但这不会影响总体趋势。同时,由于名称的模糊性问题,我们对于作者和机构的统计只提供了一个估计值,因为同一作者的名字可能有不同的写法,不同的作者可能共用同一个名字;机构名字可能在不同时期发生演变,机构的隶属关系也难以准确区分。
附表1 基因编辑和重组DNA相关的出版物的文献检索策略与结果

注:时间跨度=1900-2018,检索日期为2020年2月17日。
● 全球调查设计
我们对人类基因编辑领域的的通讯作者进行了全球在线调查。该调查基于两个专业的在线调查平台SurveyMonkey()和问卷网()展开。在2019年3月24日至2019年6月12日期间,共发送了五轮共计3326封邮件。截至2019年6月12日,我们共收到201个有效样本,回复率为6.04%。
该调查主要包括三个部分:第一部分衡量了科学家对现有规范准则的了解程度,第二部分旨在评估科学家对准则中广泛涉及的具体议题的态度,第三部分搜集了科学家对如何改善人类基因编辑全球治理的意见。在下文中,我们主要报告与本文最直接关联的两个调查问题(即Q1和Q6)的结果。
在Q1中,我们衡量了科学家对五项重要准则的了解程度,包括欣克斯顿集团(Hinxton Group)在2015年发表的《关于基因编辑技术和人类胚胎遗传修改的声明》;联合国教科文组织在2015年发表的《国际生物伦理委员会关于更新其对人类基因和人权的反思的报告》;第二届人类基因编辑国际峰会组织委员会在2018年发表的《论人类基因编辑II》;Nuffield生物伦理学委员会于2018年出版的《基因编辑与人类生殖:社会和伦理问题》;以及国家科学、工程和医学研究院于2017年出版的《人类基因编辑:科学、伦理和治理》。选择这五项准则的主要依据包括两个方面:1)它们在近期的出版物和会议中被广泛地讨论;2)它们涉及了各种类型的全球规则制定者,如政府间组织(如联合国教科文组织)、国际非政府组织(如欣克斯顿集团)、国家科学委员会(如英国纳菲尔德生物伦理委员会,美国国家科学、工程和医学研究院)和国际科学会议委员会(如第二届人类基因编辑国际峰会组织委员会)。受访者对于该问题回答的描述性统计结果如附表2中所示。
附表2 受访者报告的对准则的熟悉程度分布情况
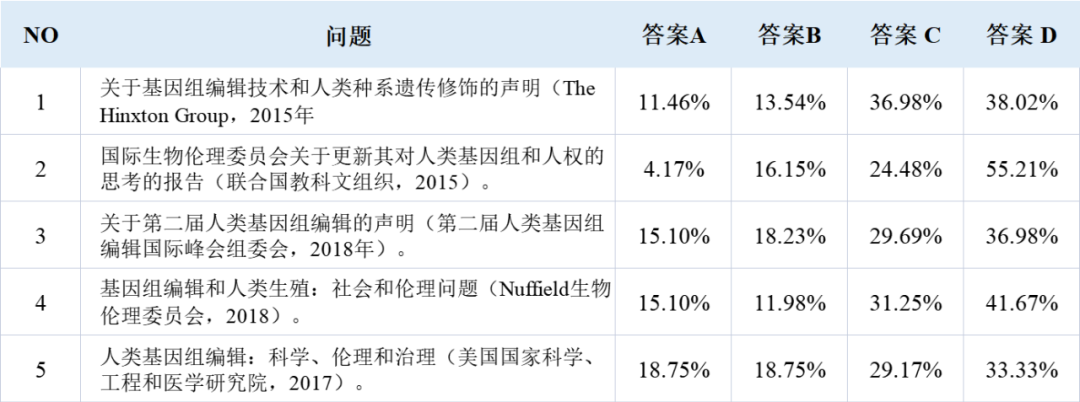
注:问题的具体陈述和选项如下:请告诉我们您对下面的报告和声明的熟悉程度。A“我已经详细阅读了该报告”;B“我已经简单浏览了该报告”;C“我没有阅读该报告,但知道其主要内容和主要观点”;D“我没有听说过该报告”。
在Q6中,我们设置的问题如下:“你是否同意暂时禁止所有针对人类可遗传基因编辑基础研究活动对是必要的?”受访者被要求从五个选项中选择,其中“1-5”分别表示非常不同意、不同意、中立、同意、非常同意五个选项。这五个选项的支持率分别为21.7%、34.4%、12.2%、14.3%和16.4%。此外,我们还计算了各类回复的平均值,以了解各地区对这一问题的态度(见附表3)。单向方差分析显示组间(地区)差异显著(在0.05水平)。
附表3 不同地区的受访者对Q6的态度报告
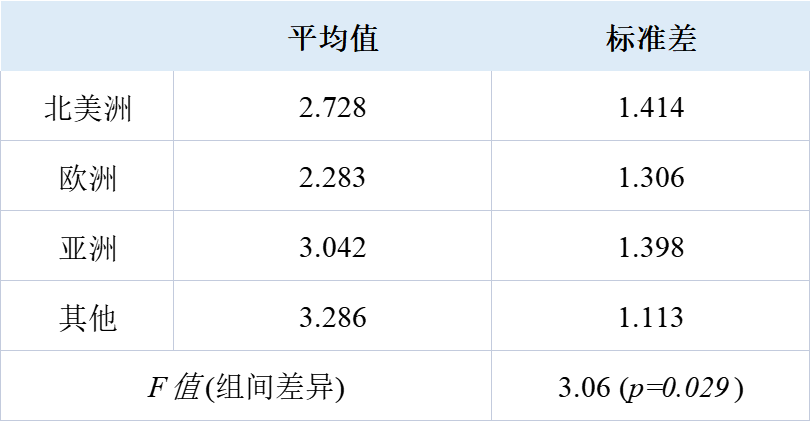
参考文献:
Y.Huang, A. Porter, Y. Zhan g, R. Barrangou, Collaborative networks in gene editing. Nat.Biotechnol.37, 1107-1109 (2019).
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 